Protective Effects of Propolis Ethanol Extract on Mouse Aortic Endothelial Cells Injury
-
摘要: 目的:探究蜂胶乙醇提取物(ethanol extracts of propolis,EEP)对脂多糖(lipopolysaccharide,LPS)诱导的小鼠主动脉内皮细胞(mouse aortic endothelial cell,MAEC)炎症因子损伤的保护作用。方法:将细胞分为对照组,LPS模型组,蜂胶低(2.5 μg/mL)、中(5 μg/mL)、高(10 μg/mL)剂量组。采用CCK-8检测MAEC的细胞增殖率,ELISA酶联免疫吸附实验测定MAEC炎症细胞中TNF-α、IL-6的含量,Western Blot法测定MAEC炎症细胞中ICAM-1、VCAM-1、MCP-1的表达水平。结果:与对照组相比,LPS组MAEC的细胞增殖率极其显著降低(P<0.001),ICAM-1、VCAM-1、MCP-1、TNF-α以及IL-6的水平极其显著升高(P<0.001)。经不同浓度EEP处理后,MAEC的细胞增殖率显著上升(P<0.05或P<0.01),TNF-α、IL-6的含量以及ICAM-1、VCAM-1、MCP-1表达水平降低,各蜂胶组与LPS组相比均有显著性差异(P<0.01或P<0.001)。结论:EEP能够抑制LPS诱导的MAEC中炎症因子的表达,对血管内皮细胞具有保护作用。Abstract: Objective: The aim of this study was to investigate the protective effects of ethanol extracts of propolis (EEP) on mouse aortic endothelial cells (MAEC) from injury induced by lipopolysaccharide (LPS). Methods: Cell proliferation rate was determined by CCK-8. Then MAEC were divided into the blank group, LPS model group, low-dose (2.5 μg/mL), middle-dose (5 μg/mL), and high-dose (10 μg/mL) groups of EEP. The TNF-α and IL-6 levels were evaluated by ELISA. The expression levels of ICAM-1, VCAM-1 and MCP-1 were measured by Western Blot. Results: Compared with the control group, the cell proliferation rate of MAEC in the LPS group was extremely significant reduced (P<0.001), and the levels of ICAM-1, VCAM-1, MCP-1, TNF-α and IL-6 were extremely significant increased (P<0.001). The cell proliferation rate of EEP groups increased significantly (P<0.05 or P<0.01), and the content of TNF-α, IL-6 and the expression levels of ICAM-1, VCAM-1, and MCP-1 decreased compared with these of LPS group. There were significant differences between each propolis group and LPS group (P<0.01 or P<0.001). Conclusion: EEP could effectively inhibit LPS-induced the expression of inflammatory factors in MAEC, and it has the effect of protecting endothelial cells.
-
动脉粥样硬化(atherosclerosis,AS)是目前常见的心脑血管疾病发病的主要原因。它的发生机理主要是代谢障碍导致脂质在血管中积累,形成斑块,使得动脉腔隙变窄,进而导致组织或器官的缺血或坏死[1-2]。血管内皮细胞的损伤是动脉粥样硬化的关键环节,血管内皮细胞的损伤会分泌大量的促炎因子和黏附因子,导致炎症反应的发生,进而加速AS进程[3-4]。
蜂胶是工蜂采集胶源植物的树脂与其上颚腺、蜡腺等分泌物混合而成的具有黏性的固体胶状物[5]。蜂胶的化学成分因胶源植物的不同而不同,其中,中国蜂胶主要的胶源植物为杨树属,目前已从中国蜂胶中鉴定出300多种化学成分,包括酚酸类、黄酮类、萜烯类、醇类、香豆素类和脂类等[6-8]。课题组前期的实验已分析过中国蜂胶的化学成分,主要有乔松素、短松叶素、高良姜素、白杨素等,含量最多的化学成分为黄酮类化合物,占71.92% [9]。现代药理研究表明,蜂胶具有抗微生物,抗肿瘤,调节血糖,抗氧化以及抗炎活性[10-13]。有研究表明蜂胶具有明显的抗炎作用,可以预防动脉粥样硬化,减少血脂,影响血管生成,并在预防和治疗心血管疾病中发挥重要作用[14-15]。Kitamura等[16]的证明蜂胶可以诱导M1型巨噬细胞向髓源性抑制细胞(MDSC)分化,有效减少M1细胞,从而抑制M1分泌重要的促炎细胞因子,如TNF-α和IL-6,将炎症过程转向消退。蜂胶提取物能降低饲喂高脂饮食的ApoE-/小鼠的总胆固醇(TC)、甘油三酸酯(TG)、非高密度脂蛋白胆固醇(non-HDL-C)的水平以及炎症因子IL-6和IL-17的产生[17]。蜂胶中的主要成分白杨素也可以减轻内皮细胞间的黏附,并降低IL-1β损伤的人脐静脉内皮细胞中炎症因子的表达[18]。
本实验用脂多糖(lipopolysaccharide,LPS)刺激小鼠主动脉内皮细胞构建损伤模型,研究蜂胶乙醇提取物(ethanol extracts of propolis,EEP)对LPS诱导的小鼠主动脉内皮细胞内炎症因子的影响,为治疗心脑血管疾病提供新的思路和理论依据。
1. 材料与方法
1.1 材料与仪器
蜂胶 胶源植物杨树属,−20 ℃保存,福建省神蜂科技开发有限公司;CP-M075小鼠主动脉内皮细胞、CM-M075小鼠主动脉细胞完全培养基 普诺赛生命科技有限公司;A3160802胎牛血清 赛默飞世尔科技有限公司;胰酶-EDTA、PBS、D-Hanks 吉诺生物医药技术有限公司;小鼠IL-6、TNF-α ELISA试剂盒 欣博盛生物科技有限公司;一抗GAPDH、ICAM-1、VCAM-1、MCP-1兔抗 abcam公司;二抗 HRP-Goat anti Rabbit Elabscience公司。
SCO6WE CO2恒温培养箱 SHEL LAB实验器材有限公司;SW-CJ-1FD洁净工作台 苏净安泰公司;IX51倒置显微镜 OLYMPUS有限公司;DR-200Bs酶标检测仪 无锡华卫德朗仪器有限公司;TD6低速离心机 湖南平凡科技有限公司。
1.2 实验方法
1.2.1 EEP的制备
参照Xu等[9]的方法进行EEP的制备:蜂胶溶于70%乙醇(v/v),室温浸泡2 d,60 ℃,20 min,40 kHz超声提取3次,得到的混合液离心,弃上清,真空浓缩至溶剂蒸发,储于4 ℃备用。
1.2.2 细胞复苏与培养
将冻有MAEC的细胞冻存管从液氮中拿出,37 ℃水浴中快速解冻后迅速转移至装有3 mL培养液的5 mL离心管中,1400 r/min离心4 min。离心后倒掉上清液,加1 mL培养基重悬细胞,转移至含有3 mL培养基的细胞培养瓶中进行细胞培养,培养条件为5%的CO2,37 ℃。
1.2.3 药物配制及细胞分组
用小鼠主动脉细胞完全培养基溶解LPS,配制成终浓度为10 μg/mL的LPS药液;用小鼠主动脉细胞完全培养基溶解EEP,根据后续实验配制成相应浓度的EEP药液。使用处于生长对数期(细胞状态好)的细胞进行实验,浓度调整为1×105个/mL,接种于96孔板中,分为五组,空白组、LPS模型组,蜂胶低剂量组(LPS+2.5 μg/mL EEP)、中剂量组(LPS+5 μg/mL EEP)、高剂量组(LPS+10 μg/mL EEP),每组设置5个复孔。空白组给予100 μL的完全培养基,LPS模型组给予10 μg/mL的LPS药液,蜂胶低、中、高剂量组给予10 μg/mL 的LPS和2.5、5、10 μg/mL的EEP药液共培养,培养条件37 ℃,5%的CO2。
1.2.4 细胞增殖率检测
采用CCK-8检测MAEC的增殖活性:按照1.2.3的方式培养细胞,24 h后将10 μLCCK-8溶液添加到每个孔中,并在37 ℃的5% CO2中培养4 h。然后,在450 nm处测量吸光度。通过以下公式计算细胞增殖率:
细胞增殖率=实验孔的吸光度/对照孔的吸光度
1.2.5 ELISA实验测定TNF-α、IL-6的含量
将处理后的各组细胞样品和ELISA试剂盒取出平衡至室温。配制标准品溶液并绘制标准曲线。随后进行蛋白测定。空白孔中加入标准品,其余孔中加入待测样品(100 μL/孔),封板,37 ℃孵育90 min。洗板5次。依次加入生物素化抗体工作液,封孔,37 ℃孵育60 min。洗板5次。加入酶结合物工作液,封板,37 ℃避光孵育30 min。洗板,加入显色底物37 ℃孵育15 min。加入终止液100 μL/孔,混匀后立即在3 min内用酶标仪测量OD450值,每组三个平行。随后将OD值带入标准曲线中,计算得到相对含量。
1.2.6 Western Blot法测定ICAM-1、VCAM-1、MCP-1的表达水平
经处理后的各组细胞用TBS缓冲液洗涤3次,加入总蛋白提取试剂裂解3~5 min。收集细胞于离心管冰浴30 min后4 ℃12000 g离心5 min。总蛋白浓度用BCA试剂盒测定,每组三个平行。处理好的样品以每组上样量10 μL开始电泳,浓缩胶电压80 V,分离胶电压130 V,待条带到玻璃板底部时结束电泳。随后将样品转移至PVDF膜上,放入适量5%脱脂奶粉中,振荡封闭1 h。然后与一抗封闭4 ℃孵育过夜。TBST洗涤5次,每次5 min。再于二抗中孵育1 h,TBST洗涤5次,每次5 min。随后进行发光检测,Alpha Ease FC软件处理系统分析目标带的光密度值。结果以与上样对照甘油醛-3-磷酸脱氢酶(GAPDH)[18]的光密度值的比值表示。
1.3 数据处理
采用SPSS 26.0统计软件进行统计分析,Graph Pad Prism 8.0.2作图,所有数据以均数±标准差(
2. 结果与分析
2.1 EEP对MAEC细胞增殖的影响
结果如图1所示,LPS模型组MAEC的细胞增殖率下降21%,与空白组相比差异极其显著(P<0.001),经不同浓度的EEP处理后MAEC的增殖率均有上升,与LPS组相比,10 μg/mL EEP组差异显著(P<0.05),2.5 μg/mL 和5 μg/mL EEP差异极显著(P<0.01)。
2.2 EEP对MAEC细胞中IL-6、TNF-α的影响
结果如图2所示,空白对照组中,IL-6、TNF-α有极少量的表达,经LPS刺激后的MAEC中IL-6、TNF-α的表达明显升高,其中IL-6由空白组的29.950 pg/mL升高到126.437 pg/mL升高至原来的4.22倍,TNF-α由空白组的37.407 pg/mL升高到123.613 pg/mL,升高至原来的3.3倍,与空白对照组相比差异极其显著(P<0.001),EEP的处理极其显著降低了IL-6、TNF-α的表达(P<0.001),且呈剂量依赖性。
2.3 EEP对MAEC细胞中ICAM-1、VCAM-1、MCP-1表达的影响
结果如图3所示,空白对照组的MAEC中ICAM-1、VCAM-1、MCP-1均有少量表达,当LPS刺激细胞后ICAM-1、VCAM-1、MCP-1的表达均有极其显著的上升(P<0.001)。经不同浓度的EEP处理后,ICAM-1、VCAM-1、MCP-1均有明显下降,且它们的表达量随着EEP浓度的增加而降低,各蜂胶给药组与LPS组均有不同程度的显著差异(P<0.01或P<0.001)。
3. 讨论
LPS是革兰氏阴性菌细胞壁的主要成分,进入血液的LPS可与单核巨噬细胞、内皮细胞等的细胞膜的受体相结合,通过胞内的信号转导刺激机体细胞合成和释放多种炎症因子,从而诱导内皮细胞的损伤[19]。当内皮细胞受到LPS、ox-LDL等刺激时,可释放多种细胞因子刺激平滑肌细胞增殖,内皮细胞与平滑肌细胞相互作用推动血管损伤和动脉粥样硬化的发展[20]。
肿瘤坏死因子TNF-α是一种由巨噬细胞和单核细胞产生的促炎因子,在机体的炎症反应和免疫反应中起重要的作用[21]。之前的研究构建了LPS损伤的MAEC模型,证实了LPS可以刺激MAEC产生TNF-α引发炎症,TNF-α还可以诱导黏附分子的表达与IL-6、IL-8等细胞因子的激活,使损伤的内皮细胞通透性增加、脂质更容易穿过血管膜造成脂质堆积,形成斑块,在炎症反应和AS的发展过程中起关键性作用[22-24]。IL-6也属于促炎因子,它可以通过激活免疫系统,募集单核细胞,刺激内皮细胞和平滑肌细胞表达,抑制调节性T细胞分化和凋亡,起到促炎作用[25-26]。本研究中Elisa的检测结果表明LPS的刺激可以大量增加MAEC中TNF-α和IL-6的释放,经EEP处理后MAEC中的TNF-α和IL-6的表达量与LPS模型组相比均有明显下降。由此可见,EEP可以减少血管内皮细胞中炎症反因子的分泌,起到抗炎作用保护内皮细胞免受损伤。
ICAM-1和VCAM-1是免疫球蛋白超家族中的黏附分子,在受损部位介导白细胞与血管内皮细胞的黏附[27]。正常生理状况下,ICAM-1在血管内皮细胞中的表达水平极低,在细胞损伤或肿瘤坏死因子TNF-α、IL-6等炎症介质的刺激下其表达水平上调,使白细胞和单核细胞不断附着内皮细胞于[28-29],VCAM-1也能在炎症刺激的内皮细胞中过量表达,与其配体VLA-4共同作用,将炎性细胞更牢固地附着于血管内皮细胞上[30]。之前的研究表明去除 ICAM-1 后,高脂喂养的小鼠 AS 斑块总量与对照组相比减少了50%左右[31],研究证明
ApoE小鼠 的VCAM-1基因沉默会减少AS斑块的体积及斑块内脂质的含量[32]。两者的高表达是内皮细胞损伤的重要标志,在动脉粥样硬化的发展的过程中也起着重要作用。本实验中LPS的刺激下ICAM-1和VCAM-1的表达显著增加,而EEP处理能有效降低受损MAEC中ICAM-1和VCAM-1的表达,说明EEP可以减少炎性细胞的黏附,从而减轻内皮细胞的损伤。 细胞单核细胞趋化蛋白MCP-1是化学趋化因子β亚组代表,主要在炎症细胞和内皮细胞表达,具有募集和活化特定蛋白细胞的功能[33]。LPS对MCP-1的影响主要通过激活Pyk2活化 p38 MAPK激酶,P38MAPK激酶进而激活转录因子NF-κB来驱动的[34]。受损的内皮细胞中MCP-1与其受体结合可以引导单核细胞的聚集并在黏附因子的作用下黏附于损伤部位,导致炎症反应加重[35-36]。本实验Western Blot结果表明LPS的刺激可引起MAEC中MCP-1的表达明显增加,经EEP处理后可以有效降低MCP-1的表达,说明EEP有抑制炎症处单核细胞的聚集,减轻血管内皮细胞的炎症反应。
4. 结论
综上所述,LPS的刺激可以诱导MAEC炎症的发生并降低其细胞活性。EEP能降低促炎因子IL-6、TNF-α的含量,抑制黏附因子ICAM-1、VCAM-1和趋化因子MCP-1的表达,抑制炎性细胞在血管内膜的迁移及其在病变部位的趋化作用,减少单核细胞的黏附,缓解血管内膜的炎性损伤,发挥了良好的抗炎作用。
-
-
[1] 胡钟竞, 王杰. 动脉粥样硬化形成机制及影响因素研究概况[J]. 临床医药文献电子杂志,2020,50(7):197−198. [2] Taleb Soraya. Inflammation in atherosclerosis[J]. Archives of Cardiovascular Diseases,2016,109(12):708−715. doi: 10.1016/j.acvd.2016.04.002
[3] Small D M. Cellular mechanisms for lipid deposition in atherosclerosis (first of two parts)[J]. The New England Journal of Medicine,1977,297(16):873−877. doi: 10.1056/NEJM197710202971608
[4] 刘俊田. 动脉粥样硬化发病的炎症机制的研究进展[J]. 西安交通大学学报(医学版),2015,36(2):141−152. [5] 全国蜂产品标准化工作组(SAC/SWG 2). GB/T 24283-2018蜂胶[S]. 国家市场监督管理总局, 中国国家标准化管理委员会, 2018. [6] Huang Y L, Huang Z Q, Watanabe C, et al. Combined direct analysis in real-time mass spectrometry (DART-MS) with analytical pyrolysis for characterization of Chinese crude propolis[J]. Journal of analytical and applied pyrolysis,2019,137:227−236. doi: 10.1016/j.jaap.2018.11.030
[7] 张婷婷. GC-MS和紫外光谱法分析中国蜂胶乙醇提取物[D]. 南昌: 南昌大学, 2017. [8] Santos L M, Fonseca M S, Sokolonski Ana R, et al. Propolis: Types, composition, biological activities, and veterinary product patent prospecting[J]. Journal of the Science of Food and Agriculture,2020,100(4):1369−1382. doi: 10.1002/jsfa.10024
[9] Xu X L, Pu R X, Li Y J, et al. Chemical compositions of propolis from china and the united states and their antimicrobial activities against Penicillium notatum[J]. Molecules,2019,24(19):3576. doi: 10.3390/molecules24193576
[10] Okińczyc P, Paluch E, Franiczek R, et al. Antimicrobial activity of Apis mellifera L. and Trigona sp. propolis from Nepal and its phytochemical analysis[J]. Biomedicine & Pharmacotherapy,2020,129:110435.
[11] Zhang H, Fu Y Y, Niu F G, et al. Enhanced antioxidant activity and in vitro release of propolis by acid-induced aggregation using heat-denatured zein and carboxymethyl chitosan[J]. Food Hydrocolloids,2018,81:104−112. doi: 10.1016/j.foodhyd.2018.02.019
[12] Annie R P, Mikhael H F, Rodrigues T, et al. Green propolis increases myeloid suppressor cells and CD4 + Foxp3 + cells and reduces Th2 inflammation in the lungs after allergen exposure[J]. Journal of Ethno Pharmacology,2020,252:112496.
[13] Shi Y Z, Liu Y C, Zheng Y F, et al. Ethanol extract of chinese propolis attenuates early diabetic retinopathy by protecting the blood retinal barrier in streptozotocin induced diabetic rats[J]. Journal of Food Science,2019,84(2):358−369. doi: 10.1111/1750-3841.14435
[14] Lima L D C, Andrade S P, Campos P P, et al. Brazilian green propolis modulates inflammation, angiogenesis and fibrogenesis in intraperitoneal implant in mice[J]. BMC Complement Altern Med,2014,14:177. doi: 10.1186/1472-6882-14-177
[15] Franchin M, Freires I A, Lazarini J G, et al. The use of Brazilian propolis for discovery and development of novel anti-inflammatory drugs[J]. European Journal of Medicinal Chemistry,2018,153:49−55. doi: 10.1016/j.ejmech.2017.06.050
[16] Kitamura H, Saito K, Fujimoto J, et al. Brazilian propolis ethanol extract and its component kaempferol induce myeloid-derived suppressor cells from macrophages of mice in vivo and in vitro[J]. BMC complementary medicine and therapies,2018,18(1):138. doi: 10.1186/s12906-018-2198-5
[17] Fang Y, Sang H, Yuan N, et al. Ethanolic extract of propolis inhibits atherosclerosis in Apo E-knockout mice[J]. Lipids in Health and Disease,2013,12:123. doi: 10.1186/1476-511X-12-123
[18] 赵胜男. 白杨素通过抑制NF-κB信号通路缓解血管内皮炎症[D]. 武汉: 华中科技大学, 2019. [19] Dauphinee S M, Karsan A. Lipopolysaccharide signaling in endothelial cells[J]. Laboratory Investigation,2006,86(1):9−22. doi: 10.1038/labinvest.3700366
[20] 任德成. 内皮细胞损伤的机制及保护药物的筛选研究[D]. 北京: 中国协和医科大学, 2002. [21] Zhong Y, Liu C, Feng J, et al. Curcumin affects ox-LDL-induced IL-6, TNF-α, MCP-1 secretion and cholesterol efflux in THP-1 cells by suppressing the TLR4/NF-κB/miR33a signaling pathway[J]. Experimental and Therapeutic Medicine,2020,20(3):1856−1870.
[22] 周信, 张小荣, 张秋燕, 等. 生半夏及其炮制品对小鼠主动脉内皮细胞炎性因子分泌的影响[J]. 中国实验方剂学杂志,2013,19(10):261−265. [23] Klinghammer L, Urschel K, Cicha K, et al. Impact of telmisartan on the inflammatory state in patients with coronary atherosclerosis Influence on IP-10, TNF-α and MCP-1[J]. Cytokine,2013,62(2):290−296. doi: 10.1016/j.cyto.2013.02.001
[24] Zhang Y, Yang X, Bian F, et al. TNF-α promotes early atherosclerosis by increasing transcytosis of LDL across endothelial cells: crosstalk between NF-κ B and PPAR-γ[J]. Journal of Molecular and Cellular Cardiology,2014,72:85−94. doi: 10.1016/j.yjmcc.2014.02.012
[25] 张伟洁, 郑宏. IL-6介导免疫炎性反应作用及其与疾病关系的研究进展[J]. 细胞与分子免疫学杂志,2017,33(5):699−703. [26] 解慧梅, 胡格, 索占伟, 等. 人参皂甙Rb1和黄芪多糖对微血管内皮细胞分泌NO、IL-6和TNF-α的影响[J]. 畜牧兽医学报,2006(9):903−907. doi: 10.3321/j.issn:0366-6964.2006.09.013 [27] 郭建恩, 高飞, 胡亚涛, 等. 瓜蒌薤白半夏汤对动脉粥样硬化小鼠炎症因子、ICAM-1、VCAM-1表达的影响[J]. 暨南大学学报(自然科学与医学版),2017,38(3):234−239. [28] 黄志广. 重组SAK-HV对小鼠主动脉内皮细胞的作用及机制研究[D]. 南宁: 广西医科大学, 2016. [29] Kan I, Takeshi K, Hiroyuki I, et al. Induction of ICAM-1 and VCAM-1 on the mouse lingual lymphatic endothelium with TNF-α[J]. Acta Histochemica et Cytochemica,2008,41(5):115−120. doi: 10.1267/ahc.08017
[30] Liang C J, Lee C W, Sung H C, et al. Magnolol reduced TNF-α-induced vascular cell adhesion molecule-1 expression in endothelial cells via JNK/p38 and NF-κB signaling pathways[J]. The American Journal of Chinese Medicine: An International Journal of Comparative Medicine East and West,2014,42(3):619−37.
[31] Nageh M F, Sandberg E T, Marotti K R, et al. Deficiency of inflammatory cell adhesion molecules protects against atherosclerosis in mice[J]. Arteriosclerosis, Thrombosis, and Vascular Biology,1997,17(8):1517−1520. doi: 10.1161/01.ATV.17.8.1517
[32] 穆伟. 动脉粥样硬化中血管细胞粘附分子-1的表达与基因干预研究[D]. 济南: 山东大学, 2015. [33] Lin J T, Kakkar V, Lu X J. Impact of MCP-1 in atherosclerosis[J]. Current Pharmaceutical Design,2014,20(28):4580−4588. doi: 10.2174/1381612820666140522115801
[34] Appakkudal R A, Bradley R, Ganju R K. LPS-induced MCP-1 expression in human microvascular endothelial cells is mediated by the tyrosine kinase, Pyk2 via the p38 MAPK/NF-κ B-dependent pathway[J]. Molecular immunology,2009,46(5):962−968. doi: 10.1016/j.molimm.2008.09.022
[35] Zhang Y J, Catherine A E, Barrett J R. MCP-1: Structure/Activity Analysis[J]. Methods,1996,10(1):93−103. doi: 10.1006/meth.1996.0083
[36] Chang M L, Guo F, Zhou Z D, et al. HBP induces the expression of monocyte chemoattractant protein-1 via the FAK/PI3K/AKT and p38 MAPK/NF-κB pathways in vascular endothelial cells[J]. Cellular Signaling,2018,43:85−94. doi: 10.1016/j.cellsig.2017.12.008





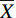

 下载:
下载:


 下载:
下载:
