Effect of Pectin Oligosaccharides from Hawthorn on the H2O2-induced Human Embryonic Lung Fibroblast Cells
-
摘要: 以过氧化氢(H2O2)诱导的人胚肺成纤维细胞(Human embryonic lung fibroblast cells,MRC-5)作为衰老模型,通过对细胞活力、存活率、β-半乳糖苷酶活性、线粒体膜电位、活性氧(ROS)含量、抗氧化能力和p53/p21/p16信号通路相关蛋白的表达水平等指标进行测定,研究山楂果胶寡糖(HPOS)对MRC-5衰老细胞的抗衰老作用。结果表明:与模型组相比,在浓度为0.8 mg/mL的山楂果胶寡糖干预下,MRC-5衰老细胞的细胞活力(约16.4%)、存活率(约17.0%)和线粒体膜电位(约284.3%)均显著增加(P<0.01);β-半乳糖苷酶阳性细胞比例(约66.9%)和ROS荧光强度(约77.2%)均显著降低(P<0.01);超氧化物歧化酶(SOD)和谷胱甘肽过氧化物酶(GSH-Px)活力较模型组细胞分别增加了72.0%和50.0%,而丙二醛(MDA)含量降低了42.6%(P<0.01)。浓度为0.8 mg/mL的山楂果胶寡糖干预显著抑制了p53/p21/p16信号通路中p53、p21和p16蛋白的表达(P<0.01)。总之,山楂果胶寡糖通过抑制由衰老诱发的细胞凋亡和氧化应激损伤,调节p53/p21/p16通路,从而改善H2O2诱导的MRC-5细胞衰老。本研究结果将为开发山楂果胶寡糖作为抗衰老的功能性食品配料提供科学依据。
-
关键词:
- 山楂果胶寡糖 /
- 衰老 /
- 细胞凋亡 /
- 抗氧化能力 /
- p53/p21/p16通路
Abstract: In this current study, the anti-aging effects and mechanism of action of pectin oligosaccharides from hawthorn (HPOS) on H2O2-induced human embryonic lung fibroblast cells were evaluated using the MRC-5 cell line. The effects on cell viability, survival rate, β-galactosidase activity, mitochondrial membrane potential, the content of reactive oxygen species (ROS), antioxidant capacity, and the expression levels of proteins associated with the p53/p21/p16 signaling pathway were evaluated. The findings illustrated that HPOS at a concentration of 0.8 mg/mL could significantly increased cell viability (approximately 16.4%), survival rate (approximately 17.0%), and mitochondrial membrane potential (approximately 284.3%), compared with that in the model group (P<0.01). Furthermore, the proportion of β-galactosidase-positive cells (approximately 66.9%) and fluorescence intensity of ROS (approximately 77.2%) significantly decreased (P<0.01). The superoxide dismutase (SOD) and glutathione peroxidase (GSH-Px) contents increased by 72.0% and 50.0%, respectively, compared to that in the model group, whereas the malondialdehyde (MDA) content decreased by 42.6% (P<0.01). HPOS at a concentration of 0.8 mg/mL significantly inhibited p53, p21, and p16 expression in the p53/p21/p16 pathway (P<0.01). Thus, HPOS ameliorates the H2O2-induced aging of MRC-5 cells by inhibiting apoptosis and oxidative stress damage along with regulating the p53/p21/p16 pathway, thereby providing a scientific basis for the development of HPOS as a functional food ingredient that acts against aging. -
随着生物体年龄的增长,细胞、组织、器官的形态和结构逐步地发生退行性改变,会损害组织功能和再生能力,从而导致与衰老相关的慢性代谢性疾病等患病风险的增加[1]。衰老的发病机制极其复杂,主要是与氧化应激和细胞凋亡有关[2]。然而,目前还没有有效的治疗方法来预防衰老。研究表明,合理的饮食和营养管理可以降低衰老及相关老年疾病的发病率[3]。因此,寻找能够缓解衰老的膳食补充剂已成为当前食品科学中亟待解决的问题。
山楂作为一种特有的药食同源的物种,已被广泛应用于功能性食品、中药等。山楂具有保护大脑神经、延年益寿等功效,被誉为“长寿果”[4−5]。《本草纲目》中用山楂、鹿茸等分研末,和蜂蜜为丸,治老年性疾病的记载是古代用药经验的总结;现代长期以生山楂泡水代茶使老人长寿的经验,开辟了山楂药用的新途径。目前,国内外对山楂的功能研究多集中于山楂多糖、黄酮、多酚和有机酸等成分的药理作用上,具有抗氧化、减肥、助消化和预防糖尿病、高血压、动脉粥样硬化等多种功效[6−9]。
研究表明,山楂中果胶的相对含量达6.4%,但其结构复杂且不稳定,进入机体后难以通过肠道吸收,而是被结肠的微生物降解而发挥作用[10]。此外,研究表明,山楂果胶寡糖比山楂果胶具有更好的功能作用[11−12]。寡糖,作为多糖的水解产物,具有改善免疫、调节血糖和抗氧化等功效,还具有热量低、稳定性高及安全无毒等理化特性,同时由于其相对分子质量较低,很容易被人体吸收利用[13]。研究表明,功能性寡糖有着良好的益生活性,可改变肠道菌群的组成和活力,有效调节机体肠道菌群的平衡,并通过肠-脑轴、肠-肝轴等多种作用机制调节机体健康[14−15]。衰老会引起机体损伤与氧化应激,加剧细胞老化或凋亡等,从而影响机体健康[16]。目前已经证明功能性寡糖具有延缓衰老的作用[17−19]。前期研究表明,新琼寡糖、部分水解香豆胶(聚合度在2~6之间的甘露寡糖占35.6%)和部分水解瓜尔豆胶(聚合度<7的寡糖占24.9%)可通过抑制大脑神经元损伤进而改善衰老引发的记忆障碍[20−22]。山楂果胶富含聚半乳糖醛酸,经聚半乳糖醛酸酶水解为果胶寡糖。研究表明,山楂果胶寡糖具有调控脂代谢,促进短链脂肪酸产生和改善肠道菌群结构等作用[23]。然而,目前尚未有山楂果胶寡糖改善衰老及相关慢性病的报道。因此,本研究主要探讨山楂果胶寡糖(HPOS)对H2O2诱导的MRC-5细胞的抗衰老作用及其机制,对开发山楂果胶寡糖功能产品、推动药食同源类植物寡糖的研究和医药领域的发展具有重要意义。
本研究利用超声波辅助果胶酶制备山楂果胶寡糖,建立过氧化氢(H2O2)诱导的人胚肺成纤维细胞(MRC-5)衰老模型,探究山楂果胶寡糖对MRC-5衰老细胞的抗衰老作用及其作用机理,旨在为进一步开发和利用山楂果胶寡糖提供科学依据。
1. 材料与方法
1.1 材料与仪器
山楂果 山东滨州健源有限公司;人胚肺成纤维细胞(MRC-5)、MRC-5细胞专用MEM培养基 中国武汉普诺赛生命科技有限公司提供;果胶酶3.2.1.15(比酶活为5 U/mg蛋白质) Sigma-Aldrich有限公司;胰酶细胞消化液 赛默飞世尔科技有限公司;超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)、丙二醛(MDA)检测试剂盒 南京建成生物科技公司;台盼蓝染色试剂盒、衰老β-半乳糖苷酶染色试剂盒、线粒体膜电位测定试剂盒、活性氧检测试剂盒、BCA蛋白检测试剂盒 碧云天生物技术有限公司(中国上海);β-肌动蛋白(β-actin,货号ab8226)、Bcl-2关联X蛋白(Bax,货号ab32503)、活化半胱胺酸蛋白酶蛋白-3(Cleaved Caspase-3,货号ab2302)、肿瘤抑制蛋白p53(货号ab26)、肿瘤抑制蛋白p21(货号ab188224)、肿瘤抑制蛋白p16(货号ab51243) 美国Abcam公司;IgG抗体 成都正能生物技术有限责任公司;Takara RNA 9767提取试剂盒、PrimeScriptTM RT Master Mix RR036A反转录试剂盒、TB Green Premix Ex Taq II试剂盒 日本Takara公司。
HF90/HF240二氧化碳培养箱 上海力申科学仪器有限公司;BXM-50VE立式压力蒸汽灭菌锅 上海博迅医疗生物仪器股份有限公司;TGL-16A型离心机 湖南湘仪实验室仪器开发有限公司;Spark多功能酶标仪 瑞士Tecan公司;Olympus CKX53倒置显微镜、FV3000激光共聚焦显微镜 奥林巴斯株式会社;QS5实时荧光定量PCR仪 美国ThermoFisher公司;ChemiScope 6200 Touch化学发光成像仪 上海勤翔科学仪器有限公司。
1.2 实验方法
1.2.1 山楂果胶寡糖的制备
参考Li等[24]的方法并略作修改。将山楂切片烘干,粉碎过20目筛。称山楂粉100 g,加入去离子水配成10%的溶液。用2 mol/L的柠檬酸溶液调节pH至2,90 ℃水浴加热120 min,同时500×g搅拌。浸提结束后5000×g离心10 min,保留上清液,冷却至室温。加入3倍体积乙醇缓慢搅拌,随后4 ℃过夜醇沉,5000×g离心10 min获得沉淀。用0.02 mol/L醋酸盐缓冲液调节料液pH至3.5,采用超声波(800 W,20 kHz)处理20 min,然后加入0.2 U/mL果胶酶于50 ℃水解2 h。利用DEAE-SephadexA-25葡聚糖凝胶层析色谱柱分离,色谱柱先用蒸馏水洗脱,再用0.3 mol/L NH4HCO3洗脱。分离液经蒸发浓缩后,真空冷冻干燥制备山楂果胶寡糖。测定其单糖组成和分子量,其成分为聚合度在2~5之间的低聚半乳糖醛酸(纯度≥90%);糖醛酸含量为99.8%,化学结构为α-(1,4)-D-半乳糖醛酸。
1.2.2 细胞分组及处理
参考Li等[25]的方法,将MRC-5细胞在专用MEM培养基中进行常规一分二传代培养(37 ℃;5% CO2饱和湿度)。细胞按2×104个/mL接种于96孔细胞培养板,分为:正常对照组、衰老模型组、阳性对照组(30 μmol/L白藜芦醇)、加样组(含浓度为0.2、0.8和2.0 mg/mL山楂果胶寡糖)。培养24 h后,换无血清培养基继续培养4 h。然后在衰老模型组、阳性对照组和加样组加入H2O2(200 μmol/L),置于二氧化碳培养箱中继续培养24 h后,观察细胞形态并进行各项指标测定。
1.2.3 细胞活力测定
按方法1.2.2培养和处理细胞,各组细胞检测前4 h换为无血清培养基后每孔加20 μL MTT溶液(5 mg/mL),37 ℃继续培养4 h后终止培养,吸除孔内上清液后,每孔加150 μL二甲基亚砜,室温下避光处理20 min,在490 nm处测定各孔的吸光度值。通过计算处理组与对照组的吸光度比值来表示细胞活力。
1.2.4 细胞存活率测定
按方法1.2.2培养和处理细胞,将细胞用0.4%台盼蓝染色10 min,再以4%多聚甲醛在4 ℃下固定30 min。利用倒置显微镜台盼蓝染色细胞形态,并随机计数300个相邻视野中蓝染的细胞,按下式计算细胞存活率。
细胞存活率(%)=(细胞总数−蓝色细胞数)/细胞总数×100。
1.2.5 β-半乳糖苷酶活性测定
细胞按2×105个/mL接种于24孔细胞培养板,随后按方法1.2.2培养和处理细胞,检测前移去原有的培养基,用PBS润洗后加入400 μL β-半乳糖苷酶固定液,室温固定15 min,吸除细胞固定液,用PBS洗涤细胞3次后加入250 μL β-半乳糖苷酶染色液。37 ℃孵育过夜,置于倒置显微镜下观察并拍照,阳性细胞显示为蓝色。采用Image J软件计算阳性细胞占总细胞比值来表示β-半乳糖苷酶活性。
1.2.6 线粒体膜电位测定
按方法1.2.2培养和处理细胞,随后用胰酶细胞消化液消化2.5 min,将其制成细胞悬液,0.5 mL装于离心管中。室温下400×g离心5 min除去上清,用0.5 mL的JC-1工作液重悬细胞。置于37 ℃细胞培养箱,孵育15 min。室温下400×g离心5 min,去除上清。用2 mL的PBS缓冲液重悬细胞,离心去除上清,重复一次。用0.5 mL的PBS重悬细胞,用免疫荧光染色分析。
1.2.7 抗氧化能力测定
细胞按8×105个/mL接种于6孔细胞培养板,随后按方法1.2.2培养和处理细胞。处理结束后去除细胞培养液,加入DCFH-DA(1:1000稀释),37 ℃孵育20 min。洗涤细胞3次后,利用激光共聚焦显微镜检测活性氧(ROS)的荧光强度(激发光488 nm,发射光波长525 nm)。细胞内SOD、GSH-Px和MDA含量的测定参照试剂盒说明。
1.2.8 p53/p21/p16信号通路相关蛋白和基因表达测定
取细胞在蛋白裂解缓冲液中裂解后均质,10000×g离心10 min收集上清液。采用BCA蛋白检测试剂盒定量测定细胞的蛋白浓度,随后将蛋白样品(20 μg)分离并转移到硝酸纤维素膜上。膜与一抗(β-actin、Bax、Cleaved Caspase-3、肿瘤抑制蛋白p53、肿瘤抑制蛋白p21和肿瘤抑制蛋白p16;1:1000稀释)在4 ℃下过夜。用洗涤缓冲液洗涤后,用二抗(1:5000稀释)孵育1 h。采用Image J软件,以β-actin作为内参,对内参蛋白、目的蛋白条带灰度进行定量,计算目的蛋白与内参蛋白的条带灰度值比值。
从细胞中提取总RNA后,使用反转录试剂盒对总RNA进行反转录反应。使用TB Green Premix Ex Taq II试剂盒,以cDNA作为模板,分析mRNA表达水平。qPCR程序如下:初始保持步骤,在95 ℃ 30 s;95 ℃ 5 s、60 ℃ 30 s,40个循环;72 ℃ 30 s。55~95 ℃逐步获得熔解曲线。以β-actin作为内参,采用(2-ΔΔCt)比较方法,分析靶基因的表达量。靶基因的引物见表1。
表 1 qPCR分析的引物序列Table 1. Primer sequences used for quantitative real-time polymerase chain reaction基因 正向引物(5’~3’) 反向引物(5’~3’) p16 CTACTCTCCTCCGCTGGGAA GGCCTAACTTAGCGCTGCTT p53 TGGCCATCTACAAGCAGTCACA GCAAATTTCCTTCCACTCGGAT β-actin GACTCCTATGTGGGTGACGA ACGGTTGGCCTTAGGGTTCA 1.3 数据处理
采用IBM SPSS 23.0软件,所有数据均表示为mean±SD。组间数据的显著性分析采用一维方差分析(One-Way ANOVA)中的Tukey’s多重比较进行。*P<0.05表示数据具有显著差异,**P<0.01表示数据具有极显著差异。
2. 结果与分析
2.1 山楂果胶寡糖对MRC-5细胞活力的影响
本实验利用山楂果胶寡糖先干预MRC-5细胞,后经H2O2诱导衰老。如图1A所示,不同浓度的山楂果胶寡糖干预组与对照组相比,各组细胞活力无显著性差异(P>0.05),表明山楂果胶寡糖不会对细胞产生毒性作用。如图1B所示,与对照组相比,H2O2在200 μmol/L浓度下MRC-5的细胞活力极显著降低(P<0.01)。因此,本文选用浓度为200 μmol/L的H2O2建立MRC-5衰老细胞模型。如图1C所示,相较于模型组,白藜芦醇和较高浓度的山楂果胶寡糖干预后MRC-5衰老细胞活力均显著增加,其中在0.8 mg/mL和2.0 mg/mL浓度的山楂果胶寡糖干预下细胞活力分别增加了16.4%(P<0.01)和13.4%(P<0.05)。结果表明,0.8 mg/mL和2.0 mg/mL浓度的山楂果胶寡糖干预显著提高了H2O2诱导的MRC-5细胞的活力。
![]() 图 1 山楂果胶寡糖对MRC-5细胞活力的影响。注:(A)毒性实验,(B)H2O2建模浓度,(C)细胞活力;与对照组比,*P<0.05,**P<0.01;与模型组比,#P<0.05,##P<0.01,图2~5同。Figure 1. Effects of pectin oligosaccharides from hawthorn on the cells viability of MRC-5 cells
图 1 山楂果胶寡糖对MRC-5细胞活力的影响。注:(A)毒性实验,(B)H2O2建模浓度,(C)细胞活力;与对照组比,*P<0.05,**P<0.01;与模型组比,#P<0.05,##P<0.01,图2~5同。Figure 1. Effects of pectin oligosaccharides from hawthorn on the cells viability of MRC-5 cells2.2 山楂果胶寡糖对MRC-5细胞凋亡的影响
死细胞可被台盼蓝染成蓝色,因此可利用台盼蓝染色法检测MRC-5细胞的存活率情况。如图2A所示,与对照组相比,H2O2处理后细胞死亡数量明显增加,而白藜芦醇和山楂果胶寡糖干预后MRC-5细胞死亡数量降低。如图2B所示,与模型组相比,0.2、0.8和2.0 mg/mL浓度的山楂果胶寡糖干预后MRC-5细胞存活率显著增加,增加量分别为6.6%(P<0.05)、17.0%(P<0.01)和10.4%(P<0.01)。进一步利用Western Bloting法检测了细胞凋亡相关蛋白Cleaved Caspase-3和Bax的表达。如图2C~2E所示,与模型组相比,山楂果胶寡糖干预抑制了Cleaved Caspase-3和Bax蛋白的表达水平,其中0.8 mg/mL浓度的山楂果胶寡糖干预后降低量分别为31.7%和35.0%(P<0.01)。结果表明,山楂果胶寡糖抑制了H2O2诱导的MRC-5细胞凋亡,其中在0.8 mg/mL浓度下最优。
2.3 山楂果胶寡糖对MRC-5细胞β-半乳糖苷酶活性和线粒体膜电位的影响
细胞在衰老状态下会产生高酶活性的β-半乳糖苷酶。以X-Gal为底物,在该酶的催化下会产生深蓝色产物。图3A所示,与对照组相比,H2O2处理后细胞的β-半乳糖苷酶活性显著增加。如图3B,与模型组相比,白藜芦醇和不同浓度的山楂果胶寡糖干预,细胞中β-半乳糖苷酶活性均降低。其中,山楂果胶寡糖在0.8 mg/mL和2.0 mg/mL浓度处理后β-半乳糖苷酶阳性细胞比例分别极显著降低了66.9%和47.8%(P<0.01)。结果表明,0.8 mg/mL和2.0 mg/mL浓度的山楂果胶寡糖降低了H2O2诱导的MRC-5细胞中的β-半乳糖苷酶活性。
线粒体功能障碍通常表现为线粒体膜电位损伤等,是细胞衰老的重要生物标志。细胞在衰老过程中,线粒体基因突变积累,线粒体膜电位降低[26]。利用JC-1染色检测线粒体膜电位的变化,结果如图3C~3D所示,与对照组相比,H2O2诱导MRC-5细胞的红色荧光减弱,绿色荧光增强,红绿荧光比值极显著降低(P<0.01),表明线粒体膜电位降低。与模型组相比,0.8 mg/mL和2.0 mg/mL浓度的山楂果胶寡糖处理后,红绿荧光比值分别增加了284.3%(P<0.01)和220.4%(P<0.05)。结果表明,0.8 mg/mL和2.0 mg/mL浓度的山楂果胶寡糖可通过显著增加H2O2诱导的MRC-5细胞中的线粒体膜电位抑制其衰老。
2.4 山楂果胶寡糖对MRC-5细胞抗氧化能力的影响
荧光探针DCFH-DA可用于检测活性氧,荧光强度代表细胞内的活性氧水平。图4A所示,与对照组相比,H2O2诱导细胞的ROS荧光强度明显增加。如图4B,相较于模型组,在0.8 mg/mL和2.0 mg/mL浓度的山楂果胶寡糖干预后ROS荧光强度分别极显著降低了77.2%和71.8%(P<0.01)。为了研究山楂果胶寡糖是否介导抗氧化酶活性保护H2O2诱导的细胞凋亡,进一步测定了SOD、GSH-Px活性和MDA含量(图4C~4E)。MRC-5细胞被H2O2处理后,细胞内SOD和GSH-Px活性较对照组极显著降低(P<0.01),而MDA含量极显著增加(P<0.01)。在浓度为0.8 mg/mL的山楂果胶寡糖干预下,细胞内SOD和GSH-Px活性分别比模型组极显著提高了72.0%和50.0%,而MDA含量显著降低了42.6%(P<0.01)。结果表明,干预浓度为0.8 mg/mL和2.0 mg/mL的山楂果胶寡糖显著提高了H2O2诱导的MRC-5细胞的抗氧化能力。
2.5 山楂果胶寡糖对MRC-5细胞p53/p21/p16信号通路相关蛋白和基因表达的影响
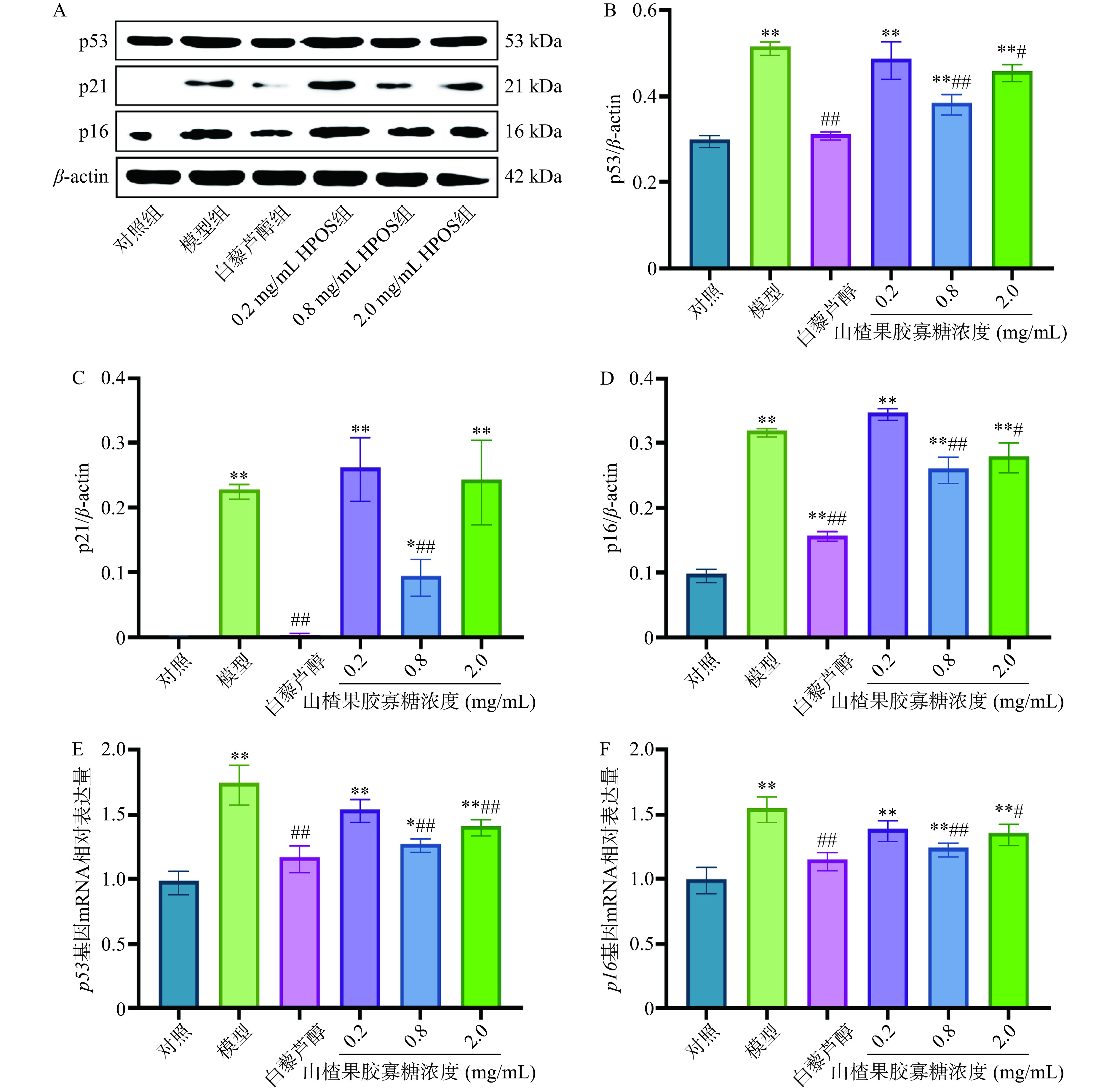
为了进一步明确山楂果胶寡糖抑制MRC-5细胞衰老的潜在机制,探讨了山楂果胶寡糖对p53/p21/p16信号通路中的相关蛋白和基因的表达情况的影响。如图5A~5D所示,与对照组相比,模型组细胞中p53、p21和p16蛋白的表达极显著增加(P<0.01)。相较于模型组,在浓度为0.8 mg/mL的山楂果胶寡糖干预下极显著下调MRC-5衰老细胞中p53、p21和p16蛋白的表达,降低量分别为25.3%、58.6%和18.2%(P<0.01)。如图5E~5F所示,相对于衰老细胞中p53和p16基因mRNA表达量,白藜芦醇和山楂果胶寡糖干预抑制其表达。其中,在0.8 mg/mL浓度的山楂果胶寡糖干预下,MRC-5衰老细胞中p53和p16基因mRNA的相对表达量分别极显著降低了27.1%和19.6%(P<0.01)。结果表明,浓度为0.8 mg/mL的山楂果胶寡糖显著抑制了H2O2诱导的MRC-5细胞中p53/p21/p16信号通路。
3. 讨论
细胞在衰老过程中会逐渐表现出细胞活力下降和细胞凋亡现象增加[27]。凋亡调控蛋白在组织细胞中表达比例的改变,可控制细胞凋亡的过程[28]。本研究发现,山楂果胶寡糖干预增加了MRC-5衰老细胞的活力,抑制其Cleaved Caspase-3和Bax凋亡蛋白的表达(图1和图2)。研究发现,促凋亡蛋白Bax是启动细胞凋亡通路的关键[29]。这表明山楂果胶寡糖可通过抑制凋亡蛋白的表达对细胞凋亡发挥积极的干预作用。随着细胞的衰老,β-半乳糖苷酶的活力会逐步累积,其阳性率反映细胞的衰老程度[30]。本研究发现山楂果胶寡糖干预降低了MRC-5衰老细胞中β-半乳糖苷酶的活性(图3A~3B),表明了山楂果胶寡糖延缓了细胞的衰老进程。线粒体是衰老过程中的关键参与者,在氧化应激和细胞凋亡的调节中发挥着关键作用[31]。线粒体膜电位的降低是细胞凋亡的标志性事件,本研究发现山楂果胶寡糖干预引起H2O2诱导的MRC-5衰老细胞线粒体膜电位增加(图3C~3D)。因此表明,山楂果胶寡糖对H2O2诱导MRC-5细胞线粒体功能紊乱具有改善作用,可通过增加线粒体膜电位来调节细胞凋亡。
过量ROS累积会导致氧化应激,而氧化应激是导致细胞衰老的重要原因[32−33]。本研究发现经山楂果胶寡糖干预后MRC-5衰老细胞中ROS含量降低(图4A~4B)。研究发现,魔芋甘露寡糖能够通过维持机体内ROS的动态平衡来提高其抗氧化能力[34]。在衰老状态下,机体内氧化与抗氧化易失衡,导致中性粒细胞炎症性浸润,进而产生大量的关键氧化产物,从而导致细胞损伤[35]。细胞内防御抗氧化酶如SOD和GSH-Px,可通过抑制细胞过多ROS产生从而延缓衰老的进程[36]。MDA是由ROS和细胞膜中的脂质之间的反应产生,其含量可以反映细胞脂质过氧化的程度[37]。本研究发现,在浓度为0.8 mg/mL山楂果胶寡糖的干预下MRC-5衰老细胞中MDA含量显著降低,而SOD和GSH-Px活性极显著增加(P<0.01,图4C~4E)。综上结果表明,山楂果胶寡糖可改善细胞凋亡和提高抗氧化能力,从而抑制H2O2诱导的MRC-5细胞衰老。
氧化损伤的产生会激活p53/p21/p16信号通路,导致细胞周期阻滞和衰老[38]。为进一步明确山楂果胶寡糖抑制衰老的潜在机制,继续探讨了山楂果胶寡糖对p53/p21/p16信号通路中相关蛋白和基因表达的影响。研究表明,p53、p21和p16蛋白的过表达可导致细胞衰老[39]。本研究发现,浓度为0.8 mg/mL山楂果胶寡糖干预显著抑制了衰老诱发的p53/p21/p16信号通路中p53、p21和p16蛋白和基因的过度表达(图5)。因此,山楂果胶寡糖可能是通过提高抗氧化能力减少氧化损伤,进而抑制了p53/p21/p16信号通路,从而延缓H2O2诱导的MRC-5细胞衰老。
4. 结论
本研究从细胞活力、存活率、β-半乳糖苷酶活性、线粒体膜电位、抗氧化能力以及衰老相关通路蛋白和基因表达水平等方面对山楂果胶寡糖调节细胞衰老的潜在机制进行了探究。结果表明山楂果胶寡糖改善了H2O2诱导的MRC-5细胞衰老程度,特别是在其浓度0.8 mg/mL干预下,这可能与其能够抑制促凋亡蛋白的表达和增加线粒体膜电位来改善细胞凋亡,增强抗氧化能力,抑制p53/p21/p16衰老信号通路有关。山楂果胶寡糖有望作为膳食补充剂的配料,发挥抗衰老的功能活性。
-
图 1 山楂果胶寡糖对MRC-5细胞活力的影响。
注:(A)毒性实验,(B)H2O2建模浓度,(C)细胞活力;与对照组比,*P<0.05,**P<0.01;与模型组比,#P<0.05,##P<0.01,图2~5同。
Figure 1. Effects of pectin oligosaccharides from hawthorn on the cells viability of MRC-5 cells
表 1 qPCR分析的引物序列
Table 1 Primer sequences used for quantitative real-time polymerase chain reaction
基因 正向引物(5’~3’) 反向引物(5’~3’) p16 CTACTCTCCTCCGCTGGGAA GGCCTAACTTAGCGCTGCTT p53 TGGCCATCTACAAGCAGTCACA GCAAATTTCCTTCCACTCGGAT β-actin GACTCCTATGTGGGTGACGA ACGGTTGGCCTTAGGGTTCA -
[1] LÓPEZ-OTÍN C, BLASCO M A, PARTRIDGE L, et al. Hallmarks of aging:An expanding universe[J]. Cell,2023,186(2):243−278. doi: 10.1016/j.cell.2022.11.001
[2] HOSSEINI L, FAROKHI-SISAKHT F, BADALZADEH R, et al. Nicotinamide mononucleotide and melatonin alleviate aging-induced cognitive impairment via modulation of mitochondrial function and apoptosis in the prefrontal cortex and hippocampus[J]. Neuroscience,2019,423:29−37. doi: 10.1016/j.neuroscience.2019.09.037
[3] ZHANG J, CHEN Z W, YU H X, et al. Anti-aging effects of a functional food via the action of gut microbiota and metabolites in aging mice[J]. Aging-US,2021,13(13):17880−17900. doi: 10.18632/aging.202873
[4] LI R Y, LUAN F, ZHAO Y Y, et al. Crataegus pinnatifida:A botanical, ethnopharmacological, phytochemical, and pharmacological overview[J]. Journal of Ethnopharmacology,2023,301:115819. doi: 10.1016/j.jep.2022.115819
[5] WANG X X, LI X, LI L Y, et al. Hawthorn fruit extract ameliorates H2O2-induced oxidative damage in neuronal PC12 cells and prolongs the lifespan of Caenorhabditis elegans via the IIS signaling pathway[J]. Food and Function,2022,13(20):10680−10694. doi: 10.1039/D2FO01657E
[6] ZHANG S Y, SUN X L, YANG X L, et al. Botany, traditional uses, phytochemistry and pharmacological activity of Crataegus pinnatifida (Chinese hawthorn):A review[J]. Journal of Pharmacy and Pharmacology,2022,74(11):1507−1545. doi: 10.1093/jpp/rgac050
[7] GUO Q B, DU J H, JIANG Y, et al. Pectic polysaccharides from hawthorn:Physicochemical and partial structural characterization[J]. Food Hydrocolloids,2019,90:146−153. doi: 10.1016/j.foodhyd.2018.10.011
[8] MIAO J, LI X, FAN Y, et al. Effect of different solvents on the chemical composition, antioxidant activity and alpha-glucosidase inhibitory activity of hawthorn extracts[J]. International Journal of Food Science and Technology,2016,51(5):1244−1251. doi: 10.1111/ijfs.13076
[9] LU M, ZHANG L, PAN J, et al. Advances in the study of the vascular protective effects and molecular mechanisms of hawthorn (Crataegus anamesa Sarg.) extracts in cardiovascular diseases[J]. Food and Function,2023,14(13):5870−5890. doi: 10.1039/D3FO01688A
[10] ZHANG X, HAN Y, HUANG W, et al. The influence of the gut microbiota on the bioavailability of oral drugs[J]. Acta Pharmaceutica Sinica B,2021,11(7):1789−1812. doi: 10.1016/j.apsb.2020.09.013
[11] LI T P, LI S H, DU L J, et al. Effects of haw pectic oligosaccharide on lipid metabolism and oxidative stress in experimental hyperlipidemia mice induced by high-fat diet[J]. Food Chemistry,2010,121:1010−1013. doi: 10.1016/j.foodchem.2010.01.039
[12] ZHU R G, SUN Y D, LI T P, et al. Comparative effects of hawthorn (Crataegus pinnatifida Bunge) pectin and pectin hydrolyzates on the cholesterol homeostasis of hamsters fed high-cholesterol diets[J]. Chemico-Biological Interactions,2015,238:42−47. doi: 10.1016/j.cbi.2015.06.006
[13] YANG S Q, WU C X, YAN Q J, et al. Nondigestible functional oligosaccharides:Enzymatic production and food applications for intestinal health[J]. Annual Review of Food Science and Technology,2023,14:297−322. doi: 10.1146/annurev-food-052720-114503
[14] NERI-NUMA I A, PASTORE G M. Novel insights into prebiotic properties on human health:A review[J]. Food Research International,2020,131:108973. doi: 10.1016/j.foodres.2019.108973
[15] ZHU D, YAN Q J, LIU J, et al. Can functional oligosaccharides reduce the risk of diabetes mellitus?[J]. FASEB Journal,2019,33(11):11655−11667. doi: 10.1096/fj.201802802RRR
[16] XU Q X, FU Q, LI Z, et al. The flavonoid procyanidin C1 has senotherapeutic activity and increases lifespan in mice[J]. Nature Metabolism,2021,3(12):1706−1726. doi: 10.1038/s42255-021-00491-8
[17] LIU X Y, LIU D, LIN G P, et al. Anti-ageing and antioxidant effects of sulfate oligosaccharides from green algae Ulva lactuca and Enteromorpha prolifera in SAMP8 mice[J]. International Journal of Biological Macromolecules,2019,139:342−351. doi: 10.1016/j.ijbiomac.2019.07.195
[18] TUSI S K, KHALAJ L, ASHABI G, et al. Alginate oligosaccharide protects against endoplasmic reticulum- and mitochondrial-mediated apoptotic cell death and oxidative stress[J]. Biomaterials,2011,32(23):5438−5458. doi: 10.1016/j.biomaterials.2011.04.024
[19] 牟婕, 冯文静, 毛拥军. 甘露糖醛酸寡糖对过氧化氢诱导的衰老心肌细胞的影响[J]. 青岛大学学报(医学版),2019,55(4):411−414,418. [MOU J, FENG W J, MAO Y J. Effect of mannuronic acid oligosaccharides on hydrogen peroxide-induced cardiomyocyte senescence[J]. Journal of Qingdao University (Medical Sciences),2019,55(4):411−414,418.] MOU J, FENG W J, MAO Y J. Effect of mannuronic acid oligosaccharides on hydrogen peroxide-induced cardiomyocyte senescence[J]. Journal of Qingdao University (Medical Sciences), 2019, 55(4): 411−414,418.
[20] LI T, YANG S Q, LIU X Y, et al. Dietary neoagarotetraose extends lifespan and impedes brain aging in mice via regulation of microbiota-gut-brain axis[J]. Journal of Advanced Research,2023,52:119−134. doi: 10.1016/j.jare.2023.04.014
[21] 李涛, 刘晓艳, 王楠楠, 等. β-甘露聚糖酶部分水解香豆胶对自然衰老小鼠的抗衰老作用[J]. 食品科学,2022,43(9):111−119. [LI T, LIU X Y, WANG N N, et al. Anti-aging effect of partially hydrolyzed fenugreek gum by β-mannanase on naturally aging mice[J]. Food Science,2022,43(9):111−119.] LI T, LIU X Y, WANG N N, et al. Anti-aging effect of partially hydrolyzed fenugreek gum by β-mannanase on naturally aging mice[J]. Food Science, 2022, 43(9): 111−119.
[22] 李涛, 许云聪, 陈峻波, 等. 部分水解瓜尔豆胶对阿尔茨海默病小鼠学习记忆能力的改善作用[J]. 食品科学技术学报,2023,41(5):34−44. [LI T, XU Y C, CHEN J B, et al. Effect of partially hydrolyzed guar gum on learning and memory ability of Alzheimer's disease mice[J]. Journal of Food Science and Technology,2023,41(5):34−44.] doi: 10.12301/spxb202300039 LI T, XU Y C, CHEN J B, et al. Effect of partially hydrolyzed guar gum on learning and memory ability of Alzheimer's disease mice[J]. Journal of Food Science and Technology, 2023, 41(5): 34−44. doi: 10.12301/spxb202300039
[23] LI Q, WANG M, ZHANG Y, et al. Pectin-derived oligogalacturonic acids ameliorate high-fat diet-induced obesity in mice by regulating gut microbiota and inflammation[J]. Journal of Functional Foods,2024,112:105928. doi: 10.1016/j.jff.2023.105928
[24] LI S H, LI T P, JIA Y F, et al. Fractionation and structural characterization of haw pectin oligosaccharides[J]. European Food Research and Technology,2011,233:731−734. doi: 10.1007/s00217-011-1568-8
[25] LI T, LI Y X, YAN Q J, et al. Co-treatment of nicotinamide mononucleotide and neoagarooligosaccharide mitigates aging-induced cognitive impairment by promoting mitochondrial dynamics[J]. Journal of Functional Foods,2024,112:105922. doi: 10.1016/j.jff.2023.105922
[26] CHEN P X, ZHANG L Y, CHEN Y, et al. Mitochondrial stress and aging:Lessons from C. elegans[J]. Seminars in Cell & Developmental Biology,2024,154:69−76.
[27] OGRODNIK M. Cellular aging beyond cellular senescence:Markers of senescence prior to cell cycle arrest in vitro and in vivo[J]. Aging Cell,2021,20(4):e13338. doi: 10.1111/acel.13338
[28] LI L, ZHANG H, CHEN B B, et al. BaZiBuShen alleviates cognitive deficits and regulates Sirt6/NRF2/HO-1 and Sirt6/P53-PGC-1 alpha-TERT signaling pathways in aging mice[J]. Journal of Ethnopharmacology,2022,282:114653. doi: 10.1016/j.jep.2021.114653
[29] WANG C C, WANG D, XU J, et al. DHA enriched phospholipids with different polar groups (PC and PS) had different improvements on MPTP-induced mice with Parkinson’s disease[J]. Journal of Functional Foods,2018,45:417−426. doi: 10.1016/j.jff.2018.04.017
[30] DIMRI G P, LEE X, BASILE G, et al. A biomarker that identifies senescent human cells in culture and in aging skin in vivo[J]. PNAS,1995,92(20):9363−9367. doi: 10.1073/pnas.92.20.9363
[31] GREEN D R, REED J C. Mitochondria and apoptosis[J]. Science,1998,281:1309−1312. doi: 10.1126/science.281.5381.1309
[32] KUMAR P, LIU C, SULIBURK J, et al. Supplementing glycine and n-acetylcysteine (GlyNAC) in older adults improves glutathione deficiency, oxidative stress, mitochondrial dysfunction, inflammation, physical function, and aging hallmarks:A randomized clinical trial[J]. Journals of Gerontology Series a-Biological Sciences and Medical Sciences,2023,78(1):75−89. doi: 10.1093/gerona/glac135
[33] BHATT M P, LIM Y C, KIM Y M, et al. C-peptide activates AMPKα and prevents ROS-mediated mitochondrial fission and endothelial apoptosis in diabetes[J]. Diabetes,2013,62:3851−3862. doi: 10.2337/db13-0039
[34] LU J T, QI C L, LIMBU S M, et al. Dietary mannan oligosaccharide (MOS) improves growth performance, antioxidant capacity, non-specific immunity and intestinal histology of juvenile Chinese mitten crabs (Eriocheir sinensis)[J]. Aquaculture,2019,510(15):337−346.
[35] DENG X J, LIANG X H, YANG H Y, et al. Nicotinamide mononucleotide (NMN) protects bEnd. 3 cells against H2O2-induced damage via NAMPT and the NF-κB p65 signalling pathway[J]. FEBS Open Bio,2021,11:866−879. doi: 10.1002/2211-5463.13067
[36] MORRONE M D, DE ASSIS A M, DA ROCHA R F, et al. Passiflora manicata (Juss.) aqueous leaf extract protects against reactive oxygen species and protein glycation in vitro and exvivo models[J]. Food and Chemical Toxicology,2013,60:45−51. doi: 10.1016/j.fct.2013.07.028
[37] SHADAB M, AGRAWAL D K, ASLAM M, et al. Occupational health hazards among sewage workers:Oxidative stress and deranged lung functions[J]. Journal of Clinical and Diagnostic Research,2014,8(4):BC11−BC12.
[38] YANG F, YI M Q, LIU Y, et al. Glutaredoxin-1 silencing induces cell senescence via p53/p21/p16 signaling axis[J]. Journal of Proteome Research,2018,17(3):1091−1100. doi: 10.1021/acs.jproteome.7b00761
[39] BAO Y Z, HE X Y, WU W L, et al. Sulfated galactofucan from Sargassum thunbergii induces senescence in human lung cancer A549 cells[J]. Food and Function,2020,11(5):4785−4792. doi: 10.1039/D0FO00699H





 下载:
下载:




 下载:
下载:
