Optimization of Extraction of Pectin from Jackfruit Peel by Ultrasonic-assisted Enzymatic Method and Modification of De-Esterification
-
摘要: 为提高菠萝蜜果皮果胶(Jackfruit peel pectin,JFPP)的得率,并得到高纯度具有良好的功能特性的果胶,本研究通过响应面试验优化超声辅助纤维素酶法对果胶的提取工艺,对提取的果胶进行初步纯化,包括脱脂、脱蛋白、脱色和透析浓缩,并对纯化后果胶进行酶法低酯化(De-esterification)改性,得到低酯菠萝蜜果皮果胶(DE-JFPP),对比分析改性前后果胶的基本成分组成、分子量、单糖组成、官能团特征、热稳定性和微观结构。结果表明,最优提取工艺参数为加酶量0.7%,酶解温度30.4 ℃,pH4.6,此条件下JFPP得率为15.26%±0.07%。改性后的果胶的半乳糖醛酸含量由79.10%增加到83.24%,总糖含量由43.42%降低为41.90%,酯化度由84.25%降低为32.36%,重均分子量由29.24 ku降低为28.49 ku。JFPP和DE-JFPP均有11种单糖,均属于RG-I型果胶,DE-JFPP支链化程度减小。傅里叶变换红外光谱显示改性前后的果胶均具有果胶特征吸收峰,改性后的果胶分子对应酯化羧基的吸收峰峰面积下降。JFPP和DE-JFPP的溶解温度分别为160.22 ℃和123.28 ℃,降解温度分别为255.11 ℃和230.56 ℃,均具有较高的热稳定性。扫描电镜图显示,JFPP表面光滑,结构紧凑,DE-JFPP表面粗糙,结构疏松。本研究优化了JFPP提取工艺,提高其得率,并证明低酯化后的果胶具有较好的理化性质及微观结构,可满足不同领域中对凝胶负载体系需求,进一步拓展菠萝蜜果皮果胶的利用空间。Abstract: In order to improve the yield of jackfruit peel pectin (JFPP) and obtain high-purity pectin with good functional properties, this study optimized the extraction process of pectin by ultrasound-assisted cellulase enzyme method through response surface experiments. The extracted pectin was preliminarily purified, including degreasing, deproteinization, decolorization, and dialysis concentration process. The purified pectin was then enzymatically esterified and modified by de-esterification to obtain de-esterified jackfruit peel pectin (DE-JFPP), and a comparative analysis was conducted on the basic composition, molecular weight, monosaccharide composition, functional group characteristics, thermal stability, and microstructure of the pectin before and after modification. The results showed that the optimal conditions for the extraction process were enzyme dosage of 0.7%, the enzymatic hydrolysis temperature of 30.4 ℃, and the pH of 4.6. It was observed that the yield of JFPP was 15.26%±0.07% under the specified conditions. The galacturonic acid content in the modified pectin increased from 79.10% to 83.24%, with a decrease in total sugar content from 43.42% to 41.90%, a decrease in esterification degree from 84.25% to 32.36%, and a decrease in weight-average molecular weight from 29.24 ku to 28.49 ku. Both JFPP and DE-JFPP contained eleven monosaccharides and belonged to the RG-I pectin with a decrease in the degree of branching in DE-JFPP. Fourier transform infrared (FTIR) spectroscopy demonstrated that both the pectin before and after modification had characteristic absorption peaks of pectin, and the peak area corresponding to the esterified carboxyl acid group decreased after modification. The JFPP and DE-JFPP demonstrated high thermal stability, with solubilization temperatures of 160.22 ℃ and 123.28 ℃, and degradation temperatures of 255.11 ℃ and 230.56 ℃, respectively. Scanning electron micrographs (SEM) showed that JFPP had a smooth surface and a compact structure, and DE-JFPP had a rough surface and a loose structure. This study optimized the extraction process of jackfruit peel pectin, improving its yield. Results demonstrated that the esterified pectin had favorable physicochemical properties and microstructure, meeting requirements for gel carrier systems in various fields and expanding the utilization space of jackfruit peel pectin.
-
菠萝蜜(Artocarpus heterophyllus Lam.)在我国的主要种植区是海南、云南、广东和广西等省份,它的果皮占比达果实质量的60%左右[1],常被视为加工废弃物,但菠萝蜜果皮中具有多种可利用的天然活性成分,例如黄酮类物质、多酚类物质、多糖类物质等,其中,属于多糖类物质的果胶含量十分丰富[2]。如今,国内外的学者进行了一些关于废弃菠萝蜜果皮中的果胶提取工艺的研究,台建祥等[3]采用正交试验优化酶法提取工艺,果胶得率为13.69%,半乳糖醛酸含量高达87.6%,所得果胶纯度高;Begum等[4]将果胶从菠萝蜜废料中分别用草酸铵和酸提取出来,初步纯化后得到纯度63.33%和62.71%的果胶。因此,以菠萝蜜果皮作为原料提取果胶具有较大的开发应用价值。
果胶是一种弱酸性的天然植物多糖,除了对高脂血症、高血压等病症有一定的预防作用外,还可作为凝胶剂在食品行业中广泛应用[5]。通常根据酯化度(Degree of esterification,DE)将果胶分为低酯果胶(DE<50%)和高酯果胶(DE>50%)两类,其中,高酯果胶在低酸性和可溶性固形物浓度大于55%的条件下可形成凝胶[6],此凝胶条件也使得高酯果胶在食品应用上受到限制;而低酯果胶分子链间的羧基更容易与Ca2+或其他二价金属离子反应从而形成凝胶[7],这种钙凝胶机理更符合低热量食品的应用趋势。因此,为了扩大果胶的应用范围,许多学者对果胶进行了改性研究,其中低酯化是一种重要的果胶基团取代改性方法,通常使用碱法、酶法、酰胺化法和酸法等,酶法与其他方法相比具有反应底物专一性,产物分子量高的特点[8]。目前,对于果胶的改性研究,多集中于柑橘果胶、苹果果胶等,尚未有酶法低酯化改性应用于菠萝蜜果皮低酯果胶制备的报道。
本研究采用超声辅助酶法提取菠萝蜜果皮果胶(Jackfruit Peel Pectin,JFPP),对提取工艺条件进行优化来提高果胶得率,再对其进行初步纯化,获得高纯度JFPP。采用果胶甲基酯酶对JFPP进行低酯化改性,并对改性前后JFPP的理化性质及结构表征进行综合分析,以期为开发具有良好生物学活性的菠萝蜜果皮果胶产品提供理论依据,进一步提高菠萝蜜加工副产物的加工价值。
1. 材料与方法
1.1 材料与仪器
菠萝蜜果皮 广西百色市田阳区鲜果拍档提供;氢氧化钠 色谱纯,美国Sigma公司;三氟乙酸 色谱纯,上海安谱实验科技股份有限公司;牛血清白蛋白、葡萄糖标准品 北京索莱宝科技有限公司;纤维素酶(10000 U/g) 上海麦克林生化科技股份有限公司;果胶甲基酯酶(10000 PE/g) Novozymes公司;其它实验试剂均为国产分析纯。
TLE204E/02电子天平(0.1 mg) 梅特勒-托利多仪器(上海)有限公司;DSC2500差示扫描量热仪 美国TA公司;EMS-30磁力搅拌恒温水浴器 常州爱华仪器制造有限公司;ICS 5000+离子色谱分析仪 美国Thermo公司;QL-720B水分测定仪 厦门米德电子科技有限公司;F16502扫描电镜 荷兰PHENOM公司;高效液相色谱仪(配有2414折光示差检测器) 美国Waters公司;Frontier傅立叶红外光谱仪 美国PE公司。
1.2 实验方法
1.2.1 菠萝蜜果皮果胶的提取
1.2.1.1 菠萝蜜果皮的预处理
菠萝蜜果皮用自来水洗净,切成小块,放入热风烤箱60 ℃烘干24 h。将烘干的菠萝蜜果皮磨碎,用60目的筛网筛成细粉,样品置于干燥器中备用。
1.2.1.2 菠萝蜜果皮粗果胶的提取工艺
取5 g菠萝蜜果皮粉末,提取液为邻苯二甲酸氢钾,利用NaOH/HCl调节pH,按料液比1:50 (g/mL)加提取液,加入纤维素酶酶解7 h,酶解结束后作灭酶处理,接着将样品于240 W超声波下继续提取40 min,超声结束后10000 r/min离心15 min取上清液,旋蒸至一定体积后加3倍体积无水乙醇(体积分数99.5%),在4 ℃下醇沉24 h,醇沉结束后分离出沉淀,待乙醇挥发干净后,50 ℃烘干,粉碎后得菠萝蜜果皮粗果胶。
1.2.2 菠萝蜜果皮果胶提取单因素实验
固定制备条件为加酶量0.6%(加酶量为酶与底物的质量比)、提取液pH为5、酶解温度45 ℃,分别调节以上三个因素,进行单因素实验。其中,调节加酶量分别为0.4%、0.5%、0.6%、0.7%、0.8%,调节酶解温度分别为25、30、35、40、45 ℃,调节pH分别为3.5、4、4.5、5、5.5,当其中一个因素为变量时,其他条件固定不变,各种因素的最优值以果胶得率为指标来确定。
1.2.3 响应面试验优化菠萝蜜果皮果胶提取工艺
基于单因素实验,以加酶量(A)、酶解温度(B)、pH(C)为自变量,果胶得率为响应值,采用Box-Behnken设计,通过响应面试验优化提取工艺,表1为因素水平设计。
表 1 响应面因素水平设计Table 1. Response surface factor level design水平 因素 A加酶量(%) B酶解温度(℃) C pH −1 0.6 25 4 0 0.7 30 4.5 1 0.8 35 5 1.2.4 果胶得率的计算
果胶得率按式(1)计算。
(1) 式中:W表示果胶得率,%;m表示提取的粗果胶质量,g;M表示菠萝蜜果皮粉质量,g。
1.2.5 菠萝蜜果皮果胶的初步纯化
1.2.5.1 脱脂
取适量的粗果胶参照GB 5009.6-2016索氏抽提法进行脱脂。
1.2.5.2 脱蛋白
参考吴彤等[9]的方法略作修改,取适量粗果胶溶于去离子水中,配制三氯甲烷与正丁醇4:1的混合溶剂,将1/4的混合溶剂倒入300 mL样品溶液中,混合振荡摇匀、静置5 min后离心除去变性蛋白,如此反复操作,直到溶剂与水层之间不再存在变性蛋白。
1.2.5.3 脱色
加入脱蛋白果胶溶液体积的1/3的D101大孔树脂进行脱色,置于45 ℃摇床中以100 r/min转速脱色3 h,充分吸附色素,脱色结束通过抽滤分离果胶溶液与大孔树脂。
1.2.5.4 透析
将透析袋MD55(8000~14000 Da)浸泡在蒸馏水中,进行15 min的煮沸预处理,在透析袋中放入已脱蛋白的果胶溶液,用夹子夹住避免渗漏,用蒸馏水进行透析,6 h更换一次水,透析48 h。将透析后的样品溶液旋转蒸发至一定体积,加3倍体积无水乙醇,在4 ℃下醇沉24 h,醇沉结束后分离出沉淀,待乙醇挥发干净后,50 ℃烘干,粉碎后得菠萝蜜果皮果胶纯品,命名为JFPP。
1.2.6 菠萝蜜果皮果胶的低酯化
参照Lee等[10]的方法使用果胶甲基酯酶进行JFPP的低酯化(deesterification),低酯化后的果胶为DE-JFPP。将JFPP(2.5 g)与250 mL去离子水混合,搅拌至果胶完全溶解,用1 mol/L NaOH/HCl调节至4.5。然后在45 ℃水浴中孵育,加入1.5 mL果胶甲基酯酶对JFPP进行低酯化。低酯化3 h后,将样品溶液煮沸10 min使酶失活,冷却至室温。加入3倍体积无水乙醇,在室温下静置过夜,将沉淀出的果胶在50 ℃下干燥过夜,粉碎后得DE-JFPP。
1.2.7 菠萝蜜果皮果胶的理化特性
1.2.7.1 基本成分测定
水分含量用水分测定仪进行测定;脂肪含量的测定方法同1.2.5.1;按照GB 5009.4-2016中的直接灰化法进行灰分的测定。
蛋白质含量参照吕冰冰等[11]的方法。将牛血清白蛋白(BSA)制备成一组不同质量浓度的溶液,每一梯度为1 mL,各加入5 mL考马斯亮蓝溶液,摇匀后静置10 min,在595 nm波长下测定吸光度,并做空白试验,得出标准曲线的线性关系式:y=3.7157x+0.456,R²=0.9977。配制0.4 mg/mL的果胶溶液,按上述操作测定吸光度并计算蛋白质含量。
1.2.7.2 半乳糖醛酸含量的测定
参照NY/T 2016-2011分光光度法测定半乳糖醛酸含量,配制一组不同质量浓度的半乳糖醛酸溶液,每一梯度各取1.0 mL于试管中,分别加入0.25 mL的1 g/L咔唑乙醇溶液和5.0 mL硫酸,晃动均匀后在85 ℃水浴中加热20 min,待其冷却后,在避光处显色1 h,于波长525 nm处测定紫外吸光度,得到关于半乳糖醛酸的标准曲线,其回归方程为:y=0.0046x+0.058,R2=0.9924。配制一定质量浓度的样品溶液,按同样操作测定吸光度并计算半乳糖醛酸含量。
1.2.7.3 总糖含量测定
参照孟凡磊等[12]的苯酚-硫酸法测定总糖含量,称取适量D-葡萄糖标准品,配制一组不同质量浓度的梯度溶液,每一梯度各取1.0 mL放入试管中,再加入1.0 mL质量分数5%的苯酚溶液和5 mL硫酸,摇匀之后,在室温下静置30 min,在490 nm波长处测定紫外吸光度,得到了标准曲线的线性关系式:y=5.8273x+0.072,R²=0.9975。配制0.4 mg/mL的果胶溶液,按上述操作测定吸光度并计算总糖含量。
1.2.7.4 酯化度测定
酯化度的测度参照让凤菊等[13]的方法稍作修改,首先以酚酞为指示剂,用标定后的0.1 mol/L NaOH标准溶液滴定一质量浓度的果胶溶液至溶液变粉色,1 min后溶液颜色不变化,则记录NaOH消耗体积;接着,用2.5 mL的3 mol/LNaOH溶液使样品溶液进行酯化反应,10 min后再用2.5 mL的3 mol/L HCl溶液终止反应,此时溶液粉色消失。最后,重复第1步操作,记录第2次消耗的0.1 mol/L NaOH溶液体积,样品酯化度(DE)根据式(2)来计算。
(2) 式中:DE表示酯化度,%;V1表示0.1 mol/L NaOH溶液第1次滴定消耗体积,mL;V2表示0.1 mol/L NaOH溶液第2次滴定消耗体积,mL。
1.2.8 分子量测定
改性前后的果胶分子量采用凝胶渗透色谱进行测定,取适量样品溶解于超纯水配制成1 mg/mL,样品溶液通过0.22 μm微孔膜后上机检测。色谱柱为UltrahydrogelTM Guard Column(6×40 mm)、UltrahydrogelTM 500 Column(7.8×300 mm)和UltrahydrogelTM 250 Column (7.8×300 mm),检测器为Waters 2414示差折光(RI)检测器,在此条件下,上样体积20 μL,0.1 mol/L NaNO3作为流动相,其流速为0.8 mL/min,柱温35 ℃。
1.2.9 单糖组成测定
利用Thermo ICS 5000+离子色谱系统对样品中的单糖组分进行精确分析。参考Wang等[14]的方法,分别准确称取所需标准品后,加入超纯水配成10 mg/mL标准溶液母液单标,然后取适量标准品母液单标混合配制成一系列质量浓度梯度,并对样品进行前处理。参照Salvador等[15]的测定方法,选用为Dionex™ CarboPac™ PA20(150×3.0 mm,10 μm)为色谱柱,结合电化学检测器,设置进样量为5 μL,流动相A(H2O),流动相B(0.1 mol/L NaOH),流动相C(0.1 mol/L NaOH,0.2 mol/L NaAc),流速0.5 mL/min;柱温为30 ℃。
1.2.10 红外光谱测定
将适量样品粉末与干燥后的溴化钾固体粉末均匀混合后压成片剂,红外光谱扫描范围为4000~500 cm−1。
1.2.11 热力学测定
热力学测定参照李文佳[16]的方法稍作修改,差示扫描量热法。将大约5 mg的样品粉末放入固体型铝坩埚内,密封好并记录样品质量,同时使用空的固体型铝坩埚作为参照。温度从起始温度40 ℃升温至350 ℃,升温速率为10 ℃/min,氮气为保护气体和冷却气体。
1.2.12 扫描电镜
取少量干燥的果胶样品均匀沾到样品台的导电胶上,氮气吹扫残余的样品的粉末后,用离子喷射仪镀上导电膜,使用扫描电子显微镜选择500倍率对样品进行微观形态分析。
1.3 数据处理
数据平行测定三次,实验数据以平均值±标准差(Meant±SD)表示,使用SPSS 26.0软件对数据进行统计学分析,各组数据采用独立样本t检验比较差异性,显著水平为P<0.05。响应面试验数据通过Design Expert 10.0.7软件进行分析,单糖组成数据利用软件Chromeleon处理色谱数据,图形的绘制采用OriginPro 2021软件。
2. 结果与分析
2.1 超声辅助酶法提取菠萝蜜果皮果胶工艺及优化
2.1.1 不同加酶量对果胶得率的影响
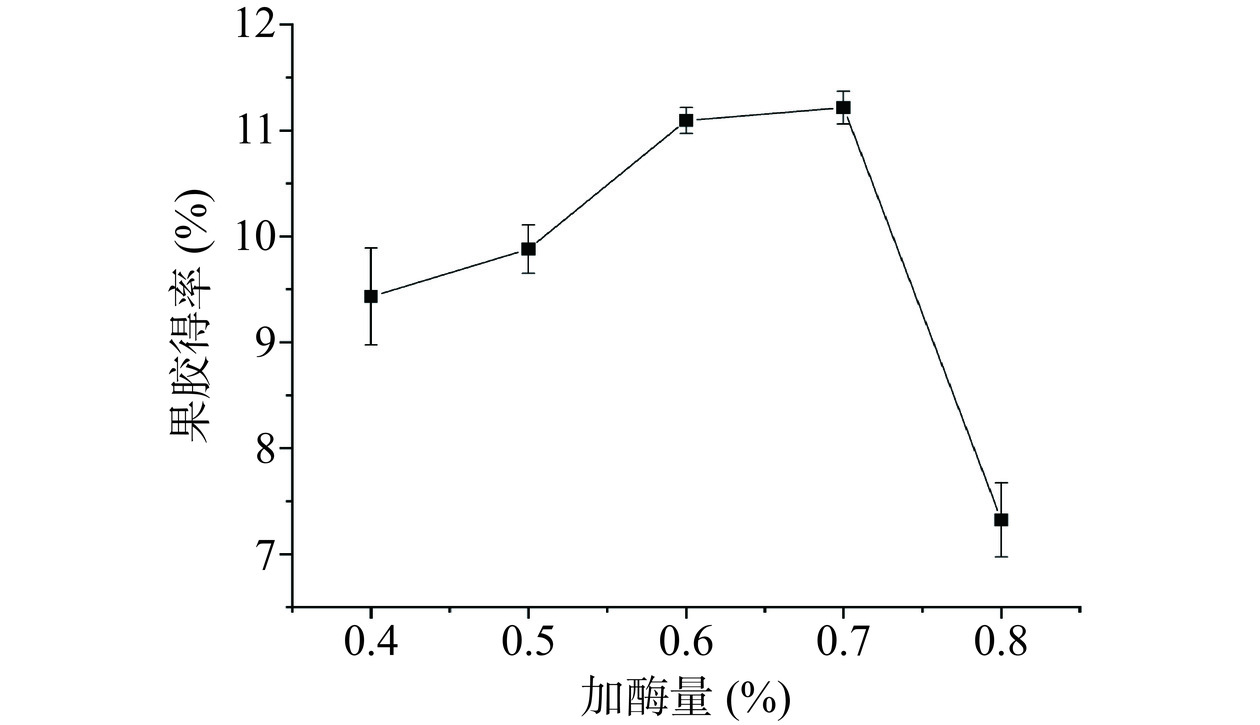
由图1可知,加酶量增加致果胶得率也增加,当加酶量为0.7%时,果胶得率达到最大,随后加酶量继续增加果胶得率反而减小,其原因可能是实验所用纤维素酶纯度并非纯酶,复合酶系中可能存在可以水解果胶的酶,如β-葡聚糖酶、半乳糖苷酶等[17],于是当酶添加量上升到一定程度时,会使果胶分子发生小部分水解,同时水解部分的果胶分子量降低,导致醇沉不完全,最终果胶得率下降。故加酶量最佳值为0.7%。
2.1.2 不同酶解温度对果胶得率的影响
由图2可知,当温度为30 ℃时,果胶得率最大,超过此温度得率下降。此实验所用纤维素酶最适温度为45 ℃,但实验结果表明,最佳酶解温度为30 ℃,其原因可能是酶在长时间的反应过程中会有消耗,随着消耗自身温度增加,会减缓酶的作用,因此降低反应温度后,反而可以使酶保持较高活性。
2.1.3 不同pH对果胶得率的影响
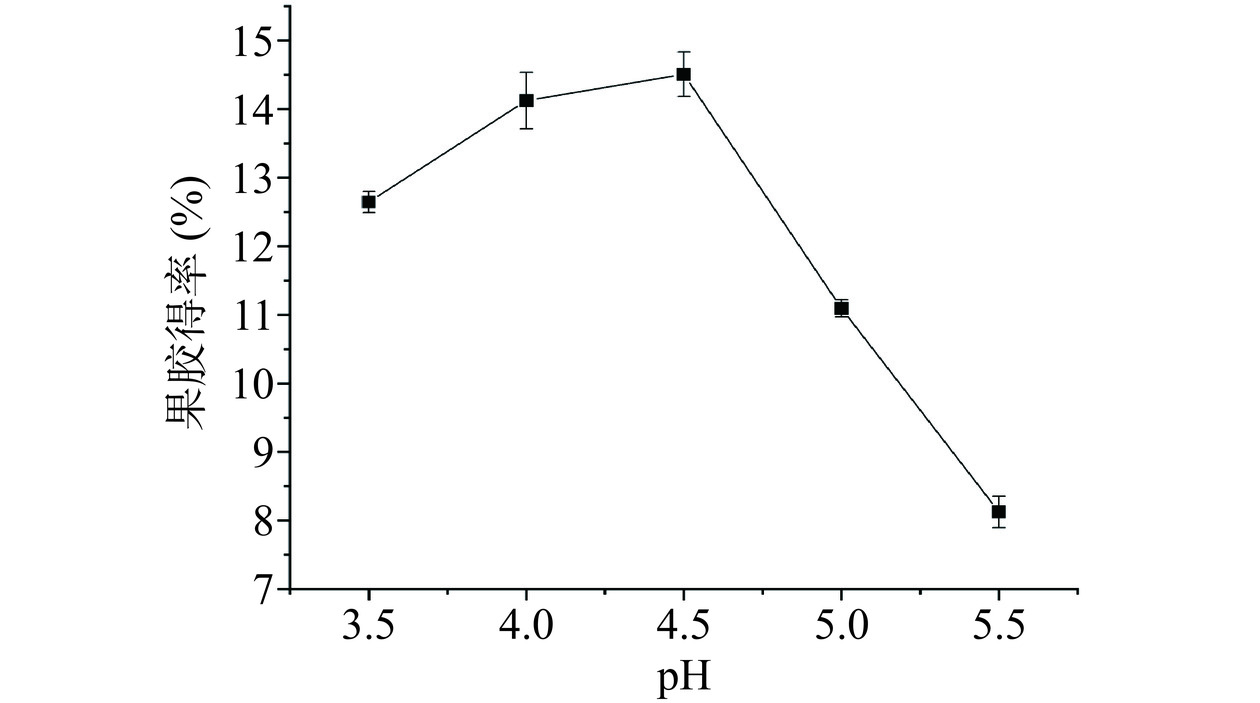
根据图3,当pH达到4.5时,果胶得率最大,因为该pH与纤维素酶的最佳工作pH相近。当pH>4.5时,果胶得率下降,这可能是由于pH条件逐渐远离酶的最适pH,以及pH增大会导致一部分果胶分子会水解为果胶酸,使得果胶得率下降。因此pH 4.5为最佳提取pH。
2.1.4 响应面试验结果与分析
2.1.4.1 模型的建立及显著性检验
在表2中给出了响应面试验的设计和测试结果。表3是对表2中试验结果所作的方差分析,由表3可知,回归方程模型的P<0.01,说明此模型极显著;该模型的失拟项P值为0.5038>0.05,不显著,说明零水平处拟合良好;R2Adj调整系数为0.9238,可说明92.38%的响应值变化可以通过该模型进行解释。R2决定系数为0.9667,表明实际值与预测值相关程度越高。因此,该模型可以较好地反映提取菠萝蜜果皮果胶的过程中各因素与响应值的关系,并对最佳提取工艺参数作出预测。对响应面实验结果进行多元二次回归分析,得到的二次多元回归方程如下:
表 2 响应面试验设计与结果Table 2. Design and results of response surface experimental实验号 A加酶量(%) B酶解温度(℃) C pH 果胶得率(%) 1 0.6 25 4.5 13.31±0.09 2 0.8 25 4.5 12.84±0.04 3 0.6 35 4.5 12.91±0.08 4 0.8 35 4.5 13.94±0.09 5 0.6 30 4 13.83±0.10 6 0.8 30 4 12.89±0.06 7 0.6 30 5 13.46±0.05 8 0.8 30 5 14.35±0.09 9 0.7 25 4 13.34±0.09 10 0.7 35 4 12.65±0.03 11 0.7 25 5 13.42±0.02 12 0.7 35 5 13.77±0.06 13 0.7 30 4.5 15.25±0.04 14 0.7 30 4.5 14.88±0.04 15 0.7 30 4.5 15.31±0.02 16 0.7 30 4.5 15.24±0.06 17 0.7 30 4.5 15.01±0.02 表 3 回归模型方差分析Table 3. Regression model analysis of variance方差来源 平方和 自由度 均方 F值 P值 显著性差异 模型 12.81 9 1.42 22.56 0.0002 ** A-加酶量 0.032 1 0.032 0.51 0.4994 B-酶解温度 0.0164 1 0.0164 0.26 0.626 C-pH 0.6578 1 0.6578 10.43 0.0145 * AB 0.5595 1 0.5595 8.87 0.0206 * AC 0.8354 1 0.8354 13.24 0.0083 ** BC 0.2694 1 0.2694 4.27 0.0777 A² 2.35 1 2.35 37.32 0.0005 ** B² 4.96 1 4.96 78.61 <0.0001 ** C² 2.08 1 2.08 32.97 0.0007 ** 残差 0.4417 7 0.0631 失拟项 0.1815 3 0.0605 0.93 0.5038 纯误差 0.2602 4 0.065 总离差 13.25 16 R2 0.9667 R2Adj 0.9238 注:*表示差异显著(P<0.05);**表示差异极显著(P<0.01)。 果胶得率(%) = 15.08 + 0.0633A + 0.0453B +0.2868C+0.374AB+0.457AC+0.2595BC−0.7478A2−1.09B2−0.7028C2
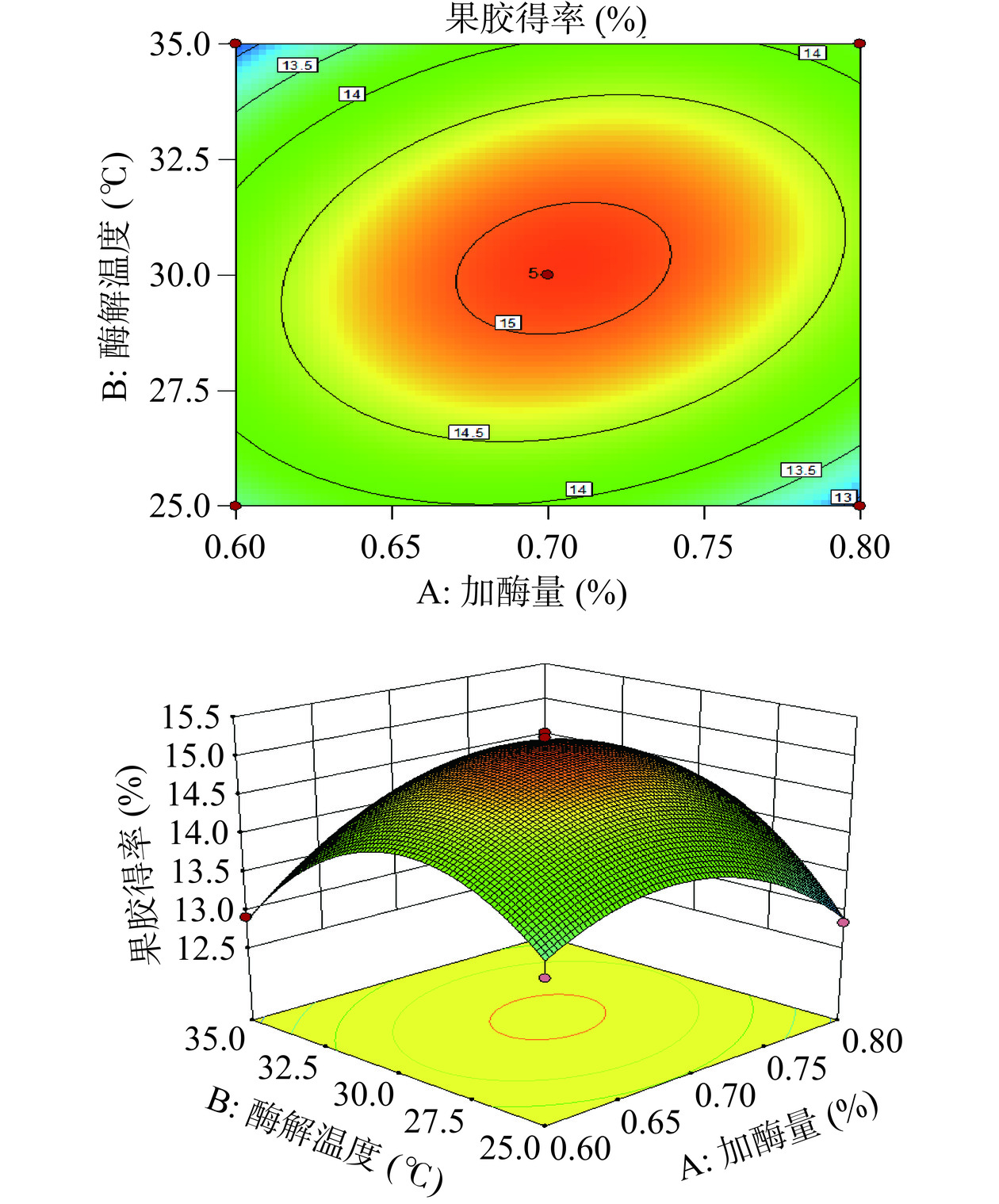
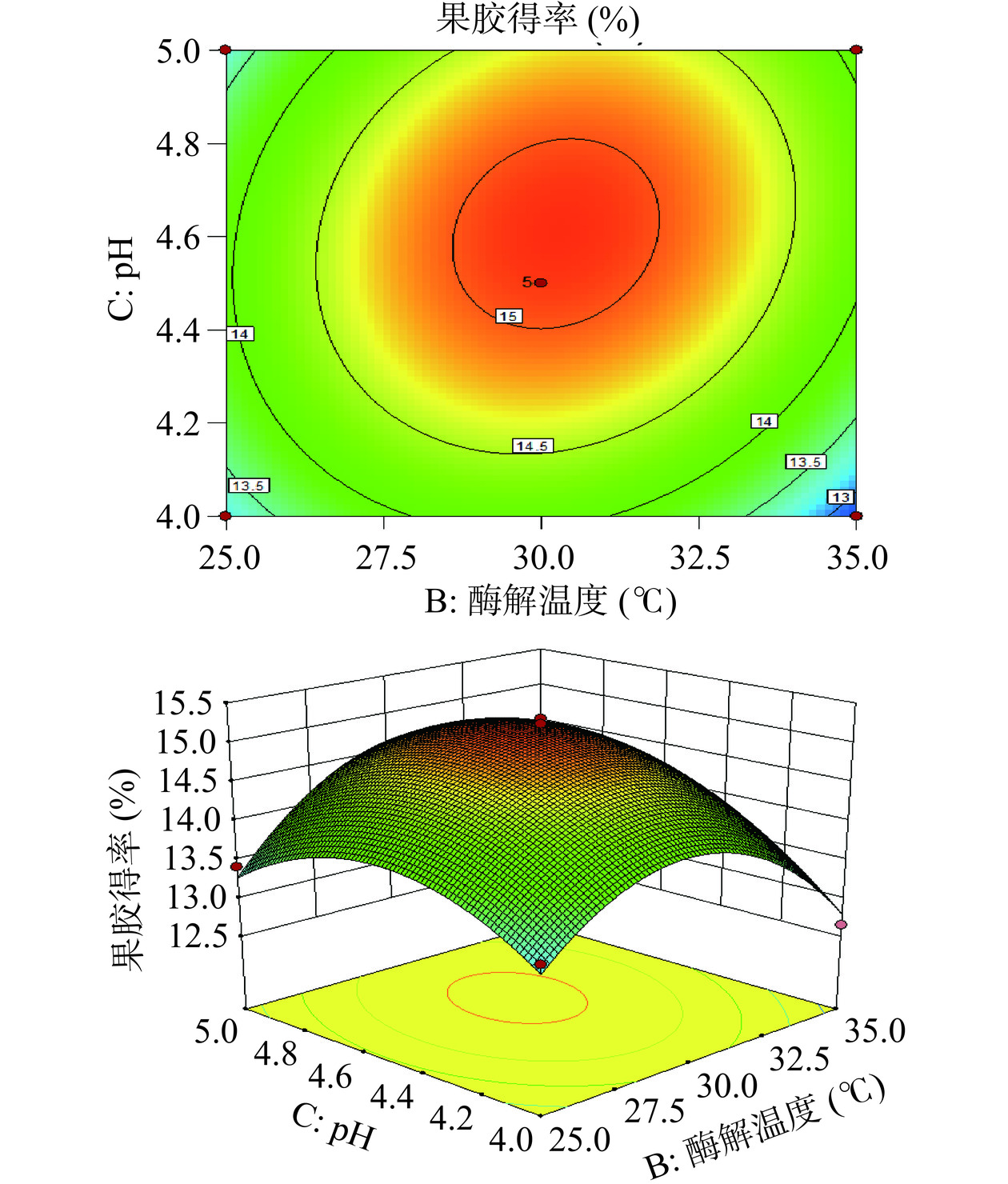
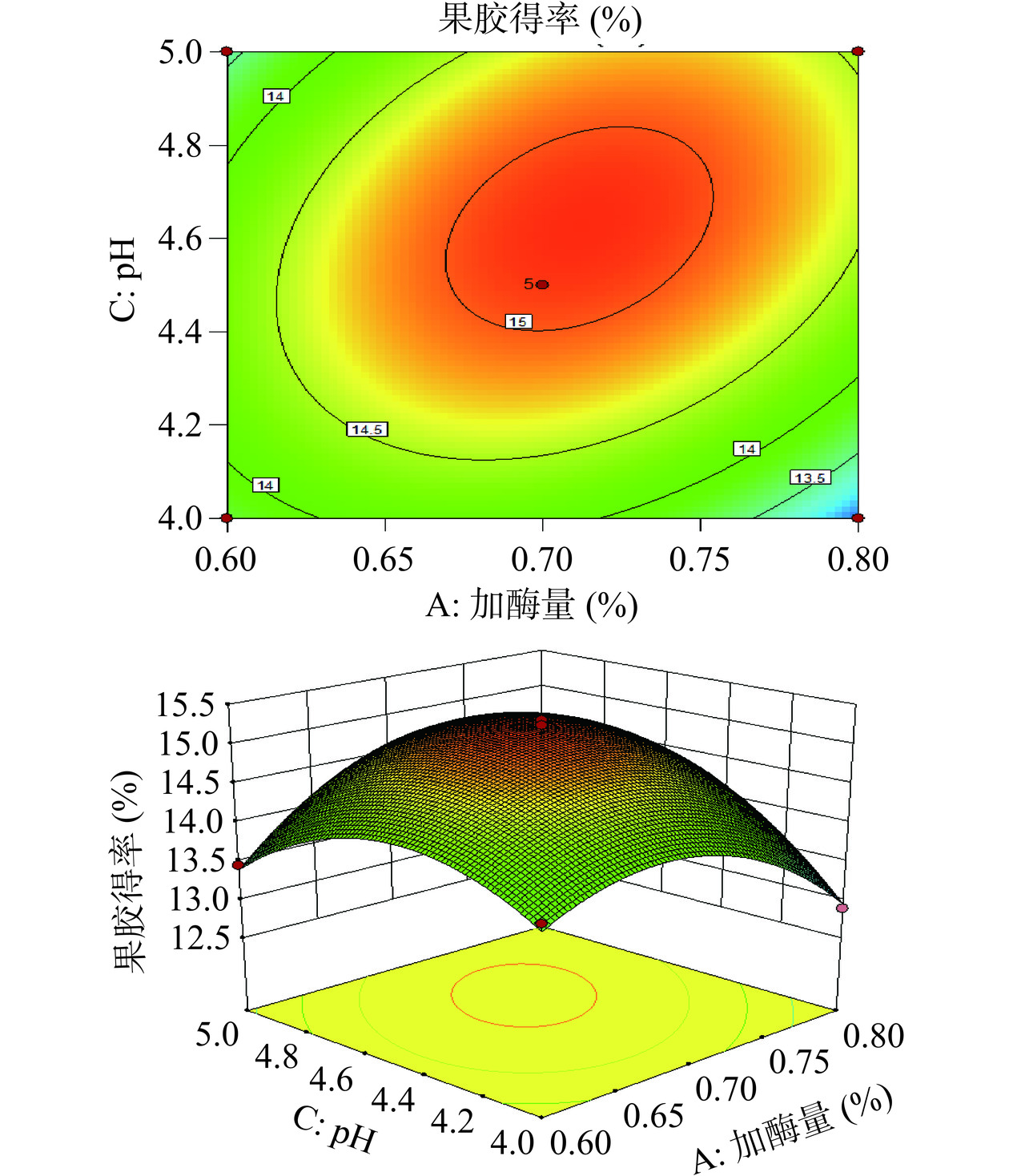
2.1.4.2 响应面图和等高线图分析
图4~图6为加酶量、酶解温度、pH对果胶得率影响的响应曲面图和等高线图。由表3的F值可知,三个因素对果胶得率的影响顺序为:C>A>B,即pH>加酶量>酶解温度。对于AB项,P<0.05,且由图4可看出,等高线分布密集且趋于椭圆形,说明交互项AB对果胶得率有显著影响。当加酶量由0.6%增加至0.71%,酶解温度由25 ℃升至30.38 ℃时,二者具有协同作用。对于AC项,P<0.01,图5显示交互项AC对果胶得率影响极显著。由图6可知,在确保加酶量一定时,交互项BC的等高线排列稀疏,且趋于圆形,说明交互项BC对响应值的影响不显著。
2.1.5 最佳提取工艺条件及验证
通过软件分析可得,最优工艺参数为加酶量0.71%,酶解温度30.38 ℃,pH为4.63,此条件下的果胶得率预测值为15.13%。根据实际的实验条件,将工艺条件修改为加酶量0.7%,酶解温度30.4 ℃,pH为4.6,做三次平行试验,果胶得率为15.26%±0.07%,与理论值接近,说明此响应面优化的工艺参数真实可信。
2.2 改性前后菠萝蜜果皮果胶的理化特性
2.2.1 基本成分测定
JFPP和DE-JFPP的理化性质如表4所示。JFPP和DE-JFPP均含有极少量的灰分、蛋白质和脂肪,两者均是在酸性条件下提取,且DE-JFPP仍是在酸性条件下进行低酯化改性,Begum等[18]在研究中发现用酸化的醇来洗涤果胶样品可降低灰分含量。因此,经过两次酸化醇沉的DE-JFPP的果胶分子与一些无机盐的离子键结合会发生水解从而使灰分含量比JFPP略低。同时,酸性条件会影响蛋白质的降解程度。因此,DE-JFPP的蛋白质含量较低。JFPP的总糖含量为43.42%,比DE-JFPP的总糖含量略高,但两者差异不显著(P>0.05),说明低酯化改性对总糖含量影响较小。半乳糖醛酸含量通常用来反应果胶含量的多少,JFPP和DE-JFPP的半乳糖醛酸含量分别为79.10%和83.24%,说明所得果胶纯度较高且符合商业果胶标准(DE>65%)[19]。低酯化后,DE-JFPP的半乳糖醛酸含量略有上升,但并无显著差异(P>0.05),其原因是果胶甲基酯酶催化HG在GalA的O-6上的特异性去甲氧基化,释放甲醇和质子,并在果胶链上产生可解离的羧基[20],这使得部分果胶分子侧链发生降解,但并不影响主链。
表 4 改性前后菠萝蜜果皮果胶的基本成分(%)Table 4. Basic components of pectin of jackfruit peel before and after modification (%)样品 水分含量 脂肪含量 灰分含量 蛋白质含量 半乳糖醛酸含量 总糖含量 JFPP 13.35±0.12 0.11±0.03 3.87±0.17 1.84±0.09 79.10±1.53 43.42±0.28 DE-JFPP 12.86±0.08 0.10±0.01 3.52±0.11 1.67±0.05 83.24±2.22 41.90±0.13 2.2.2 果胶分子量和酯化度
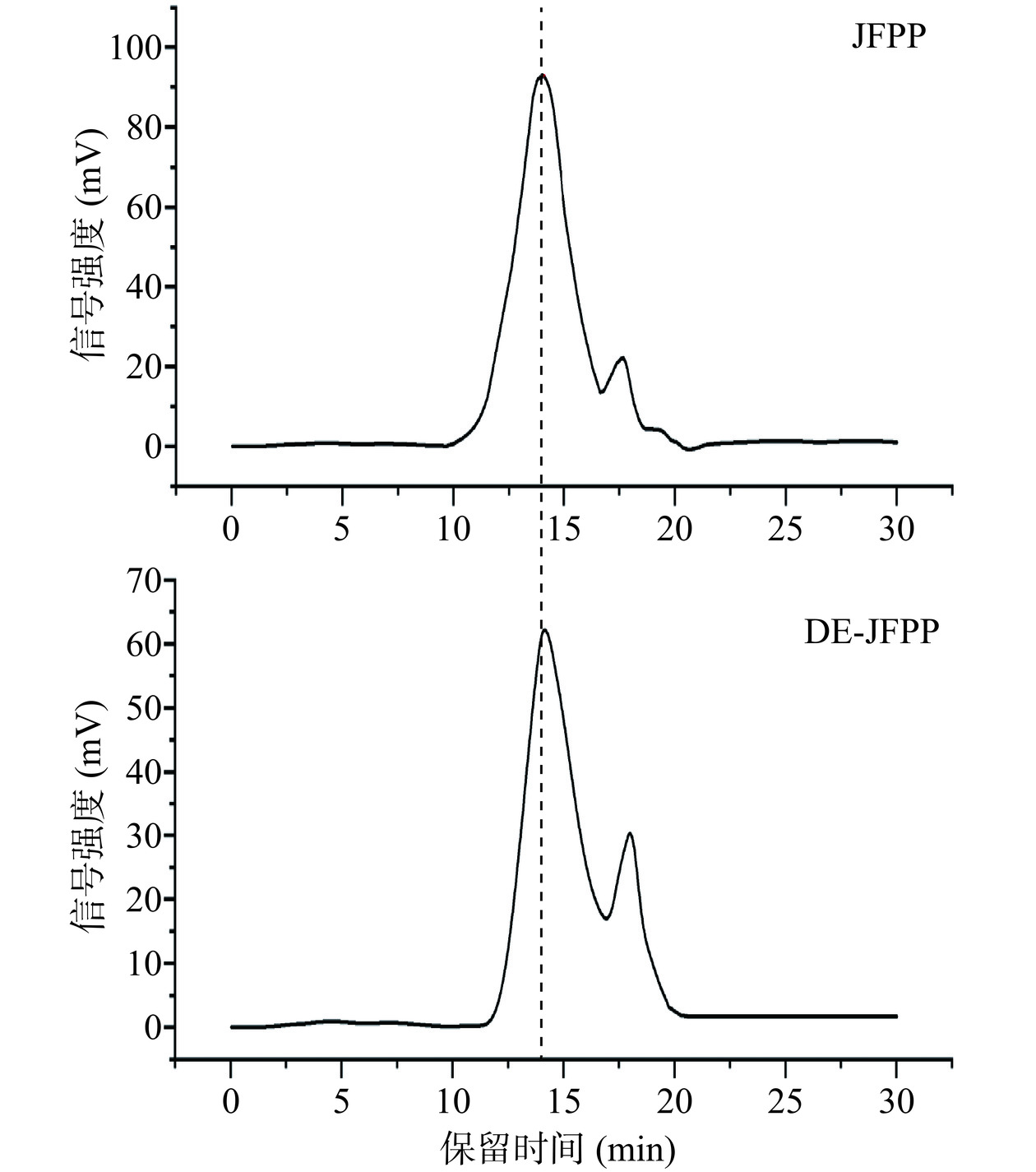
多糖的生物活性通常与分子量相关,例如,当一些多糖在分子量减小的同时表现为特性粘度降低、水溶性增加和生物活性增强[14],因此需要对果胶的分子量进行研究。由图7和表5可知,JFPP和DE-JFPP均呈现“高头+低尾”式的双峰状态,说明二者并不是由同等分子量片段组成的均一性多糖,这可能是由于聚合条件的不同,果胶分子中含有一定量的线型或环状的低聚体,而导致产物分子量分布出现差异,改性前后果胶的多分散系数(Mw/Mn)均大于1,代表果胶的分子量分布较广。JFPP和DE-JFPP的大分子量峰保留时间分别为14.01 min和14.17 min,重均分子量(Mw)分别为29.24 ku和28.49 ku,可看出改性后分子量差异不显著(P>0.05),此结果与Kim等[21]的研究结果相同,果胶甲酯酶对果胶分子量影响十分微小,因为果胶甲酯酶专一作用于半乳糖醛酸上的甲氧基团从而避免果胶分子链的降解。与Xu等[22]采用超声-微波辅助法提取的菠萝蜜果皮果胶(UM-P)相比,其Mw为51.5 ku,改性后的DE-JFPP分子量更小,也说明DE-JFPP具有更好的溶解性,更容易满足食品加工的需求,同时,果胶更容易被机体吸收而进入血液循环[23]。
表 5 改性前后菠萝蜜果皮果胶的的分子量和酯化度Table 5. Molecular weight and esterification degree of pectin of jackfruit peel before and after modification样品 Mw(ku) Mn(ku) Mw/Mn 酯化度(%) JFPP 29.24 2.56 11.42 84.25±0.75 DE-JFPP 28.49 2.49 11.44 32.36±0.81 JFPP酯化度(84.25%)大于50%,属于高酯果胶,与两种商业柑橘果胶(63.41%、61.63%)和商业苹果果胶(54.8%)相比[24],JFPP酯化度较高。低酯化后,DE-JFPP酯化度为32.36%,果胶的酯化度显著降低。赵文昌等[25]的研究表明,酯化度会影响药物的释放水平,肠溶包衣的低酯果胶骨架片靶向性强,能够使递送物质定位释放,从而提高疗效。因此,与JFPP相比,DE-JFPP的凝胶机理在生物活性物质递送方面的应用具有很大潜力。
2.2.3 单糖组成分析
各单糖含量以摩尔质量比表示。由表6可知,JFPP和DE-JFPP均主要由Rha、Ara、Gal、GalA组成,并含有少量的Glc、Fuc、Xyl、Man、GulA、GlcA、ManA,这表明酶法改性并不会改变样品的单糖类型。其中半乳糖醛酸(GalA)占比最高,分别为45.07mol%和50.21mol%,这一结果与2.2.1中测得DE-JFPP半乳糖醛酸含量较高的结果一致。根据章智[26]的方法计算JFPP和DE-JFPP中HG、RG-I所占的摩尔比,JFPP中HG、RG-I的摩尔比分别为37.66mol%和41.05mol%,DE-JFPP中HG、RG-I的摩尔比分别为40.69mol%和42.88mol%,可看出酶法低酯化并不会使HG主链发生降解,且低酯化后的果胶HG摩尔比增加,而HG链是由α-1,4糖苷键连接的D-半乳糖醛酸组成,其结果与改性后GalA含量升高的结果相对应;改性后的果胶RG-I摩尔比略有增加但差异并不显著(P>0.05)。Rha/GalA表示RG-I骨架的长度,两种果胶的Rha/GalA分别为0.16,处于0.05~1之间,可说明JFPP和DE-JFPP均属于RG-I型果胶[27]。(Gal+Ara)/Rha的摩尔比反应了RG-I区中性糖的侧链分支平均尺寸[28],JFPP和DE-JFPP的(Gal+Ara)/Rha摩尔比分别为3.54和3.40,说明两种果胶均含有一定的侧链和毛发区,改性后的果胶支链化程度减小,其原因可能是果胶甲酯酶会使果胶侧链发生部分降解。与Begum等[4]采用草酸铵提取的菠萝蜜废果胶(AOJP)相比,AOJP主要为HG型果胶,说明不同的提取方法会对果胶分子的结构有影响。郑家琪[29]在其研究中证实了RG-I型果胶阿拉伯糖侧链的缠结促进果胶链间的相互作用,并帮助形成稳定的网络结构,提高RG-I型果胶的凝胶能力,并缩短了聚合物链间的距离,有利于果胶链间的相互作用,说明改性后的果胶DE-JFPP具有开发复配RG-I型果胶凝胶递送体系的潜力。
表 6 改性前后菠萝蜜果皮果胶的单糖组成Table 6. Monosaccharide composition of pectin in jackfruit peel before and after modification组分 线性方程 R2 JFPP单糖含量
(mol%)DE-JFPP单糖
含量(mol%)岩藻糖(Fuc) Y=0.8798x 0.9968 0.42±0.00 0.39±0.00 鼠李糖(Rha) Y=0.7360x 0.9957 7.41±0.23 8.02±0.08 阿拉伯糖(Ara) Y=1.0439x 0.9986 12.24±0.47 11.73±0.17 半乳糖(Gal) Y=1.1206x 0.9989 13.99±0.53 15.53±0.68 葡萄糖(Glc) Y=1.2935x 0.9978 5.35±0.16 3.31±0.05 木糖(Xyl) Y=1.0094x 0.9939 1.71±0.02 0.58±0.00 甘露糖(Man) Y=0.8026x 0.9977 2.46±0.11 1.86±0.09 半乳糖醛酸(GalA) Y=0.1580x 0.9916 45.07±0.98 48.71±0.37 古罗糖醛酸(GulA) Y=0.1488x 0.9925 4.05±0.13 4.81±0.22 葡萄糖醛酸(GlcA) Y=0.3755x 0.9980 5.58±0.21 4.37±0.14 甘露糖醛酸(ManA) Y=0.2012x 0.9901 1.71±0.01 0.69±0.01 Rha/GalA − − 0.16±0.00 0.16±0.01 (Gal+Ara)/Rha − − 3.54±0.14 3.40±0.23 HG(GalA-Rha) − − 37.66±0.41 40.69±0.59 RG-I(2Rha+Ara+Gal) − − 41.05±0.86 42.88±0.83 2.2.4 红外光谱分析
由图8可知,改性前后的果胶均在3600~3000 cm−1范围出现宽吸收峰,是由于GalA主链分子间和分子内氢键中的O−H基团的拉伸振动引起的。2950 cm−1附近的峰是由果胶中C−H基团引起的吸收,包括CH、CH2和CH3的拉伸和弯曲振动[30],由于酶法低酯化会使果胶分子脱去甲氧基,因此导致DE-JFPP在此处的吸收峰面积下降。1740 cm−1附近的峰对应于酯化羧基(-COOR),1630 cm−1附近的峰对应于游离羧基(-COO−),这两处峰均为的果胶特征吸收峰,1400 cm−1对应于是C-O的伸缩振动,可看出JFPP改性后,在1740 cm−1和1400 cm−1附近的吸收峰面积明显下降,这是由于低酯化过程中半乳糖醛酸残基中的甲氧基被除去并将C-6转化为羧酸,此结果与Liang等[31]的研究结果一致。1240 cm−1附近的峰对应于O-CH3,此处峰面积变化不明显。1200~950 cm−1间的吸收峰被认为是果胶多糖的指纹图谱区[18],因为它可以识别多糖中的主要化学基团,例如在1100 cm−1的出峰对应醚键(R-O-R),1012 cm−1左右对应C-C键[32],960 cm−1和830 cm−1附近的小型吸收峰说明改性前后的果胶均同时具有以α型和β型糖苷键[8]。
2.2.5 热力学分析
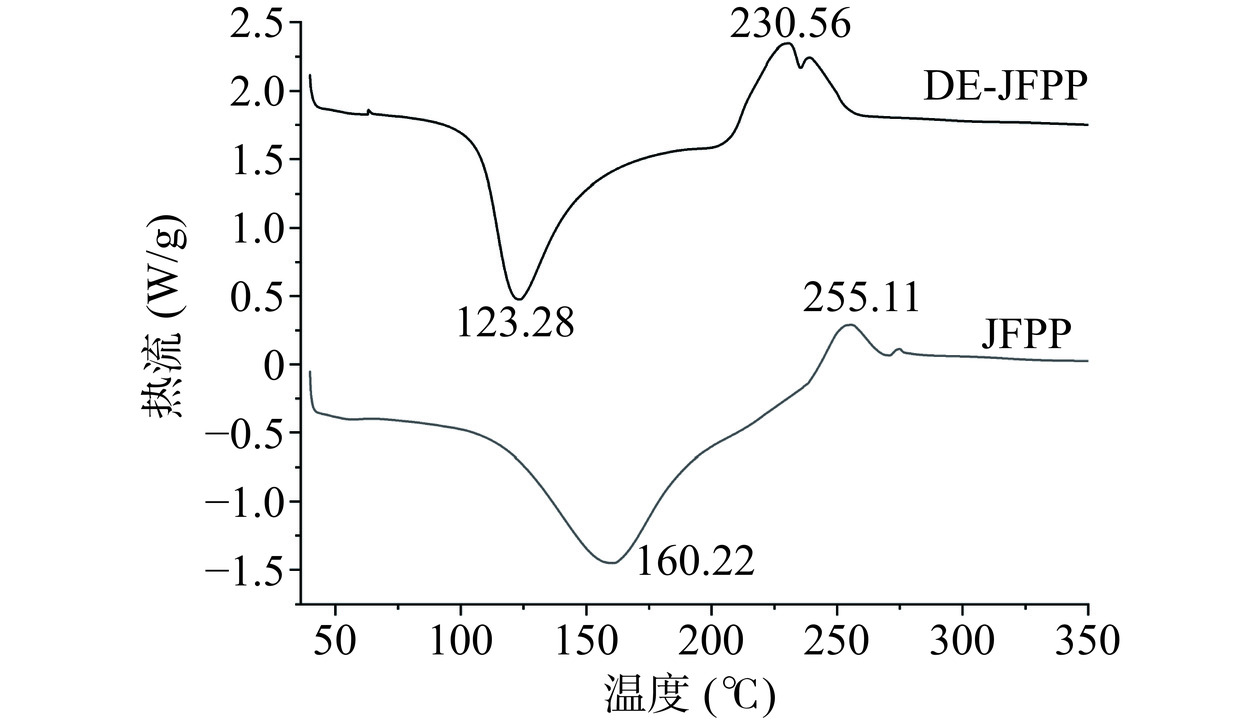
由图9可知,JFPP和DE-JFPP的DSC曲线有两个峰,第1个是明显的吸热峰,表明JFPP和DE-JFPP的溶解温度(Tm)分别为160.22和123.28 ℃,此位置出现吸热峰与样品中的水有关,在升温过程中,水分蒸发会产生吸热现象[33]。而酯化度、半乳糖醛酸含量会影响其持水能力,Iijima等[34]研究结果表明Tm和结晶度随酯化度的增加而增加,因为低酯化过程中果胶的结晶区被破坏了。因此低酯化后的DE-JFPP酯化度明显下降,因此溶解温度也降低。反之,由于JFPP的酯化度、半乳糖醛酸含量较高,使其具有较强的持水能力,与李文佳[16]用亚临界水提取的菠萝蜜果胶的相比,其溶解温度更高。此外,在吸热过程中,半乳糖醛酸环可能会发生氢键和结构上的变化,从稳定的4C1椅式构象变为逆1C4椅式构象[35]。第2个峰是放热峰,表明JFPP和DE-JFPP的降解温度(Td)分别为在255.11和230.56 ℃,此时果胶开始发生降解,果胶分子中的糖苷键被随机击穿从而释放出大量热量。此外,两种果胶的放热峰附近均出现较小的杂峰,可能是由于样品中含有的杂质引起的。热稳定性是果胶作为添加剂应用于食品工业中的重要性质之一,由热力学分析可知改性前后的果胶均具有较好的热稳定性,均可满足在热加工食品中应用。
2.2.6 微观形态观察
图10A和图10B是JFPP和DE-JFPP在500倍率下的微观图像。如图图10所示,JFPP是不规则的片状结构,DE-JFPP呈现出的微观形态更接近不规则的颗粒粉末状。JFPP的表面形貌较光滑但略有凸起,褶皱不明显边缘较锋利,结构较紧凑;DE-JFPP表面粗糙有颗粒,结构疏松,因为PME不会切断果胶分子的HG主干,可能是HG上负电荷增加导致的物理变化的结果,这导致HG链的电荷排斥和壁肿胀,进而影响压痕特性[36]。根据改性后果胶结构疏松的结果,可推测改性后的果胶吸附性能提高,对于与其他生理活性物质的结合具有良好的适应性。同时,两种果胶与李文佳[16]用亚临界水提取的菠萝蜜果皮果胶表面形貌存在一定的差异,亚临界水提取的果胶结构更紧凑,呈不平整的层状结构,表面聚集一些不规则的颗粒,这说明提取方式的不同会导致果胶的表面结构有所差异。
3. 结论
经加酶量、酶解温度、pH三个因素的响应面优化试验,以JFPP的得率为指标进行工艺条件优化,确定最佳工艺条件为加酶量0.7%,酶解温度30.4 ℃,pH为4.6,此条件下JFPP得率为15.26%±0.07%。
果胶经初步纯化后进行酶法低酯化改性,并研究改性前后果胶的理化性质及结构表征。结果表明,酶法低酯化对果胶的基本成分含量影响较小,改性前后的果胶水分含量、脂肪含量、灰分含量、蛋白质含量和总糖含量变化不显著(P>0.05),改性后果胶的半乳糖醛酸含量由79.10%增加至83.24%,但变化并不显著(P>0.05)。JFPP和DE-JFPP的酯化度分别为84.25%和32.36%,改性后酯化度显著下降(P<0.05),重均分子量分别为29.24 ku和28.49 ku,改性后分子量略微降低但变化不显著(P>0.05)。JFPP和DE-JFPP均含有11种单糖,单糖类型相同,且均为RG-I型果胶。果胶的红外光谱显示,JFPP与DE-JFPP均具有典型的果胶多糖特征吸收峰,改性后,果胶分子对应于酯化羧基的吸收峰峰面积减小。与改性前果胶相比,改性后的果胶溶解温度和降解温度分别下降为123.28 ℃和230.56 ℃,但仍具有相对较高的热稳定性。JFPP和DE-JFPP的微观形态存在一定差别,JFPP表面更光滑,结构紧凑,DE-JFPP表面粗糙,结构疏松。
本研究优化了超声辅助酶法提取JFPP的工艺,经优化后果胶得率有所提高,但还需进一步探讨超声条件对提取工艺的影响,从而为JFPP的提取工艺研究提供理论依据。初步纯化果胶后,采用酶法低酯化改性成功制备了低酯化度、高纯度的DE-JFPP,该法有效保护了果胶分子,避免其发生降解。改性后果胶凝胶机制的改变,使其在负载体系的构建上具有很好的开发应用潜力,并提高了菠萝蜜加工废弃物的附加值。
-
表 1 响应面因素水平设计
Table 1 Response surface factor level design
水平 因素 A加酶量(%) B酶解温度(℃) C pH −1 0.6 25 4 0 0.7 30 4.5 1 0.8 35 5 表 2 响应面试验设计与结果
Table 2 Design and results of response surface experimental
实验号 A加酶量(%) B酶解温度(℃) C pH 果胶得率(%) 1 0.6 25 4.5 13.31±0.09 2 0.8 25 4.5 12.84±0.04 3 0.6 35 4.5 12.91±0.08 4 0.8 35 4.5 13.94±0.09 5 0.6 30 4 13.83±0.10 6 0.8 30 4 12.89±0.06 7 0.6 30 5 13.46±0.05 8 0.8 30 5 14.35±0.09 9 0.7 25 4 13.34±0.09 10 0.7 35 4 12.65±0.03 11 0.7 25 5 13.42±0.02 12 0.7 35 5 13.77±0.06 13 0.7 30 4.5 15.25±0.04 14 0.7 30 4.5 14.88±0.04 15 0.7 30 4.5 15.31±0.02 16 0.7 30 4.5 15.24±0.06 17 0.7 30 4.5 15.01±0.02 表 3 回归模型方差分析
Table 3 Regression model analysis of variance
方差来源 平方和 自由度 均方 F值 P值 显著性差异 模型 12.81 9 1.42 22.56 0.0002 ** A-加酶量 0.032 1 0.032 0.51 0.4994 B-酶解温度 0.0164 1 0.0164 0.26 0.626 C-pH 0.6578 1 0.6578 10.43 0.0145 * AB 0.5595 1 0.5595 8.87 0.0206 * AC 0.8354 1 0.8354 13.24 0.0083 ** BC 0.2694 1 0.2694 4.27 0.0777 A² 2.35 1 2.35 37.32 0.0005 ** B² 4.96 1 4.96 78.61 <0.0001 ** C² 2.08 1 2.08 32.97 0.0007 ** 残差 0.4417 7 0.0631 失拟项 0.1815 3 0.0605 0.93 0.5038 纯误差 0.2602 4 0.065 总离差 13.25 16 R2 0.9667 R2Adj 0.9238 注:*表示差异显著(P<0.05);**表示差异极显著(P<0.01)。 表 4 改性前后菠萝蜜果皮果胶的基本成分(%)
Table 4 Basic components of pectin of jackfruit peel before and after modification (%)
样品 水分含量 脂肪含量 灰分含量 蛋白质含量 半乳糖醛酸含量 总糖含量 JFPP 13.35±0.12 0.11±0.03 3.87±0.17 1.84±0.09 79.10±1.53 43.42±0.28 DE-JFPP 12.86±0.08 0.10±0.01 3.52±0.11 1.67±0.05 83.24±2.22 41.90±0.13 表 5 改性前后菠萝蜜果皮果胶的的分子量和酯化度
Table 5 Molecular weight and esterification degree of pectin of jackfruit peel before and after modification
样品 Mw(ku) Mn(ku) Mw/Mn 酯化度(%) JFPP 29.24 2.56 11.42 84.25±0.75 DE-JFPP 28.49 2.49 11.44 32.36±0.81 表 6 改性前后菠萝蜜果皮果胶的单糖组成
Table 6 Monosaccharide composition of pectin in jackfruit peel before and after modification
组分 线性方程 R2 JFPP单糖含量
(mol%)DE-JFPP单糖
含量(mol%)岩藻糖(Fuc) Y=0.8798x 0.9968 0.42±0.00 0.39±0.00 鼠李糖(Rha) Y=0.7360x 0.9957 7.41±0.23 8.02±0.08 阿拉伯糖(Ara) Y=1.0439x 0.9986 12.24±0.47 11.73±0.17 半乳糖(Gal) Y=1.1206x 0.9989 13.99±0.53 15.53±0.68 葡萄糖(Glc) Y=1.2935x 0.9978 5.35±0.16 3.31±0.05 木糖(Xyl) Y=1.0094x 0.9939 1.71±0.02 0.58±0.00 甘露糖(Man) Y=0.8026x 0.9977 2.46±0.11 1.86±0.09 半乳糖醛酸(GalA) Y=0.1580x 0.9916 45.07±0.98 48.71±0.37 古罗糖醛酸(GulA) Y=0.1488x 0.9925 4.05±0.13 4.81±0.22 葡萄糖醛酸(GlcA) Y=0.3755x 0.9980 5.58±0.21 4.37±0.14 甘露糖醛酸(ManA) Y=0.2012x 0.9901 1.71±0.01 0.69±0.01 Rha/GalA − − 0.16±0.00 0.16±0.01 (Gal+Ara)/Rha − − 3.54±0.14 3.40±0.23 HG(GalA-Rha) − − 37.66±0.41 40.69±0.59 RG-I(2Rha+Ara+Gal) − − 41.05±0.86 42.88±0.83 -
[1] 黄浩燃, 张星启, 温辉翠, 等. 球磨处理对菠萝蜜果皮不溶性膳食纤维结构及性能的影响[J]. 食品工业科技,2023,44(11):211−218. [HUANG H R, ZHANG X Q, WEN H C, et al. Effect of ball milling on the structure and properties of insoluble dietary fiber in jackfruit peel[J]. Science and Technology of Food Industry,2023,44(11):211−218.] HUANG H R, ZHANG X Q, WEN H C, et al. Effect of ball milling on the structure and properties of insoluble dietary fiber in jackfruit peel[J]. Science and Technology of Food Industry, 2023, 44(11): 211−218.
[2] 吕飞杰, 台建祥, 尹道娟, 等. 菠萝蜜副产品综合利用研发[J]. 中国热带农业,2015(1):9−12. [LÜ F J, TAI J X, YIN D J, et al. Development of comprehensive utilization of jackfruit by-product[J]. China Tropical Agriculture,2015(1):9−12.] doi: 10.3969/j.issn.1673-0658.2015.01.003 LÜ F J, TAI J X, YIN D J, et al. Development of comprehensive utilization of jackfruit by-product[J]. China Tropical Agriculture, 2015(1): 9−12. doi: 10.3969/j.issn.1673-0658.2015.01.003
[3] 台建祥, 范鸿雁, 薛慧, 等. 菠萝蜜果皮果胶提取工艺的优化[J]. 食品科技,2014,39(1):236−239. [TAI J X, FAN H Y, XUE H, et al. The optimum extraction process of pectin from jackfruit peel[J]. Food Science and Technology,2014,39(1):236−239.] TAI J X, FAN H Y, XUE H, et al. The optimum extraction process of pectin from jackfruit peel[J]. Food Science and Technology, 2014, 39(1): 236−239.
[4] BEGUM R, AZIZ M G, YUSOF Y A, et al. Evaluation of gelation properties of jackfruit (Artocarpus heterophyllus) waste pectin[J]. Carbohydrate Polymer Technologies and Applications,2021,2:100160. doi: 10.1016/j.carpta.2021.100160
[5] 刘英, 邱逸凡, 许希贤. 果胶研究和应用进展[J]. 现代食品,2019(24):17−20. [LIU Y, QIU Y F, XU X X. Research and applications of pectin[J]. Modern Food,2019(24):17−20.] LIU Y, QIU Y F, XU X X. Research and applications of pectin[J]. Modern Food, 2019(24): 17−20.
[6] CELUS M, KYOMUGASHO C, SALVIA-TRUJILLO L, et al. Interactions between citrus pectin and Zn2+ or Ca2+ and associated in vitro Zn2+ bioaccessibility as affected by degree of methylesterification and blockiness[J]. Food Hydrocoll,2018,79:319−330. doi: 10.1016/j.foodhyd.2018.01.003
[7] BASAK R, BANDYOPADHYAY R. Formation and rupture of Ca2+ induced pectin biopolymer gels[J]. Soft Matter,2014,10(37):7225−7233. doi: 10.1039/C4SM00748D
[8] 万力. 超高压辅助酶法果胶低酯化改性及其凝胶性能研究[D]. 武汉:华中农业大学, 2021. [WAN L. Study on de-esterified modification and its gel properties of pectin by high hydrostatic pressure assisted enzymatic method[D]. Wuhan:Huazhong Agricultural University, 2021.] WAN L. Study on de-esterified modification and its gel properties of pectin by high hydrostatic pressure assisted enzymatic method[D]. Wuhan: Huazhong Agricultural University, 2021.
[9] 吴彤, 冯进, 黄午阳, 等. 牛蒡果胶多糖/玉米醇溶蛋白复合颗粒稳定的Pickering乳液构建及对姜黄素的递送功效[J]. 食品科学,2023,44(14):37−46. [WU T, FENG J, HUANG W Y, et al. Fabrication of pickering emulsions stabilized by burdock rhamnogalacturonan I(RG-l)-Type pectin/zein composite particles and their utilization for the delivery of curcumin[J]. Food Science,2023,44(14):37−46.] doi: 10.7506/spkx1002-6630-20221102-014 WU T, FENG J, HUANG W Y, et al. Fabrication of pickering emulsions stabilized by burdock rhamnogalacturonan I(RG-l)-Type pectin/zein composite particles and their utilization for the delivery of curcumin[J]. Food Science, 2023, 44(14): 37−46. doi: 10.7506/spkx1002-6630-20221102-014
[10] LEE T, CHANG Y H. Structural, physicochemical, and in-vitro release properties of hydrogel beads produced by oligochitosan and de-esterified pectin from yuzu (Citrus junos) peel as a quercetin delivery system for colon target[J]. Food Hydrocolloids,2020,108:106086. doi: 10.1016/j.foodhyd.2020.106086
[11] 吕冰冰, 谢笔钧, 孙智达. 红肉番石榴果胶的理化特性及其体外降脂作用[J]. 食品工业科技,2021,42(20):51−60. [LÜ B B, XIE B J, SUN Z D. Physical and chemical properties of red-flesh guava pectin and its lipid-lowering effect in vitro[J]. Science and Technology of Food Industry,2021,42(20):51−60.] LÜ B B, XIE B J, SUN Z D. Physical and chemical properties of red-flesh guava pectin and its lipid-lowering effect in vitro[J]. Science and Technology of Food Industry, 2021, 42(20): 51−60.
[12] 孟凡磊, 褚智慧, 宋凤玲, 等. 改性石榴皮果胶性质及抗氧化活性[J]. 食品科技,2020,45(1):326−329. [MENG F L, CHU Z H, SONG F L, er al. Properties of modified pectins extracted from pomegranate peel and antioxidant activity[J]. Food Science and Technology,2020,45(1):326−329.] MENG F L, CHU Z H, SONG F L, er al. Properties of modified pectins extracted from pomegranate peel and antioxidant activity[J]. Food Science and Technology, 2020, 45(1): 326−329.
[13] 让凤菊, 王俊龙, 刘伟, 等. 西兰花茎果胶的提取及理化性质研究[J]. 食品研究与开发,2022,43(16):104−110. [RANG F J, WANG J L, LIU W, et al. Extraction and physicochemical characterization of pectin from broccoli stalks[J]. Food Research and Development,2022,43(16):104−110.] doi: 10.12161/j.issn.1005-6521.2022.16.013 RANG F J, WANG J L, LIU W, et al. Extraction and physicochemical characterization of pectin from broccoli stalks[J]. Food Research and Development, 2022, 43(16): 104−110. doi: 10.12161/j.issn.1005-6521.2022.16.013
[14] WANG L, ZHANG B, XIAO J, et al. Physicochemical, functional, and biological properties of water-soluble polysaccharides from Rosa roxburghii Tratt fruit[J]. Food Chemistry,2018,249:127−135. doi: 10.1016/j.foodchem.2018.01.011
[15] SALVADOR L D, SUGANUMA T, KITAHARA K, et al. Monosaccharide composition of sweetpotato fiber and cell wall polysaccharides from sweetpotato, cassava, and potato analyzed by the high-performance anion exchange chromatography with pulsed amperometric detection method[J]. Journal of Agricultural and Food Chemistry,2000,48(8):3448−3454. doi: 10.1021/jf991089z
[16] 李文佳. 亚临界水提取菠萝蜜果皮果胶多糖及其性能研究[D]. 海口:海南大学, 2019. [LI W J. Study on extraction and propertiies of pectic polysaccharides obtianed by subcritical water from jackfruit peel[D]. Haikou:Hainan University, 2019.] LI W J. Study on extraction and propertiies of pectic polysaccharides obtianed by subcritical water from jackfruit peel[D]. Haikou: Hainan University, 2019.
[17] 韩冬梅, 廖小军, 李淑燕, 等. 酶法制取橙皮果胶的研究[J]. 食品工业科技,2011,32(2):183−186. [HAN D M, LIAO X J, LI S Y, et al. Cellulase extraction of pectin from orange peel[J]. Science and Technology of Food Industry,2011,32(2):183−186.] HAN D M, LIAO X J, LI S Y, et al. Cellulase extraction of pectin from orange peel[J]. Science and Technology of Food Industry, 2011, 32(2): 183−186.
[18] BEGUM R, AZIZ M G, UDDIN M B, et al. Characterization of jackfruit (Artocarpus heterophyllus) waste pectin as influenced by various extraction conditions[J]. Agriculture and Agricultural Science Procedia,2014,2:244−251. doi: 10.1016/j.aaspro.2014.11.035
[19] 陈瑞云. 薜荔籽果胶自凝胶机制及其对淀粉性质影响[D]南昌:南昌大学, 2022. [CHEN R Y. The gelation and the effect on starch physicochemical properties mechanism of pectin from creeping fig[D]. Nanchang:Nanchang University, 2022.] CHEN R Y. The gelation and the effect on starch physicochemical properties mechanism of pectin from creeping fig[D]. Nanchang: Nanchang University, 2022.
[20] JOLIE R P, CHRISTIAENS S, DE ROECK A, et al. Pectin conversions under high pressure:implications for the structure-related quality characteristics of plant-based foods[J]. Trends in Food Science & Technology,2012,24(2):103−118.
[21] KIM Y, TENG Q, WICKER L. Action pattern of Valencia orange PME de-esterification of high methoxyl pectin and characterization of modified pectins[J]. Carbohydrate Research,2005,340(17):2620−2629. doi: 10.1016/j.carres.2005.09.013
[22] XU S Y, LIU J P, HUANG X S, et al. Ultrasonic-microwave assisted extraction, characterization and biological activity of pectin from jackfruit peel[J]. LWT - Food Science and Technology,2018,90:577−582. doi: 10.1016/j.lwt.2018.01.007
[23] 应姗姗. 火龙果皮中果胶提取及改性研究[D]. 杭州:浙江大学, 2014. [YING S S. Study on the extraction and modification of pectin from pitava peel[D]. Hangzhou:Zhejiang University, 2014.] YING S S. Study on the extraction and modification of pectin from pitava peel[D]. Hangzhou: Zhejiang University, 2014.
[24] LIU H Y, DAI T T, CHEN J, LIU W, et al. Extraction, characterization, and spontaneous gelation mechanism of pectin from Nicandra physaloides (Linn.) Gaertn seeds[J]. International Journal of Biological Macromolecules,2022,195:523−529. doi: 10.1016/j.ijbiomac.2021.12.032
[25] 赵文昌, 邓虹珠, 宋丽军, 等. 不同酯化度果胶对苦豆子总碱水凝胶骨架片体外释放的影响[J]. 中国中药杂志,2008(19):2188−2192. [ZHAO W C, DENG H Z, SONG L J, et al. Effect of pectins of different degree of esterification on in-vitro sophoridine release of hydrophilic matrix tablets containing total alkaloids of Sophora alopecuroides[J]. China Journal of Chinese Materia Medica,2008(19):2188−2192.] doi: 10.3321/j.issn:1001-5302.2008.19.009 ZHAO W C, DENG H Z, SONG L J, et al. Effect of pectins of different degree of esterification on in-vitro sophoridine release of hydrophilic matrix tablets containing total alkaloids of Sophora alopecuroides[J]. China Journal of Chinese Materia Medica, 2008(19): 2188−2192. doi: 10.3321/j.issn:1001-5302.2008.19.009
[26] 章智. 3种提取方法对重瓣栀子花果胶结构、流变和乳化性质的影响研究[D]. 杭州:浙江农林大学, 2022. [ZHANG Z. The research of the influence of three extraction methods on the structural, rheological and emulsifying characterization of pectins from Gardenia jasminoides var. fortuniana[D]. Hangzhou:Zhejiang A&F University, 2022.] ZHANG Z. The research of the influence of three extraction methods on the structural, rheological and emulsifying characterization of pectins from Gardenia jasminoides var. fortuniana[D]. Hangzhou: Zhejiang A&F University, 2022.
[27] 孙玮璇, 田金虎, 陈健乐, 等. 提取方法对马铃薯渣果胶多糖组成及分子链构象的影响[J]. 中国食品学报,2021,21(7):216−224. [SUN W X, TIAN J H, CHEN J L, et al. Effects of extraction methods on chemical composition and chain morphology of potato pulp pectic polysaccharide[J]. Journal of Chinese Institute of Food Science and Technology,2021,21(7):216−224.] SUN W X, TIAN J H, CHEN J L, et al. Effects of extraction methods on chemical composition and chain morphology of potato pulp pectic polysaccharide[J]. Journal of Chinese Institute of Food Science and Technology, 2021, 21(7): 216−224.
[28] 支梓鉴, 邹明明, 李珊, 等. 柑橘果肉果胶的流变和结构特性[J]. 高等学校化学学报,2016,37(6):1175−1181. [ZHI Z J, ZHOU M M, LI S, et al. Rheological and structural characterization of pectin polysaccharides from citrus pulp[J]. Chemical Journal of Chinese Universities,2016,37(6):1175−1181.] doi: 10.7503/cjcu20160066 ZHI Z J, ZHOU M M, LI S, et al. Rheological and structural characterization of pectin polysaccharides from citrus pulp[J]. Chemical Journal of Chinese Universities, 2016, 37(6): 1175−1181. doi: 10.7503/cjcu20160066
[29] 郑家琪. 柑橘源RG-Ⅰ型果胶凝胶机理及其应用研究[D]. 杭州:浙江大学, 2021. [ZHENG J Q. Gelling mechanism and application of citrus RG-I pectin[D]. Hangzhou:Zhejiang University, 2021.] ZHENG J Q. Gelling mechanism and application of citrus RG-I pectin[D]. Hangzhou: Zhejiang University, 2021.
[30] MA X M, JING J, WANG J B, et al. Extraction of low methoxyl pectin from fresh sunflower heads by subcritical water extraction[J]. ACS Omega,2020,5(25):15095−15104. doi: 10.1021/acsomega.0c00928
[31] LIANG W, LIAO J, QI J, et al. Physicochemical characteristics and functional properties of high methoxyl pectin with different degree of esterification[J]. Food Chemistry,2022,375:131806. doi: 10.1016/j.foodchem.2021.131806
[32] CERNA M, BARROS A S, NUNES A, et al. Use of FT-IR spectroscopy as a tool for the analysis of polysaccharide food additives[J]. Carbohydrate Polymers,2003,51(4):383−389. doi: 10.1016/S0144-8617(02)00259-X
[33] AL AMOUDI R H, TAYLAN O, KUTLU G, et al. Characterization of chemical, molecular, thermal and rheological properties of medlar pectin extracted at optimum conditions as determined by Box-Behnken and ANFIS models[J]. Food Chemistry,2019,271:650−662. doi: 10.1016/j.foodchem.2018.07.211
[34] IIJIMA M, NALAMURA K, HATAKEYAMA T, et al. Phase transition of pectin with sorbed water[J]. Carbohydrate polymers,2000,41(1):101−106. doi: 10.1016/S0144-8617(99)00116-2
[35] EINHORN STOLL U, KUNZEK H. Thermo analytical characterisation of processing-dependent structural changes and state transitions of citrus pectin[J]. Food Hydrocolloids,2009,23(1):40−52. doi: 10.1016/j.foodhyd.2007.11.009
[36] WANG X, WILSON L, COSGROVE D J. Pectin methylesterase selectively softens the onion epidermal wall yet reduces acid-induced creep[J]. Journal of Experimental Botany,2020,71(9):2629−2640. doi: 10.1093/jxb/eraa059





 下载:
下载:



 下载:
下载:
