Optimization of Extraction Process of Total Triterpenoids from Crataegus songarica by Response Surface Methodology and Its Purification Process
-
摘要: 为了提高准噶尔山楂的高值化利用,以准噶尔山楂为原料,通过单因素实验、正交试验和响应面设计优化复合酶辅助提取准噶尔山楂总三萜的工艺,并对纯化工艺进行优化。结果表明,准噶尔山楂总三萜的最优提取工艺为纤维素酶、果胶酶和木瓜蛋白酶的添加量分别为4%、4%和2%,料液比为1:24 g/mL,温度51 ℃,pH为4.5,酶解76 min,此条件下准噶尔山楂总三萜的提取量为(36.570±0.332)mg/g,通过超声再次提取,总三萜的提取量达到(53.782±0.673)mg/g。纯化工艺为:上样液浓度为6 mg/mL,流速:1 mL/min,上样量:15 mL,洗脱条件为50 mL,70%乙醇,纯化后的准噶尔山楂总三萜的纯度可达29.93%,回收率为81.25%。以上结果说明复合酶法对准噶尔山楂总三萜的提取和采用大孔树脂纯化具有可行性且稳定性高。Abstract: In order to improve the high-value utilization of Crataegus songarica, the single factor experiment, orthogonal experiment and response surface design were used to optimize the extraction process of total triterpenes from Crataegus songarica by compound enzyme assisted extraction, and the purification process was optimized. The results showed that the optimal extraction process of total triterpenes from Crataegus songarica was as follows: The addition amount of cellulase, pectinase and papain was 4%, 4% and 2%, respectively, the ratio of material to liquid was 1:24 g/mL, the temperature was 51 ℃, the pH was 4.5, and the enzymolysis time was 76 min. Under these conditions, the extraction amount of total triterpenes from Crataegus songarica was (36.570±0.332) mg/g, and the extraction amount of total triterpenes was (53.782±0.673) mg/g by ultrasonic extraction again. The purification process was as follows: The concentration of the sample solution was 6 mg/mL, the flow rate was 1 mL/min, the sample volume was 15 mL, the elution condition was 50 mL, and 70% ethanol. The purity of the total triterpenoids was 29.93%, and the recovery rate was 81.25%. The above results indicate that the compound enzymatic method is feasible and stable for the extraction and purification of total triterpenoids from Crataegus songarica by macroporous resin.
-
Keywords:
- Crataegus songarica /
- triterpenes /
- enzyme-assisted extraction /
- macroporous resin /
- purification
-
准噶尔山楂(Crataegus songarica),属蔷薇科山楂属光核组,小乔木或灌木[1],作为天山野果林的主要树种之一,准噶尔山楂具有较高的营养价值和药用价值[2]。其果实中含有多糖、黄酮和三萜等多种成分[3−4],具有抗氧化、保肝和抗衰老等功效[5−7],三萜类化合物在植物中部分以游离的形式存在,多数与糖以苷键或酯键相结合,其基本碳架是由30个碳原子构成[8−9],具有抗氧化[10]、保肝[11−12]、保护肾脏[13]、抗癌[14]、降血脂[15]、降糖[16]、抗炎[17]、抑菌[18]等生物活性,具有极大的药用价值。为了研究准噶尔山楂的药理作用是否与其总三萜的含量相关,首先对其总三萜的提取和纯化工艺进行优化,目前有关总三萜提取的方法主要有回流提取法、酶辅助提取法、超声辅助提取法、微波辅助提取法以及超临界CO2流体萃取法等。相比于其他提取方法,酶辅助提取法条件温和,操作方便且对环境无污染,是利用各种酶来破坏植物细胞壁的结构完整性,从而提高植物中生物活性物质的提取,多种酶协同作用,可以提高提取效率[19−20],超声辅助提取法同样能够破坏细胞壁,使有效成分溶出。大孔树脂具有机械强度高、耐酸碱性能好、使用寿命长等优点,被广泛用于天然产物的分离纯化和富集[21−22]。
目前对准噶尔山楂总三萜的研究存在空缺,无法以现有研究高效利用准噶尔山楂。因此本文采用酶-超声分步提取法提取准噶尔山楂总三萜,运用比色法[23]以准噶尔山楂总三萜提取量为指标,通过单因素实验、正交试验和响应面试验探究准噶尔山楂的提取工艺和大孔树脂纯化工艺,为准噶尔山楂的进一步研究与开发提供数据支持。
1. 材料与方法
1.1 材料与仪器
准噶尔山楂 采于新疆伊犁州伊宁市内,去核,自然晾干至恒重,粉碎后过100目筛,备用;无水乙醇 天津市致远化学试剂有限公司;冰乙酸、乙酸钠 天津市福晨化学试剂厂;高氯酸 桃浦化工厂;香草醛 上海源叶生物科技有限公司,以上试剂均为分析纯;D101型大孔吸附树脂 沧州茂全新材料科技有限公司;木瓜蛋白酶(800 U/mg)、齐墩果酸标准品(≥98%) 上海源叶生物科技有限公司;纤维素酶(>3 U/mg)、中性蛋白酶(≥50 U/mg) 伊势久(江苏连云港)生物科技有限责任公司;果胶酶(500 U/mg) 上海士锋生物科技有限公司。
BSA124S电子天平 德国赛多利斯股份公司;YB-150高速多功能粉碎机 永康市速峰工贸有限公司;HH-S1数显恒温水浴锅 金坛市医疗仪器厂;KM-300DE超声波清洗机 昆山美美超声仪器有限公司;TDZ5-WS多管架自动平衡离心机 长沙湘仪离心机仪器有限公司;WH220-HT磁力搅拌器 德国维根斯公司;Hei-VAP旋转蒸发仪 德国海道夫公司;UV2550紫外-可见分光光度计 日本岛津公司。
1.2 实验方法
1.2.1 单一酶提取单因素实验
准确称取0.5 g准噶尔山楂粉末,选择纤维素酶、果胶酶、木瓜蛋白酶和中性蛋白酶(质量比均为1%,2%,3%,4%,5%),以1:20 g/mL的料液比加入pH5.0的乙酸-乙酸钠缓冲溶液,55 ℃酶解60 min,后沸水浴灭活10 min,离心(4000 r/min,10 min),取上清液定容,计算总三萜提取量。
1.2.2 复合酶正交试验
根据单一酶提取单因素实验结果,选取纤维素酶、果胶酶和木瓜蛋白酶3个因素,每个因素选取3个水平,设计L9(34)正交试验,筛选复合酶的最优配比,正交因素水平如表1所示。
表 1 正交试验因素水平设计Table 1. Orthogonal experimental factor horizontal design水平 A纤维素酶(%) B果胶酶(%) C木瓜蛋白酶(%) 1 2 2 1 2 3 3 2 3 4 4 3 1.2.3 复合酶提取工艺单因素实验
以提取物中总三萜提取量为指标,固定其他实验条件,结合复合酶配比的正交试验结果,分别对料液比、酶解时间、酶解温度、酶解pH等4个因素对总三萜提取量的影响进行考察。
1.2.3.1 料液比对总三萜提取量的影响
称取0.5 g准噶尔山楂粉末,以最优复合酶配比加入复合酶,固定其他单因素条件为:酶解时间60 min,酶解温度为50 ℃,酶解pH5.0,考察料液比为1:10、1:15、1:20、1:25、1:30 g/mL对总三萜提取量的影响。
1.2.3.2 酶解时间对总三萜提取量的影响
称取0.5 g准噶尔山楂粉末,以最优复合酶配比加入复合酶,固定其他单因素条件为:料液比1:20 g/mL,酶解温度为50 ℃,酶解pH5.0,考察酶解时间为30、60、90、120、150 min对总三萜提取量的影响。
1.2.3.3 酶解温度对总三萜提取量的影响
称取0.5 g准噶尔山楂粉末,以最优复合酶配比加入复合酶,固定其他单因素条件为:料液比1:20 g/mL,酶解时间为60 min,酶解pH5.0,考察酶解温度为40、45、50、55、60 ℃对总三萜提取量的影响。
1.2.3.4 酶解pH对总三萜提取量的影响
称取0.5 g准噶尔山楂粉末,以最优复合酶配比加入复合酶,固定其他单因素条件为:料液比1:20 g/mL,酶解时间为60 min,酶解温度为50 ℃,考察酶解pH为4.0、4.5、5.0、5.5、6.0对总三萜提取量的影响。
1.2.4 酶辅助提取准噶尔山楂总三萜的响应面优化设计
在单因素实验结果的基础上,以总三萜提取量为响应值,选择料液比(A)、酶解温度(B)和酶解时间(C)设计三因素三水平的响应面试验,试验因素水平如表2所示。
表 2 响应面试验因素水平Table 2. Factor level of response surface experiment水平 A料液比(g/mL) B酶解温度(min) C酶解时间(℃) −1 1:15 45 30 0 1:20 50 60 1 1:25 55 90 1.2.5 酶-超声分步提取准噶尔山楂总三萜
称取0.3 g准噶尔山楂粉末,在最优酶解提取条件下提取后,滤渣以1:15 g/mL的料液比加入70%的乙醇,在超声功率为120 W,超声温度为50 ℃的条件下提取30 min,抽滤,合并两次提取液,定容,计算总三萜提取量。
1.2.6 总三萜提取量的测定
准确称取5 mg齐墩果酸标准品,70%乙醇溶解后定容至50 mL容量瓶中,摇匀,即得0.1 mg/mL的标准储备液。分别吸取标准储备液0.6、0.8、1.0、1.2、1.4、1.6、1.8 mL置于比色管中,水浴蒸干溶剂,根据前期探究显色条件的实验结果,分别加入0.4 mL显色剂5%香草醛-冰乙酸,1.0 mL稳定剂高氯酸(71%),60 ℃水浴15 min后,立即转移至冰水浴,5 min后取出,加入5 mL冰乙酸,摇匀,在最大吸收波长550 nm处测定吸光度。横坐标为齐墩果酸的质量浓度C,纵坐标为吸光度A,绘制标准曲线,得到线性回归方程A=55.88724C−0.05808,R2=0.9995。公式(1)为准噶尔山楂总三萜提取量的计算公式[24]:
总三萜提取量(mg/g)=C×V×nm (1) 式中:C为总三萜的质量浓度,mg/mL;V为所取提取液体积,mL;n为稀释倍数;m为样品质量,g。
1.2.7 大孔树脂纯化准噶尔山楂总三萜提取物
1.2.7.1 上样液的制备
取准噶尔山楂粉末50 g,以1.2.5的方法提取,合并提取液,减压浓缩至无醇味,备用。
1.2.7.2 大孔树脂预处理
称取适量D101型大孔树脂以95%乙醇浸泡24 h,充分溶胀后过滤,湿法装柱。先用95%的乙醇冲洗至流出液与蒸馏水混合无浑浊后,再用蒸馏水冲洗至流出液无醇味,备用[25]。
1.2.7.3 大孔树脂纯化准噶尔山楂总三萜的工艺优化
上样液浓度的选择:称取相同质量预处理好的D101型大孔树脂5份,湿法装柱,柱体积为20 mL,分别制备浓度为2、4、6、8、10、12 mg/mL的上样液各10 mL,上样速度为1 mL/min吸附后,均用5 BV的水和 95%乙醇分步洗脱,收集洗脱液,计算洗脱液中总三萜浓度,并根据公式(2)计算吸附率,确定上样液浓度。
吸附率(%)=C0−C1C0×100 (2) 式中,C0为起始样品溶液中总三萜浓度,mg/mL;C1为吸附后样品溶液中总三萜浓度,mg/mL。
上样量的选择:称取预处理好的D101型大孔树脂,湿法装柱,上样液以1 mL/min的流速上柱,流出液每5 mL收集1次,测定并计算每份流出液的总三萜浓度,绘制泄露曲线。
洗脱剂浓度的确定:称取5份预处理好的D101型大孔树脂,湿法装柱,取5份15 mL,6 mg/mL准噶尔山楂总三萜提取液,以1 mL/min的流速上柱,吸附完成后用蒸馏水洗至流出液无色,分别用体积分数为10%、20%、50%、70%、90%的乙醇洗脱,每10 mL收集1次洗脱液,计算每份洗脱液以及合并洗脱液中总三萜的浓度,绘制不同乙醇浓度动态解吸曲线,确定洗脱液体积和浓度。
1.2.8 准噶尔山楂总三萜纯度及回收率的计算
在上述筛选的纯化工艺条件下,用D101型大孔树脂纯化准噶尔山楂总三萜粗提物,流出液旋干,取0.01 g总三萜纯化物(m1),以一定量(V1)的纯水溶解,按照1.2.6的方法测定其总三萜浓度(C2),并根据公式(3)和公式(4)计算纯度以及回收率[21]。
纯度(%)=C2×V1m1×100 (3) 回收率(%)=纯化后总三萜的含量纯化前总三萜的含量×100 (4) 1.3 数据处理
每组实验平行做3次,结果取平均值,数据使用Origin 2022软件作图,并使用IBM SPSS Statistics 26和Design-Expert 8.0.6进行数据分析。
2. 结果与分析
2.1 单一酶提取效果
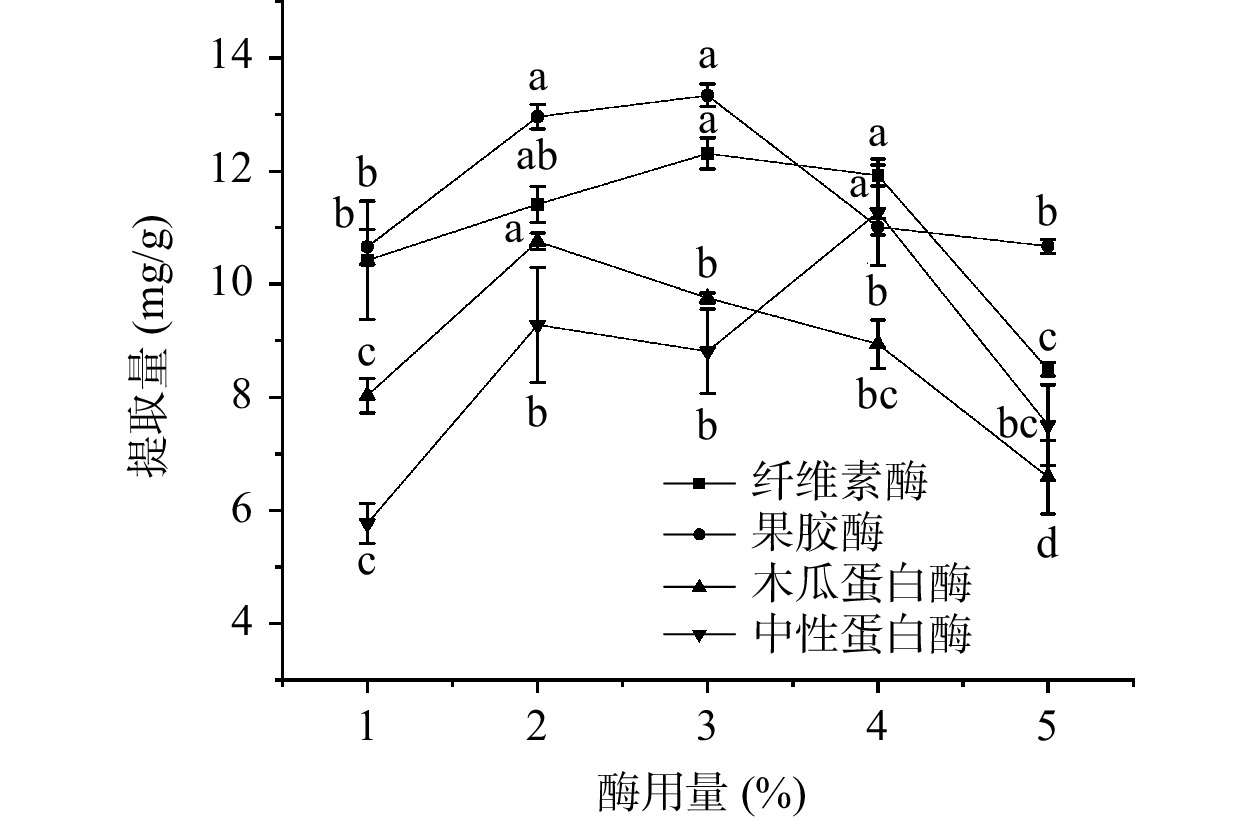
单一酶提取准噶尔山楂总三萜的用量结果如图1所示,由图可知,随着酶用量的增加,4种酶辅助提取效果均呈现先增加后减小的趋势,这可能是由于酶的作用使准噶尔山楂细胞的通透性增强,总三萜更易溶出,从而提高其提取效果,但达到最高点后呈现下降趋势,可能是过量的酶会包裹原料颗粒,不利于三萜的溶出,造成总三萜提取率的下降[26−27]。总体来看,果胶酶对准噶尔山楂总三萜的提取效果最好,木瓜蛋白酶与中性蛋白酶辅助提取的最高提取量相近,但考虑到经济效益,选择木瓜蛋白酶进行后期实验。因此选择纤维素酶(2%、3%、4%),果胶酶(2%、3%、4%),木瓜蛋白酶(1%、2%、3%)进行正交试验确定复合酶辅助提取准噶尔山楂总三萜的酶比例。
2.2 复合酶比例对总三萜提取量的影响
复合酶辅助提取准噶尔山楂总三萜的正交试验结果和方差分析结果见表3和表4,通过极差分析可知,三种酶对准噶尔山楂总三萜提取结果的影响程度的顺序为A>B>C,即纤维素酶>果胶酶>木瓜蛋白酶,且据方差分析可知,纤维素酶对准噶尔山楂总三萜提取效果有显著影响(P<0.05),果胶酶和木瓜蛋白酶无显著影响(P>0.05)。确定复合酶提取准噶尔山楂总三萜的最优比例A3B3C2,即纤维素酶4%,果胶酶4%,木瓜蛋白酶2%,与正交试验结果一致。根据优化条件进行3次平行实验,结果显示准噶尔山楂总三萜的平均提取量为(23.536±0.601)mg/g,说明此方法具有较好的稳定性和可行性。
表 3 复合酶比例正交试验结果Table 3. Orthogonal experimental results of compound enzyme ratio试验号 A纤维素酶 B果胶酶 C木瓜蛋白酶 提取量(mg/g) 1 1 1 1 15.074 2 1 2 2 17.323 3 1 3 3 19.778 4 2 1 2 14.190 5 2 2 3 15.005 6 2 3 1 14.225 7 3 1 3 20.301 8 3 2 1 18.639 9 3 3 2 23.813 K1 52.175 49.565 47.938 K2 43.420 50.967 55.326 K3 62.753 57.816 55.084 k1 17.392 16.522 15.979 k2 14.473 16.989 18.442 k3 20.918 19.272 18.361 R 6.445 2.750 2.463 表 4 方差分析结果Table 4. Results of variance analysis方差来源 偏差平方和 自由度 均方 F 显著性 A纤维素酶 62.479 2 31.239 87.866 * B果胶酶 12.995 2 6.497 18.275 C木瓜蛋白酶 11.745 2 5.873 16.518 误差 0.711 2 0.356 注:*表示该因素对准噶尔山楂总三萜提取效果影响显著(P<0.05)。 2.3 复合酶提取单因素实验
2.3.1 料液比对总三萜提取量的影响
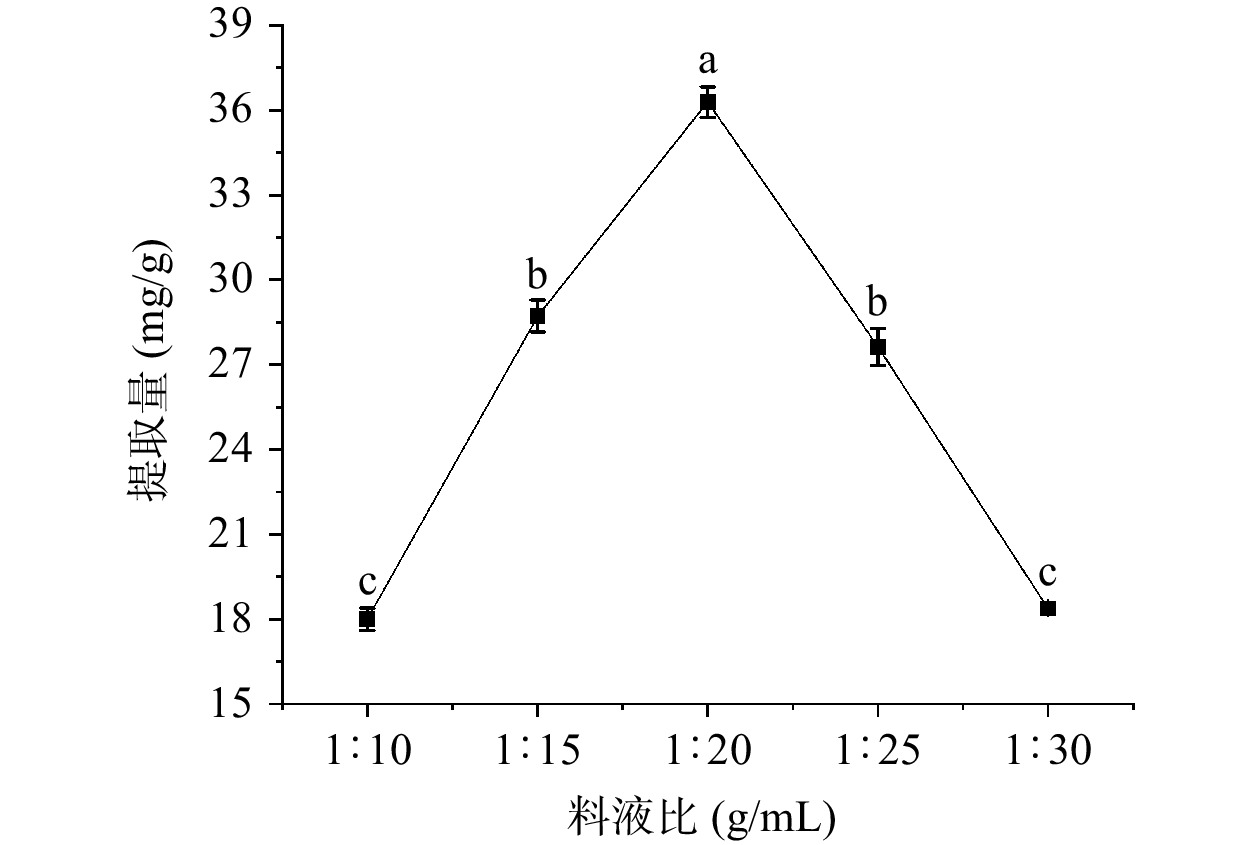
由图2可知,总三萜的提取量在此范围内随料液比的逐渐增大而呈现先增加后降低的趋势,当料液比达到1:20 g/mL时,总三萜提取量显著高于其他(P<0.05),分析原因可能是提取剂的体积增加,使固液之间总三萜的浓度差增大,有利于其传质作用,但是由于样品中总三萜提取量有限,且其他物质也更容易被溶解,并与三萜竞争溶剂,导致料液比继续增加时,总三萜提取量呈现下降趋势[28−29]。因此,选择1:15、1:20、1:25 g/mL的料液比进行下一步响应面优化试验。
2.3.2 酶解时间对总三萜提取量的影响
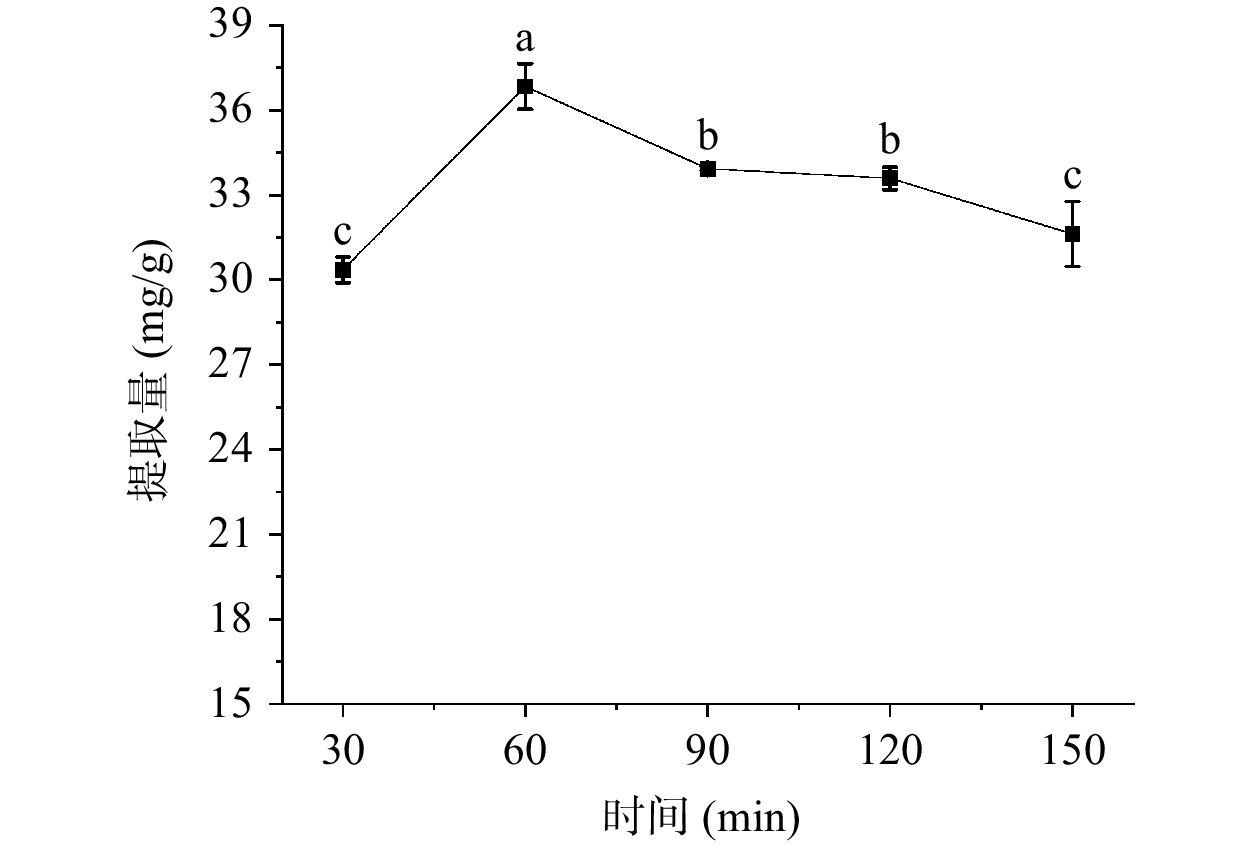
由图3可知,在30~60 min时,准噶尔山楂总三萜的提取量呈现上升趋势,而60 min之后则呈现逐渐下降趋势,酶解时间为60 min时,提取物中总三萜提取量显著高于其他(P<0.05)。这可能是由于酶解时间过短时,细胞壁的结构没有被完全破坏,酶解不充分,时间过长则会使更多其他成分溶解于提取液中,且可能会破坏有效成分的结构,影响总三萜的提取效果[30]。因此,选择酶解时间30、60、90 min进行下一步响应面优化试验。
2.3.3 酶解温度对总三萜提取量的影响
由图4可知,酶解温度对准噶尔山楂总三萜的提取效果影响较大,温度过高或过低都不利于总三萜的提取,当温度达到50 ℃时,提取液中总三萜的提取量最高,当温度持续升高时,总三萜的提取量出现急剧下降,分析原因可能是温度升高有利于提高酶活性和分子扩散速率,从而加快提取速率,但是温度超过50 ℃时,酶活性降低,提取效率下降[31]。因此,选择酶解温度45、50、55 ℃进行下一步响应面优化试验。
2.3.4 酶解pH对总三萜提取量的影响
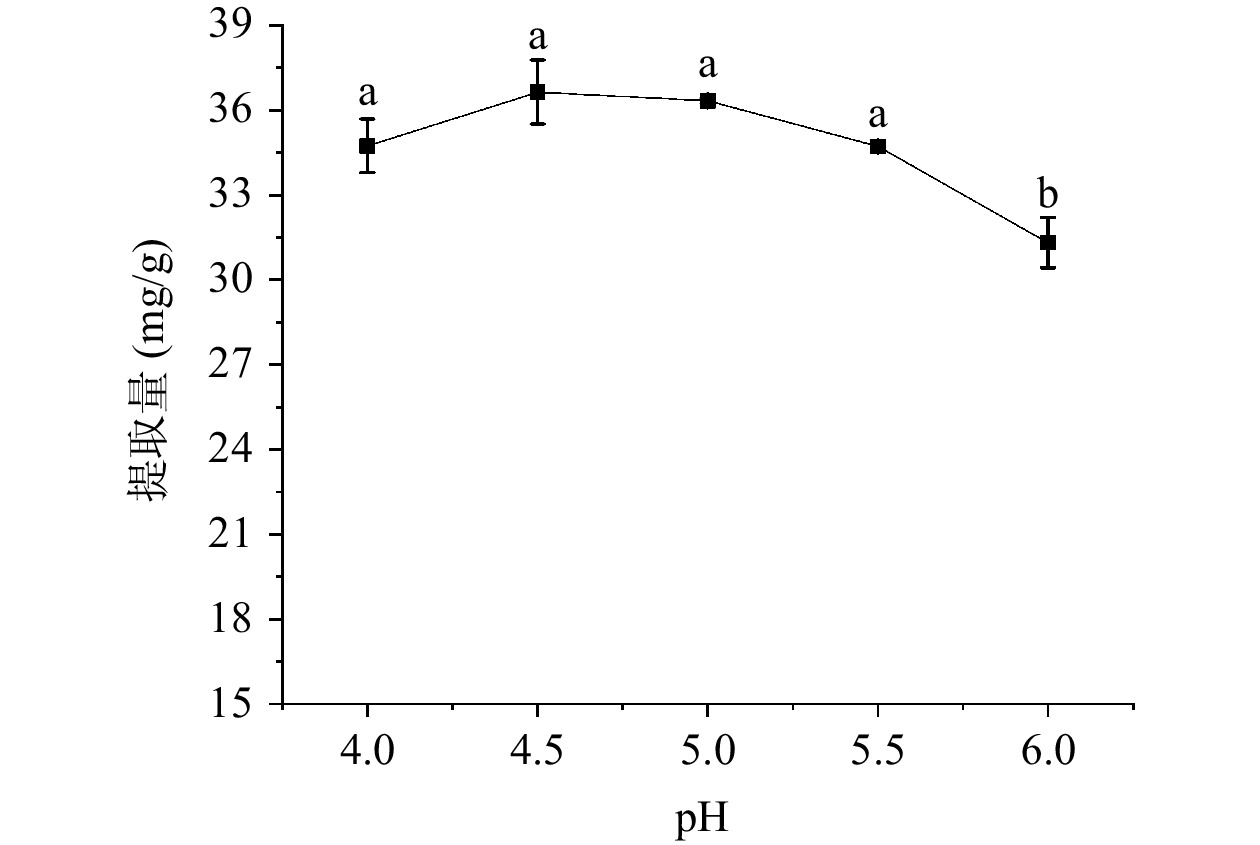
酶都有最适宜的pH,过酸或过碱都有可能造成酶的变性,从而失去活性。由图5可知,准噶尔山楂总三萜的提取量随着酶解pH的增大,总体呈现先增大后减小的趋势,当pH为4.5时,提取液中总三萜的提取量最高,继续增大pH时,提取量反而下降,说明pH4.5为酶解的最适宜pH,在此之外酶活性降低。因此,选择酶解的最适宜pH4.5进行下一步实验。
通过以上单因素实验结果可以看出,料液比、酶解温度和酶解时间的不同均对准噶尔山楂总三萜的提取量有较大影响,而改变酶解pH对准噶尔山楂总三萜提取量的影响不大,因此选择料液比、酶解温度、酶解时间进行响应面优化试验,在试验过程中,酶解pH均为4.5。
2.4 响应面优化酶辅助提取准噶尔山楂总三萜的工艺
2.4.1 响应面试验结果
根据Box-Behnken试验设计原理,优化提取工艺,分析各因素对总三萜提取效果的综合影响,试验结果见表5。
表 5 响应面试验设计方案与结果Table 5. Test design and results of response surface methodology试验号 因素 总三萜提取量
(mg/g)A料液比 B酶解温度 C酶解时间 1 1 0 1 36.785 2 0 −1 1 35.165 3 1 −1 0 35.291 4 −1 −1 0 34.894 5 1 0 −1 35.079 6 −1 1 0 35.654 7 −1 0 1 35.778 8 0 1 −1 35.062 9 0 −1 −1 34.810 10 0 1 1 35.388 11 1 1 0 36.104 12 −1 0 −1 35.864 13 0 0 0 36.896 14 0 0 0 36.446 15 0 0 0 36.749 16 0 0 0 36.780 17 0 0 0 36.713 运用Design-Expert 8.0.6软件对表中数据进行分析和数据拟合,得到二项多次回归方程为:Y=36.72+0.13A+0.26B+0.29C+0.01AB+0.45AC−7.25×10−3BC−0.23A2−1.00B2−0.61C2。为检验方程是否有效,利用软件对其回归模型进行方差分析,结果见表6。由表6可知,回归模型极显著(P<0.01),R2=0.9536,失拟项不显著(P>0.05),说明模型拟合较好,其他因素对实验结果的影响较小,可用于分析响应值,预测实验结果。由表6可知,在一次项中,酶解温度(B)和酶解时间(C)对总三萜提取量的影响差异显著(P<0.05),料液比(A)对总三萜提取量的影响差异不显著(P>0.05),二次项中B2的影响高度显著(P<0.0001),C2影响极显著(P<0.01),交互项中AC影响极显著(P<0.01),AB和BC影响不显著(P>0.05)。比较F值可知,各因素对提取量的影响大小顺序为:酶解时间(C)>酶解温度(B)>料液比(A)。
表 6 回归模型方差分析结果Table 6. Results of variance analysis of regression model方差来源 平方和 自由度 均方 F值 P值 显著性 模型 8.64 9 0.96 15.98 0.0007 ** A料液比 0.14 1 0.14 2.38 0.1668 B酶解温度 0.52 1 0.52 8.73 0.0212 * C酶解时间 0.66 1 0.66 11.02 0.0128 * AB 0.00 1 0.00 0.01 0.9169 AC 0.80 1 0.80 13.37 0.0081 ** BC 0.00 1 0.00 0.00 0.9545 A2 0.22 1 0.22 3.72 0.0950 B2 4.22 1 4.22 70.23 <0.0001 *** C2 1.57 1 1.57 26.09 0.0014 ** 残差 0.42 7 0.06 失拟项 0.31 3 0.10 3.74 0.1176 不显著 纯误差 0.11 4 0.03 总离差 9.06 16 注:***表示P<0.0001,差异高度显著;**表示P<0.01,差异极显著;*表示P<0.05,差异显著。 通过回归方程作响应面图和等高线图(见图6),可以更直观地反映各因素的交互作用对总三萜提取量的影响。响应面图曲线弯曲明显,颜色变化快,等高线呈现椭圆形说明两个因素交互作用大,反之,曲线弯曲程度小,颜色变化不快,等高线呈现圆形,则说明两个因素交互作用对响应值的影响不明显。因此,由图6可知,A(料液比)和C(酶解时间)的交互作用对总三萜提取量的影响最大,A(料液比)和B(酶解温度)交互作用影响其次,B(酶解温度)和C(酶解时间)的交互作用对总三萜提取量的影响最弱。
2.4.2 最优工艺验证实验结果
运用Design-Expert 8.0.6软件分析得出准噶尔山楂总三萜的最优提取工艺为:料液比为1:24.06 g/mL,酶解温度为50.66 ℃,酶解时间为75.99 min,预测在此条件下总三萜的提取量为36.865 mg/g。根据实际操作调节,调整最优条件为:料液比为1:24 g/mL,酶解温度为51 ℃,酶解时间为76 min。通过3次平行实验验证,得到在此条件下总三萜的平均提取量为(36.570±0.332)mg/g,实验结果与预测值相近,说明此方法具有可行性且稳定性高。
2.5 酶-超声分步提取准噶尔山楂总三萜
在最优酶解条件下提取结束后,再进行超声提取,通过3次平行实验,得出酶-超声分步提取准噶尔山楂总三萜的提取量为(53.782±0.673)mg/g。实验结果说明酶解后的滤渣再次进行超声提取能够明显增加总三萜的提取效果,且具有稳定性。
2.6 大孔树脂纯化准噶尔山楂总三萜提取物
2.6.1 大孔树脂纯化工艺
2.6.1.1 上样液浓度的选择
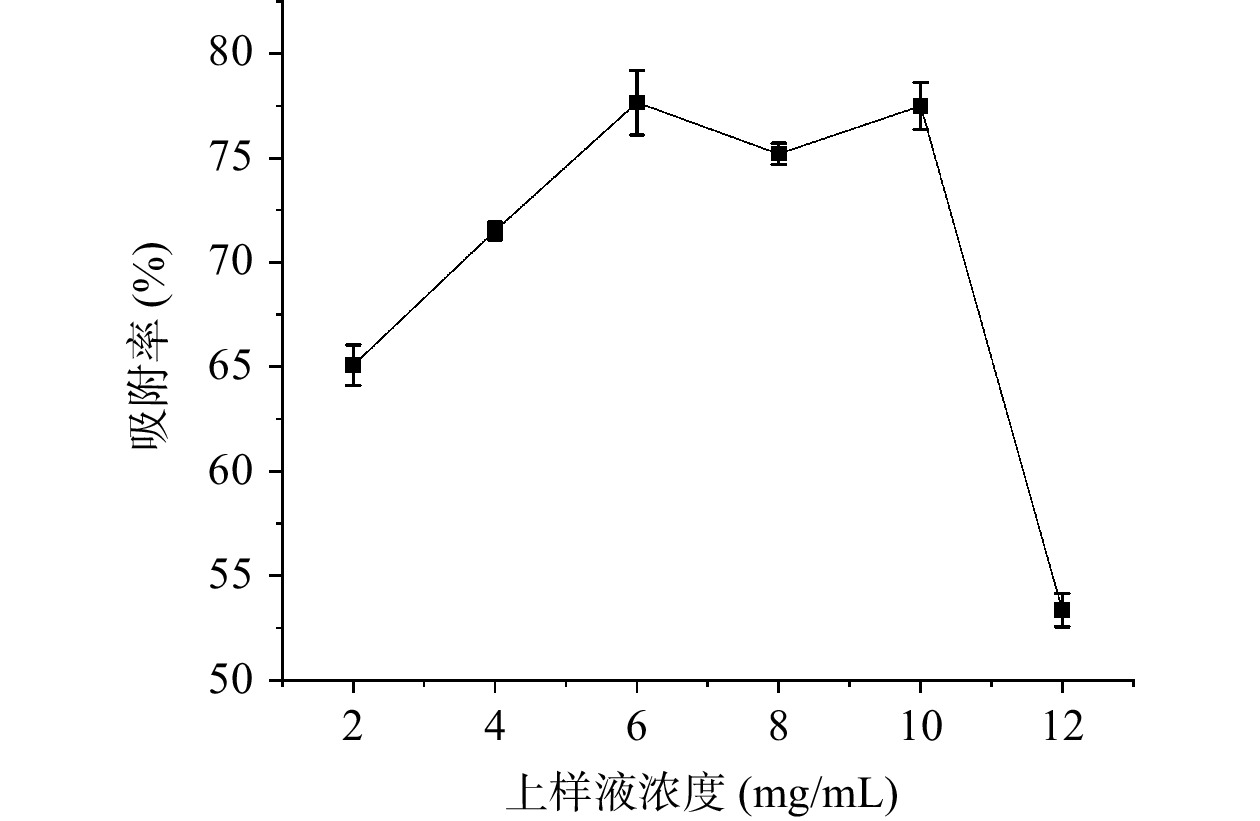
由图7可知,吸附率在2~6 mg/mL的范围内呈逐渐上升趋势,这可能是由于上样液浓度增大后,溶液中三萜与大孔树脂接触的几率也逐渐增大,而随着上样液浓度的进一步增加,样液中其他成分的浓度也会增大,与三萜竞争活性位点,导致吸附率呈下降的趋势[32]。当上样液浓度为6 mg/mL时,大孔树脂吸附率最高,之后开始呈现下降趋势。
2.6.1.2 上样量的选择
由图8可知,随着上样体积的逐渐增加,流出液中的总三萜浓度呈现先平缓后快速上升,最后又平缓上升的趋势。当流出液为15 mL时,流出液中总三萜的浓度上升到上样液总三萜浓度的1/10,达到泄露点[11],随后总三萜开始大量泄露,因此选择15 mL为上样液体积。当流出液体积为60 mL后,流出液总三萜浓度逐渐与上样液总三萜浓度接近,因此上样液体积最大不应超过60 mL。
2.6.1.3 洗脱液的选择
不同乙醇浓度的解吸曲线如图9所示。由图9可知,当乙醇浓度为70%和90%时,均能够迅速将吸附的三萜洗脱下来,在洗脱液通过体积为20 mL时达到高峰,洗脱液体积为50 mL时,被吸附的三萜类化合物基本被洗脱,洗脱曲线出峰快,无明显拖尾现象,而乙醇浓度较低时,三萜难以被洗脱。因此为了节约试剂,并提高纯化效率,选择70%的乙醇进行洗脱,洗脱液体积为50 mL。
2.6.2 大孔树脂纯化准噶尔山楂总三萜提取液的工艺
在以上优化的纯化条件下纯化准噶尔山楂总三萜粗提物,经测定计算得纯化前后总三萜的纯度由2.52%提高至29.93%,回收率为81.25%。实验结果表明D101型大孔树脂能够用于纯化准噶尔山楂总三萜,回收率较高,但纯化效果一般,提取物中仍含有其他成分,说明大孔树脂只能除去一部分杂质,并不能达到精制的目的,若想得到纯度高的总三萜纯化物,还需进行二次纯化。
3. 结论
通过设计正交试验和响应面试验确定准噶尔山楂总三萜的最优提取条件为纤维素酶、果胶酶和木瓜蛋白酶的添加量分别为4%、4%和2%,料液比为1:24 g/mL,温度51 ℃,pH为4.5,酶解76 min,提取量为(36.570±0.332)mg/g,通过超声再次提取后,总三萜提取量达到(53.782±0.673)mg/g, 说明酶-超声分步提取法能够显著提高准噶尔山楂总三萜的提取量。其次,通过D101型大孔树脂确定纯化工艺为:上样液浓度为6 mg/mL,流速:1 mL/min,上样量:15 mL,洗脱条件为50 mL,70%乙醇,纯化后的准噶尔山楂总三萜的纯度可达29.93%,回收率为81.25%,说明大孔树脂可以除去一部分杂质,提高准噶尔山楂总三萜的纯度,但若想得到纯度更高的三萜纯化物,还需进一步纯化精制。以上提取工艺和纯化工艺的建立,均为准噶尔山楂总三萜的成分研究和富集提供了新的实验依据,而且方法条件温和,效率高且稳定性好。实验只针对提取的酶解部分进行了条件优化,对超声部分的提取条件还有待进一步优化,同时还需要对大孔树脂纯化后的纯化物进行进一步精制,并对其纯化前后的生物活性进一步研究。
-
表 1 正交试验因素水平设计
Table 1 Orthogonal experimental factor horizontal design
水平 A纤维素酶(%) B果胶酶(%) C木瓜蛋白酶(%) 1 2 2 1 2 3 3 2 3 4 4 3 表 2 响应面试验因素水平
Table 2 Factor level of response surface experiment
水平 A料液比(g/mL) B酶解温度(min) C酶解时间(℃) −1 1:15 45 30 0 1:20 50 60 1 1:25 55 90 表 3 复合酶比例正交试验结果
Table 3 Orthogonal experimental results of compound enzyme ratio
试验号 A纤维素酶 B果胶酶 C木瓜蛋白酶 提取量(mg/g) 1 1 1 1 15.074 2 1 2 2 17.323 3 1 3 3 19.778 4 2 1 2 14.190 5 2 2 3 15.005 6 2 3 1 14.225 7 3 1 3 20.301 8 3 2 1 18.639 9 3 3 2 23.813 K1 52.175 49.565 47.938 K2 43.420 50.967 55.326 K3 62.753 57.816 55.084 k1 17.392 16.522 15.979 k2 14.473 16.989 18.442 k3 20.918 19.272 18.361 R 6.445 2.750 2.463 表 4 方差分析结果
Table 4 Results of variance analysis
方差来源 偏差平方和 自由度 均方 F 显著性 A纤维素酶 62.479 2 31.239 87.866 * B果胶酶 12.995 2 6.497 18.275 C木瓜蛋白酶 11.745 2 5.873 16.518 误差 0.711 2 0.356 注:*表示该因素对准噶尔山楂总三萜提取效果影响显著(P<0.05)。 表 5 响应面试验设计方案与结果
Table 5 Test design and results of response surface methodology
试验号 因素 总三萜提取量
(mg/g)A料液比 B酶解温度 C酶解时间 1 1 0 1 36.785 2 0 −1 1 35.165 3 1 −1 0 35.291 4 −1 −1 0 34.894 5 1 0 −1 35.079 6 −1 1 0 35.654 7 −1 0 1 35.778 8 0 1 −1 35.062 9 0 −1 −1 34.810 10 0 1 1 35.388 11 1 1 0 36.104 12 −1 0 −1 35.864 13 0 0 0 36.896 14 0 0 0 36.446 15 0 0 0 36.749 16 0 0 0 36.780 17 0 0 0 36.713 表 6 回归模型方差分析结果
Table 6 Results of variance analysis of regression model
方差来源 平方和 自由度 均方 F值 P值 显著性 模型 8.64 9 0.96 15.98 0.0007 ** A料液比 0.14 1 0.14 2.38 0.1668 B酶解温度 0.52 1 0.52 8.73 0.0212 * C酶解时间 0.66 1 0.66 11.02 0.0128 * AB 0.00 1 0.00 0.01 0.9169 AC 0.80 1 0.80 13.37 0.0081 ** BC 0.00 1 0.00 0.00 0.9545 A2 0.22 1 0.22 3.72 0.0950 B2 4.22 1 4.22 70.23 <0.0001 *** C2 1.57 1 1.57 26.09 0.0014 ** 残差 0.42 7 0.06 失拟项 0.31 3 0.10 3.74 0.1176 不显著 纯误差 0.11 4 0.03 总离差 9.06 16 注:***表示P<0.0001,差异高度显著;**表示P<0.01,差异极显著;*表示P<0.05,差异显著。 -
[1] 中国植物志编辑委员会. 中国植物志(第36卷)[M]. 北京:科学出版社, 1986:205. [Delectis Florae Reipublicae Popularis Sinicae Agendae Acadmiae Sinicae Edita. Flora Reipublicae Popularis Sinicae (Tomus 36)[M]. Beijing:Science Press, 1986:205.] Delectis Florae Reipublicae Popularis Sinicae Agendae Acadmiae Sinicae Edita. Flora Reipublicae Popularis Sinicae (Tomus 36)[M]. Beijing: Science Press, 1986: 205.
[2] 杨蕾, 吕海英, 李进, 等. 新疆天山野果林准噶尔山楂种群结构与动态分析[J]. 西北植物学报,2018,38(12):2314−2323. [YANG L, LÜ H Y, LI J, et al. Structure and dynamic analysis of Crataegus songarica K. Koch population in Tianshan wild fruit forest of Xinjiang[J]. Acta Botanica Boreali-Occidentalia Sinica,2018,38(12):2314−2323.] doi: 10.7606/j.issn.1000-4025.2018.12.2314 YANG L, LÜ H Y, LI J, et al. Structure and dynamic analysis of Crataegus songarica K. Koch population in Tianshan wild fruit forest of Xinjiang[J]. Acta Botanica Boreali-Occidentalia Sinica, 2018, 38(12): 2314−2323. doi: 10.7606/j.issn.1000-4025.2018.12.2314
[3] 张玉, 李进, 吕海英, 等. 响应面试验优化新疆野生准噶尔山楂残渣中多糖纯化工艺[J]. 食品科学,2015,36(12):22−28. [ZHANG Y, LI J, LÜ H Y, et al. Optimization of purification process for crude polysaccharides from the pomace of wild Crataegus songorica in Xinjiang by response surface methodology[J]. Food Science,2015,36(12):22−28.] doi: 10.7506/spkx1002-6630-201512005 ZHANG Y, LI J, LÜ H Y, et al. Optimization of purification process for crude polysaccharides from the pomace of wild Crataegus songorica in Xinjiang by response surface methodology[J]. Food Science, 2015, 36(12): 22−28. doi: 10.7506/spkx1002-6630-201512005
[4] 范馨予, 刘慧, 高红艳. 准噶尔山楂果实、叶和核的化学成分分析[J]. 伊犁师范大学学报(自然科学版),2022,16(4):38−45. [FAN X Y, LIU H, GAO H Y. Analysis of chemical constituents in fruit, leaves and seeds of Crataegus songorica K. Koch[J]. Journal of Yili Normal University (Natural Science Edition),2022,16(4):38−45.] doi: 10.3969/j.issn.1673-999X.2022.04.006 FAN X Y, LIU H, GAO H Y. Analysis of chemical constituents in fruit, leaves and seeds of Crataegus songorica K. Koch[J]. Journal of Yili Normal University (Natural Science Edition), 2022, 16(4): 38−45. doi: 10.3969/j.issn.1673-999X.2022.04.006
[5] 任艳利, 张相锋, 赵玉. 超声波提取准噶尔山楂中的熊果酸与抗氧化研究[J]. 安徽农学通报(上半月刊),2012,18(1):46−48. [REN Y L, ZHANG X F, ZHAO Y. The studies on the ultrasonic extraction of ursolic acid from Crataegus songorica K. Koch and anti-oxidation property[J]. Anhui Agricultural Science Bulletin,2012,18(1):46−48.] REN Y L, ZHANG X F, ZHAO Y. The studies on the ultrasonic extraction of ursolic acid from Crataegus songorica K. Koch and anti-oxidation property[J]. Anhui Agricultural Science Bulletin, 2012, 18(1): 46−48.
[6] GANIE A S, DAR A T, ZARGAR B, et al. Antioxidant and hepatoprotective effects of Crataegus songarica methanol extract[J]. Journal of Environmental Pathology, Toxicology and Oncology:Official Organ of the International Society for Environmental Toxicology and Cancer,2014,33(2):131−143.
[7] 马雪, 吕海英, 李进, 等. 准噶尔山楂残渣多糖对D-半乳糖衰老模型小鼠的影响[J]. 食品科学,2018,39(23):155−160. [MA X, LÜ H Y, LI J, et al. Effects of polysaccharides from Crataegus songorica K. Koch fruits on D-galactose-induced aging mice[J]. Food Science,2018,39(23):155−160.] doi: 10.7506/spkx1002-6630-201823024 MA X, LÜ H Y, LI J, et al. Effects of polysaccharides from Crataegus songorica K. Koch fruits on D-galactose-induced aging mice[J]. Food Science, 2018, 39(23): 155−160. doi: 10.7506/spkx1002-6630-201823024
[8] 蔡天娇. 红枣三萜酸提取纯化及其小鼠保肝作用研究[D]. 咸阳:西北农林科技大学, 2017. [CAI T J. Study of purification and hepatoprotective effect in mice of triterpenic acids in jujube[D]. Xianyang:Northwest A&F University, 2017.] CAI T J. Study of purification and hepatoprotective effect in mice of triterpenic acids in jujube[D]. Xianyang: Northwest A&F University, 2017.
[9] 汪弄雪. 华中五味子不同时期藤茎和叶总三萜提取及抗氧化抑菌研究[D]. 西安:陕西师范大学, 2021. [WANG N X. Study on extraction of total triterpenes from stems and leaves of Schisandra sphenanthera Rehd. et Wils. in different periods and its antioxidant and bacteriostasis[D]. Xi’an:Shaanxi Normal University, 2021.] WANG N X. Study on extraction of total triterpenes from stems and leaves of Schisandra sphenanthera Rehd. et Wils. in different periods and its antioxidant and bacteriostasis[D]. Xi’an: Shaanxi Normal University, 2021.
[10] XU H, YUAN Z Z, MA X, et al. Triterpenoids with antioxidant activities from Myricaria squamosa[J]. Journal of Asian Natural Products Research,2018,20(3):292−298. doi: 10.1080/10286020.2017.1321636
[11] 郑义, 李勇, 范晶, 等. 东方栓孔菌三萜的大孔树脂纯化工艺优化及对小鼠酒精性肝损伤的保护作用[J]. 食品工业科技,2019,40(5):264−269. [ZHENG Y, LI Y, FAN J, et al. Optimization of purification by macroporous resin and hepatoprotective effect of triterpenes from Trametes orientalis against alcohol induced liver injury in mice[J]. Science and Technology of Food Industry,2019,40(5):264−269.] ZHENG Y, LI Y, FAN J, et al. Optimization of purification by macroporous resin and hepatoprotective effect of triterpenes from Trametes orientalis against alcohol induced liver injury in mice[J]. Science and Technology of Food Industry, 2019, 40(5): 264−269.
[12] LIU L Y, CHEN H, LIU C, et al. Triterpenoids of Ganoderma theaecolum and their hepatoprotective activities[J]. Fitoterapia,2014,98:254−259. doi: 10.1016/j.fitote.2014.08.004
[13] 饶姣雨, 魏崧丞, 王小康, 等. 番石榴叶总三萜对糖尿病肾病大鼠肾损伤的改善作用及机制研究[J]. 中国临床药理学杂志,2019,35(15):1617−1620. [RAO J Y, WEI S C, WANG X K, et al. Effect and mechanism of total triterpenoids from Psidium guajava leaves on renal injury in rats with diabetic nephropathy[J]. The Chinese Journal of Clinical Pharmacology,2019,35(15):1617−1620.] RAO J Y, WEI S C, WANG X K, et al. Effect and mechanism of total triterpenoids from Psidium guajava leaves on renal injury in rats with diabetic nephropathy[J]. The Chinese Journal of Clinical Pharmacology, 2019, 35(15): 1617−1620.
[14] DONG H J, XUE Z Z, GENG Y L, et al. Lanostane triterpenes isolated from epidermis of Poria cocos[J]. Phytochemistry Letters,2017,22:102−106. doi: 10.1016/j.phytol.2017.09.018
[15] LEE I, SEO J, KIM J, et al. Lanostane triterpenes from the fruiting bodies of Ganoderma lucidum and their inhibitory effects on adipocyte differentiation in 3T3-L1 cells[J]. Journal of Natural Products,2010,73(2):172−176. doi: 10.1021/np900578h
[16] FATMAWATI S, SHIMIZU K, KONDO R. Ganoderol B:A potent α-glucosidase inhibitor isolated from the fruiting body of Ganoderma lucidum[J]. Phytomedicine,2011,18(12):1053−1055. doi: 10.1016/j.phymed.2011.03.011
[17] SOUZA D R M, MASCARENHAS S D B J, REGINA S L S, et al. Antiinflammatory activity of natural triterpenes-An overview from 2006 to 2021[J]. Phytotherapy Research,2022,36(4):1459−1506. doi: 10.1002/ptr.7359
[18] FONTANAY S, GRARE M, MAYER J, et al. Ursolic, oleanolic and betulinic acids:Antibacterial spectra and selectivity indexes[J]. Journal of Ethnopharmacology,2008,120(2):272−276. doi: 10.1016/j.jep.2008.09.001
[19] PURI M, SHARMA D, BARROW J C. Enzyme-assisted extraction of bioactives from plants[J]. Trends in Biotechnology,2011,30(1):37−44.
[20] NADAR S S, RAO P, RATHOD K V. Enzyme assisted extraction of biomolecules as an approach to novel extraction technology:A review[J]. Food Research International,2018,108:309−330. doi: 10.1016/j.foodres.2018.03.006
[21] 王小明, 陈碧, 张鹏, 等. 甜茶叶中总黄酮大孔树脂纯化工艺及抗氧化活性研究[J]. 食品工业科技,2019,40(24):28−33,39. [WANG X M, CHEN B, ZHANG P, et al. Purification process of total flavonoid in sweet tea by using the macroporous resin and its antioxidant activity[J]. Science and Technology of Food Industry,2019,40(24):28−33,39.] WANG X M, CHEN B, ZHANG P, et al. Purification process of total flavonoid in sweet tea by using the macroporous resin and its antioxidant activity[J]. Science and Technology of Food Industry, 2019, 40(24): 28−33,39.
[22] ZHOU P, FANGMA Y, JIN W, et al. Response surface optimization of the water immersion extraction and macroporous resin purification processes of anhydrosafflor yellow B from Carthamus tinctorius L.[J]. Journal of Food Science,2020,85(10):3191−3201. doi: 10.1111/1750-3841.15374
[23] 陈维冉, 王双, 蔡梅超, 等. 分光光度法测定不同产地苦楝子总三萜的含量[J]. 山东化工,2020,49(22):74−75. [CHEN W R, WANG S, CAI M C, et al. Determination of total triterpenoids in melia azedarach from different areas by spectrophotometry[J]. Shandong Chemical Industry,2020,49(22):74−75.] doi: 10.3969/j.issn.1008-021X.2020.22.028 CHEN W R, WANG S, CAI M C, et al. Determination of total triterpenoids in melia azedarach from different areas by spectrophotometry[J]. Shandong Chemical Industry, 2020, 49(22): 74−75. doi: 10.3969/j.issn.1008-021X.2020.22.028
[24] 付亚玲. 黑枣三萜酸的提取、分离纯化及抗氧化活性研究[D]. 泰安:山东农业大学, 2021. [FU Y L. Extraction, purification and antioxidant activity of triterpenic acids from blackened jujube (Zizyphus jujuba Mill.)[D]. Tai’an:Shandong Agricultural University, 2021.] FU Y L. Extraction, purification and antioxidant activity of triterpenic acids from blackened jujube (Zizyphus jujuba Mill.)[D]. Tai’an: Shandong Agricultural University, 2021.
[25] 祝朋玲, 张静, 李思雨, 等. 大孔树脂纯化灵芝子实体和孢子粉中总三萜[J]. 食品研究与开发,2023,44(4):79−85. [ZHU P L, ZHANG J, LI S Y, et al. Purification of total triterpenoids from fruiting body and spore powder of Ganoderma lucidum by macroporous adsorption resins[J]. Food Research and Development,2023,44(4):79−85.] doi: 10.12161/j.issn.1005-6521.2023.04.012 ZHU P L, ZHANG J, LI S Y, et al. Purification of total triterpenoids from fruiting body and spore powder of Ganoderma lucidum by macroporous adsorption resins[J]. Food Research and Development, 2023, 44(4): 79−85. doi: 10.12161/j.issn.1005-6521.2023.04.012
[26] 陈安徽, 巫永华, 刘恩岐, 等. 山楂叶多酚的酶法提取及抗氧化活性研究[J]. 食品科技,2017,42(2):203−208. [CHEN A H, WU Y H, LIU E Q, et al. Enzymatic extraction and antioxidant activity of polyphenols from hawthorn leaves[J]. Food Science and Technology,2017,42(2):203−208.] CHEN A H, WU Y H, LIU E Q, et al. Enzymatic extraction and antioxidant activity of polyphenols from hawthorn leaves[J]. Food Science and Technology, 2017, 42(2): 203−208.
[27] 张峰. 樟树枝叶制取精油的剩余物中活性成分及其生物活性研究[D]. 北京:中国林业科学研究院, 2018. [ZHANG F. Study on active components and biological activities from residues of leaves and twigs of camphor tree after distillation[D]. Beijing:Chinese Academy of Forestry, 2018.] ZHANG F. Study on active components and biological activities from residues of leaves and twigs of camphor tree after distillation[D]. Beijing: Chinese Academy of Forestry, 2018.
[28] 叶琴, 杨洋, 袁经权. 正交试验设计法优化超声复合酶提取甜茶苷工艺[J]. 食品工业科技,2017,38(20):216−220,239. [YE Q, YANG Y, YUAN J Q. Optimization of ultrasonic-composite enzyme extraction of rubusoside from Rubus suabissimus by orthogonal design[J]. Science and Technology of Food Industry,2017,38(20):216−220,239.] YE Q, YANG Y, YUAN J Q. Optimization of ultrasonic-composite enzyme extraction of rubusoside from Rubus suabissimus by orthogonal design[J]. Science and Technology of Food Industry, 2017, 38(20): 216−220,239.
[29] 蒋德旗, 陈晓白, 农贵珍, 等. 鸡骨草多糖的酶法提取工艺优化及其抗氧化活性[J]. 食品工业科技,2019,40(3):153−158. [JIANG D Q, CHEN X B, NONG G Z, et al. Optimization of enzymatic extraction of polysaccharide from Abrus cantoniensis Hance and its antioxidant activity[J]. Science and Technology of Food Industry,2019,40(3):153−158.] JIANG D Q, CHEN X B, NONG G Z, et al. Optimization of enzymatic extraction of polysaccharide from Abrus cantoniensis Hance and its antioxidant activity[J]. Science and Technology of Food Industry, 2019, 40(3): 153−158.
[30] 李开泉, 陶华蕾. 酶法辅助提取迷迭香中三萜酸的工艺研究[J]. 江西农业大学学报,2012,34(5):1049−1052,1057. [LI K Q, TAO H L. Study on extraction process of triterpene acids form rosemary[J]. Acta Agriculturae Universitatis Jiangxiensis,2012,34(5):1049−1052,1057.] doi: 10.3969/j.issn.1000-2286.2012.05.035 LI K Q, TAO H L. Study on extraction process of triterpene acids form rosemary[J]. Acta Agriculturae Universitatis Jiangxiensis, 2012, 34(5): 1049−1052,1057. doi: 10.3969/j.issn.1000-2286.2012.05.035
[31] 丁霄霄, 李凤伟, 余晓红. 响应面法优化复合酶提取灵芝总三萜工艺[J]. 食品工业,2018,39(8):40−44. [DING X X, LI F W, YU X H. Optimization of complex enzyme extraction technology of total triterpenoids from Ganoderma lucidum by response surface methodology[J]. The Food Industry,2018,39(8):40−44.] DING X X, LI F W, YU X H. Optimization of complex enzyme extraction technology of total triterpenoids from Ganoderma lucidum by response surface methodology[J]. The Food Industry, 2018, 39(8): 40−44.
[32] SUN L, GUO Y, FU C, et al. Simultaneous separation and purification of total polyphenols, chlorogenic acid and phlorizin from thinned young apples[J]. Food Chemistry,2013,136(2):1022−1029. doi: 10.1016/j.foodchem.2012.09.036





 下载:
下载:




 下载:
下载:
