Screening, Identification and Enzymatic Properties Study of Cold-adapted Marine Pectinase-Producing Bacteria
-
摘要: 目的:从海洋底泥样品中筛选能低温降解果胶的新颖菌株,发掘具有潜在产业化价值的果胶酶。方法:以果胶为唯一碳源,利用透明圈法和3,5-二硝基水杨酸法(DNS法)从大连渤海湾海泥中筛出一株高产果胶酶菌株。对其进行形态学、生理生化特征分析以及16S rDNA序列测定,BLAST同源基因比对后构建系统发育树,并进一步研究其酶学特性。结果:筛选高产果胶酶菌株命名为LY-1,通过16S rDNA序列分析并结合生理生化鉴定确定该菌株为橄榄灰链霉菌(Streptomyces olivogriseus)。菌株LY-1在25 ℃、180 r/min的条件下培养至24 h时,果胶酶的酶活力为30.56 U/mL。最适酶pH为8.0,最适酶温度为20 ℃。此外,该酶在60 ℃孵育2 h仍保持70%以上的酶活性,在pH7.0~9.0范围内稳定性良好,酶活性稳定维持在90%以上。金属离子Cu2+、Ba2+、Mg2+、Ca2+、K+、Co2+促进该酶活性,Mn2+、Zn2+、Hg2+、Na+则抑制该酶活性。结论:菌株LY-1所产的果胶酶具有应用于产业化商用果胶酶的潜力。Abstract: Objective: To select novel strains that could degrade pectin at low temperature from marine sediment samples and discover pectinase with potential industrial value. Methods: Take pectin as the only carbon source, screening a high-yielding pectinase strain from sea mud in Bohai Bay, Dalian with the transparent circle method and the 3,5-dinitrosalicylic acid method (DNS method). It analyzed the morphological, physiological and biochemical characteristics, and determined the 16S rDNA sequence. After comparing BLAST homologous gene, it built up a phylogenetic tree, and further studied the enzymatic properties. Results: It screened the strain with high pectinase yield which was named LY-1. Then it analyzed the 16S rDNA sequence and determined that this strain was Streptomyces olivogriseus from the physiological and biochemical index. When strain LY-1 was cultured at 25 ℃ and 180 r/min for 24 hours, the enzyme activity of pectinase was 30.56 U/mL. It showed that the optimal enzyme pH was 8.0, and the optimal enzyme temperature was 20 ℃. Furthermore, the enzymatic activity could still be maintained more than 70% when it was incubated at 60 ℃ for 2 hours, and remained stable in the pH range of 7.0~9.0 with enzyme activity at over 90%. The metal ions Cu2+, Ba2+, Mg2+, Ca2+, K+, and Co2+ could promote the activity of this enzyme, while Mn2+, Zn2+, Hg2+, and Na+ would inhibit its activity. Conclusion: The pectinase produced by strain LY-1 would have the potential to be applied to industrial commercial pectinase.
-
Keywords:
- pectinase /
- screening /
- identification /
- enzymatic properties
-
果胶是一种广泛存在于植物细胞壁中的复杂多糖,主链是通过α-1,4-糖苷键聚合而成的D-吡喃半乳糖醛酸,侧链则由各种多糖组成,如L-阿拉伯糖、L-鼠李糖、D-半乳糖等[1]。果胶酶(pectinase)是指能降解果胶物质的多酶复合体系,能够降解果胶的多种结构[2]。根据果胶酶对果胶物质中半乳糖醛酸骨架的作用模式,可将该酶分为聚半乳糖醛酸酶(polygalacturonase,PG)、果胶裂解酶(pectate lyase,PL)与果胶甲酯酶(pectin methyl esterase,PE)三大类[2],不同的果胶酶切割果胶中不同类型的α-1,4-糖苷键[3−4]。根据最适酶活性pH又可将其分为碱性和酸性两大类[5−7]。碱性果胶酶主要应用于食品生产过程中,帮助分解果胶,改善产品的质地和口感[8],对于胃肠道疾病患者来说,果胶的有效降解可以减轻胃肠道的负担,改善消化吸收。此外,果胶酶还可以用于治疗炎症和肿瘤等疾病,其降解果胶的能力可以帮助减轻炎症反应、促进肿瘤细胞的死亡[9−10];在酒类酿造过程中分解果胶,促进酒液的澄清和过滤;预处理食品加工业中含果胶的废水[11],酸性果胶酶则主要用于提取和澄清果蔬汁和果酒,降低产品的浑浊度和黏度、选择性水解组织中间薄片的多糖来保持植物细胞的完整性从而提高单细胞产品质量,单细胞产品可用作婴儿制品、乳制品的成分[12]。
在果胶酶的天然来源中,微生物因其具有广泛的适应性、多样的代谢途径、高效的酶系统以及生长周期短、培养条件易控制、分布广等优势而成为了果胶酶的主要来源[13]。其中真菌、细菌、放线菌和酵母菌等都能产生果胶酶[14−15],尤其以曲霉属最为常见[16−17]。目前,全球果胶酶市场正处于快速增长阶段,几乎占据全球酶市场的25%[18]。这主要得益于果制品行业的发展,以及人们对优质健康食品的需求增加。然而,相比于国外,我国对果胶酶的研究起步较晚[19−20],无论是在研究水平、领域、手段方面还是开发应用方面与国外都存有一定差距[19−21]。尤其是缺乏产高活性酶的菌种,目前能应用于工业中的果胶酶多来源于真菌[22],其大多存在产酶活性较低、能耗过高等问题,因而无法满足工业生产上的需求,导致效价高的商品果胶酶产量仍很低。因此,找到一种新型优质菌种来制备果胶酶是非常有必要的,海洋环境具有高盐、高压、低温、低光照、寡营养等特点,能很大程度上赋予微生物果胶酶新的代谢机制与基因特性,有利于优势菌株的筛选。
本研究从海洋底泥样品中筛选到一株高产低温碱性果胶酶的放线菌,通过形态学、生理生化及16S rDNA序列测定并构建系统发育树分析确定该菌菌属,并研究了其相关酶学性质,旨在发现新的优质低温酶源微生物资源,推动相关行业发展,同时该研究为后续提取果胶酶基因进行克隆表达和高效、低能耗大批量生产果胶酶提供了前期基础。
1. 材料与方法
1.1 材料与仪器
海泥样品 中国辽宁省大连市渤海海域(121°78'85.74'' E,39°01'79.06'' N)60~100 m深度处海底泥;果胶 上海麦克林生化科技有限公司;其他试剂均为国产分析纯。
Bioscreen C自动微生物鉴定分析仪 Biolog公司;CI-L型显微镜 尼康仪器(上海)有限公司;BPC-150F型培养箱 上海茸研仪器有限公司;Multiskan 1510酶标仪 芬兰Labsystems公司;D-37520低温冷冻离心机 Thermo公司;CRY-2112恒温摇床 上海茸研仪器有限公司;DK-S600电动恒温水浴锅 上海景洪实验设备有限公司。
1.2 实验方法
1.2.1 培养基的制备
初筛培养基[21,23](g/L):果胶30.0,NaNO3 3.0,K2HPO4·3H2O 3.3,KCl 0.5,Fe2(SO4)3 0.01,(NH4)2SO4 20,MgSO4 0.24,CaCl2 0.15,KH2PO4 3.8,溴酚蓝 0.2,琼脂粉20.0,pH自然。
基础培养基(g/L):酵母浸膏粉5.0,蛋白胨8.0,氯化钠10.0,pH7.0。
发酵培养基[24](g/L):果胶2.0,K2HPO4 0.01,MgSO4 0.05,FeSO4 0.001,(NH4)2SO4 2.0,pH自然。
1.2.2 菌株分离纯化与初筛
称取海泥10.0 g,置于装有若干玻璃珠和90 mL无菌水的250 mL锥形瓶中,放于恒温摇床,30 ℃、160 r/min、2 h充分打散。再从上述锥形瓶取1 mL加入到99 mL基础培养基中,25 ℃、180 r/min富集培养24 h。用0.85%(m/V)无菌生理盐水对菌悬液进行10倍梯度稀释,将梯度为10−1~10−7的样品稀释液各取200 μL涂布到初筛培养基上(每个梯度做3组平行实验),25 ℃倒置培养48 h。待长出菌落后,及时挑取长势良好、外观不同的单菌落进行分离纯化,后将纯化过的菌株点种在初筛培养基上(每株菌做三组平行实验),25 ℃倒置培养48 h。使用游标卡尺准确测量培养基上的黄色水解圈直径(Dp)和菌落直径(Dc)[21],挑选出Dp/Dc值较大的6株菌株作为复筛的目标菌株[22]。
1.2.3 产果胶酶菌株的复筛
挑取初筛得到6株单菌落分别接种于基础培养基中,25 ℃、180 r/min培养24 h。以接种量为2%(v/v)将活化24 h的培养物接种到发酵培养基(100/250 mL)中,25 ℃、180 r/min发酵72 h。发酵液4 ℃、8000 r/min离心20 min后,取等量上清液适当稀释作稀释粗酶液,使用3,5-二硝基水杨酸法(DNS法)[25]制作葡萄糖标准曲线并测定酶活进行复筛,底物为0.5%的果胶液。酶活力单位定义(U):在25 ℃,pH为7.0的反应条件下,每分钟释放1 μmol还原糖(以葡萄糖计)所需的酶量。发酵液酶活力单位定义为每毫升发酵液含酶活单位(U/mL)。选取酶活最高的菌株,用甘油管保存于−80 ℃冰箱。
1.2.4 菌株生长曲线及产果胶酶活性曲线测定
粗酶液的制备:取复筛选出的菌株接种于基础培养基25 ℃、180 r/min培养24 h。以接种量为2%(v/v)将活化24 h的培养液接种到发酵培养基(100/250 mL)中,25 ℃、180 r/min培养72 h。将发酵液4 ℃、8000 r/min离心20 min后取上清液适当稀释即为粗酶液。
挑取上述酶活最高菌株的单菌落于基础培养基(100/250 mL)中在25 ℃、180 r/min培养条件下培养,以未接种单菌落的基础培养基为空白对照,当培养液的OD600值达到0.5时,以接种量为1%(v/v)接种于发酵培养基中培养。使用自动微生物鉴定分析仪(每孔250 μL,25 ℃)进行振荡培养,每隔8 h检测一次OD600,连续检测4 d,得到连续时间节点处的OD600值并绘制生长曲线[26]。
在每次检测OD600的同时,吸取1.7 mL质量分数为0.5%的果胶底物溶液于具塞比色管中,加入0.3 mL稀释酶液,25 ℃水浴准确反应30 min后取出,加入3 mL DNS试剂,充分混匀后立即用沸水浴30 min灭活,然后定容至25 mL;以高温煮沸灭活10 min后的酶稀释液作为空白对照[27−28],各取200 μL于96孔板中,用酶标仪在540 nm处测OD值,实验组与空白对照组各做3次平行实验取平均值,两者的差值即为还原糖的产生量,后根据OD540差值计算酶活大小并绘制产酶活性曲线。
1.2.5 菌株的形态鉴定
将复筛所得的最高酶活的菌株进行平板划线分离纯化,25 ℃培养24 h后观察菌株生长状况、菌落形态以及革兰氏染色镜下结果。
1.2.6 菌株的生理生化鉴定
利用Biolog自动鉴定仪检测该菌株对碳源的利用率。参照文献[15]所用方法。
1.2.7 菌株的16S rDNA序列测定及同源性分析
将保存的菌株平板送往大连宝生物公司并对菌株进行16S rDNA分析鉴定:采用PCR扩增目的片段,记录扩增序列结果并进行电泳检测,采用数据库同源对比法,利用BLAST(http://www.ncbi.nlm.nih.gov/BLAST),将目的菌株LY-1的16S rDNA序列与Gen-Bank/DDBJ/EMBL数据库中菌的16S rDNA序列进行比较鉴定,找出与目的菌株基因序列同源性较高的已知分类地位的菌种。采用Mega X构建系统发育树[29]。结合上述Biolog自动微生物鉴定分析系统结果,进行分析,得到准确鉴定结果。
1.2.8 酶学特性研究
1.2.8.1 最适温度和热稳定性分析
在pH为7的条件下,将待测果胶酶液样品分别在5~80 ℃的水浴环境下与果胶底物进行酶反应30 min,以DNS法测定果胶酶酶活力,以最高酶活为100%计,绘制果胶酶最适反应温度的相对酶活曲线,得到最适反应温度。将果胶酶液样品分别置于5、10、15、20、25、30、35、40、45、50、55、60、65、70、80 ℃下保温处理2 h,后置于最适温度的条件下进行酶解反应30 min,测定酶活力。以最大酶活值定义为100%,绘制果胶酶热稳定性的相对酶活曲线,每个温度检测3组平行。
1.2.8.2 最适pH和pH稳定性分析
分别配制不同pH3.0~12.0的缓冲溶液,pH3.0~5.0的Phosphate citrate缓冲液、pH6.0~10.0的Tris-HCl缓冲液、pH为11.0~12.0的Na2HPO4-NaOH缓冲溶液。用不同pH的缓冲溶液稀释粗酶液并配制相应pH的果胶底物,用DNS法在20 ℃条件下测不同pH的果胶酶酶活力,将最大酶活值定义为100%,计算相对酶活力,绘制果胶酶最适反应pH的相对酶活曲线,得到酶的最适pH。将待测果胶酶液样品在不同pH缓冲液中放置2 h,再将其置于最适pH条件下酶解反应30 min,以最大活力为100%计,绘制果胶酶pH稳定性的相对酶活曲线。每个pH检测3组平行。
1.2.8.3 两种浓度下的不同金属离子对酶活的影响
在温度20 ℃、pH为8的情况下,在酶活测定反应体系中分别加入终浓度为1和5 mmol/L且含有Co2+、Na+、Mn2+、Zn2+、Ba2+、Hg2+、Cu2+、K+、Mg2+、Ca2+的金属离子试剂,在对照组中添加相应体积的缓冲液PB,并在测量酶活性后计算其相对活性。每种金属离子检测3组平行。
1.3 数据处理
所有实验均为三组平行。使用 GraphPad Prism 9.5.1软件对筛菌结果、菌株生长量以及酶活性高低等数据进行处理与统计学分析。
2. 结果与分析
2.1 产酶菌株初筛结果
如表1所示,计算出培养基中菌株的Dp/Dc值,并挑选出Dp/Dc值较大的6株作为目标复筛菌株并继续培养。其编号分别为LY-1,LY-6,LY-7,LY-9,LY-11,LY-16。其中LY-11的Dp/Dc值最大为5.28±0.35,LY-7的Dp/Dc最小为3.15±0.35。
表 1 产果胶酶菌株初筛结果Table 1. Results of the initial screening of pectinase-producing strains菌株编号 水解圈直径Dp(mm) 菌落直径Dc(mm) Dp/Dc LY-1 10.30±0.56 2.20±0.20 4.72±0.67 LY-6 6.76±0.35 1.73±0.25 3.94±0.51 LY-7 9.76±0.61 3.13±0.55 3.15±0.35 LY-9 11.86±0.45 3.00±0.36 4.00±0.60 LY-11 12.67±0.45 2.40±0.10 5.28±0.35 LY-16 9.03±0.42 1.83±0.21 4.99±0.38 2.2 产酶菌株复筛结果
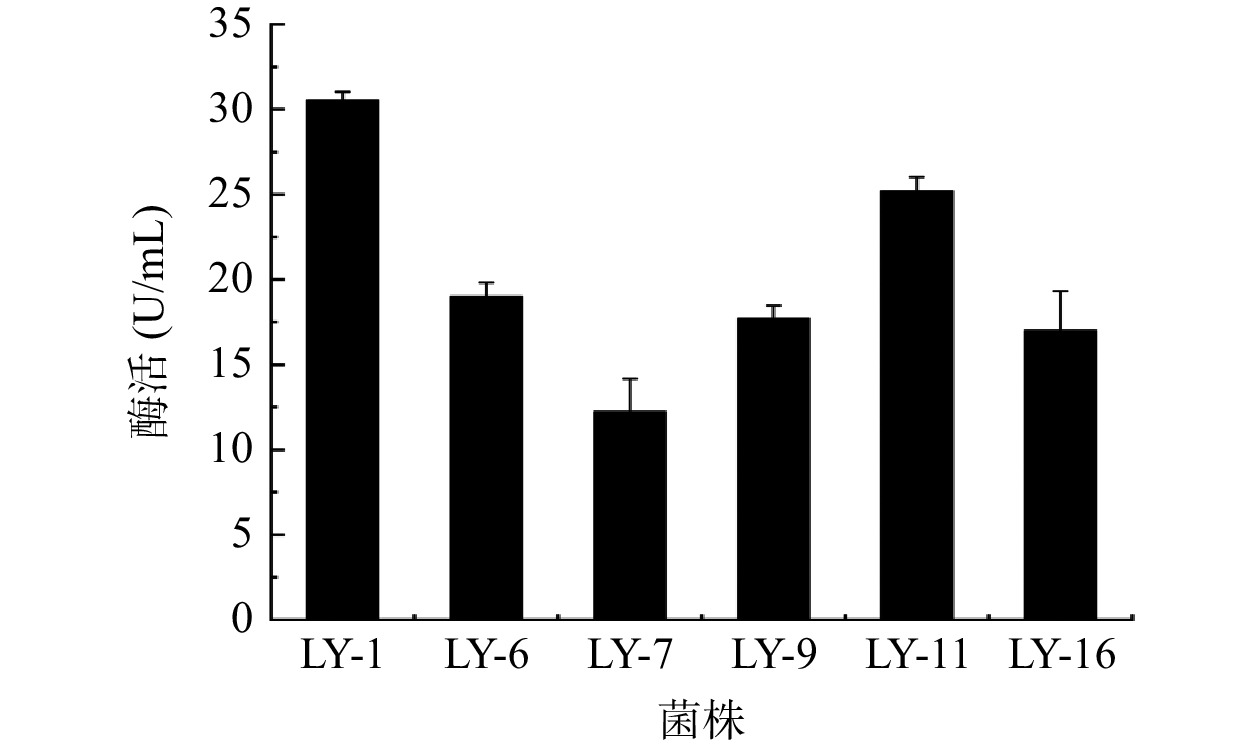
根据DNS法制作葡萄糖标准曲线,线性回归方程为y=0.9614x+0.0276(R²=0.9880),表明线性拟合良好可用于果胶酶活力的计算。挑取上述初筛得到的Dp/Dc值较大的菌株LY-1,LY-6,LY-7,LY-9,LY-11,LY-16进行平板划线得到单菌落后接种于发酵培养基,用DNS法对其粗酶液进行酶活检测,每株菌进行三次平行实验。因为酶活力和测定的吸光度值呈正比例线性关系,故用吸光度值的大小来代表其粗酶液的酶活力的大小酶活检测,结果如图1所示,其中编号为LY-1的菌株酶活力(30.56 U/mL)显著高于其他5个菌株(P<0.05)。
2.3 菌株生长曲线及产酶活性曲线
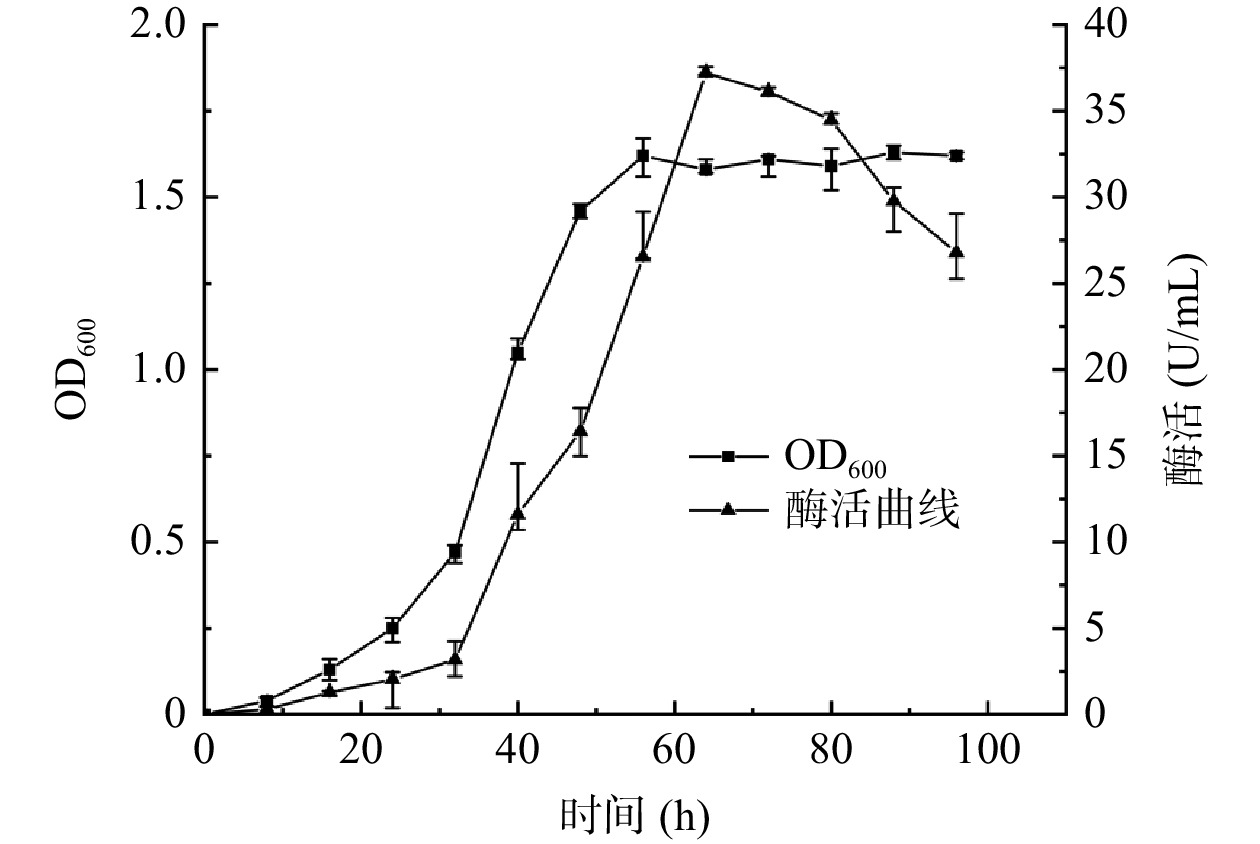
复筛选出的Dp/Dc值最大且酶活性最高的菌株LY-1为目的菌株,对该菌株进行生长曲线的测定并用其制取的酶液进行酶活性测定,结果如图2,菌株LY-1接种发酵24 h内为迟缓期。接种后24~56 h达到对数增长期,生长曲线上的活菌数呈线性增加,而酶活相对于生长曲线表现出了一定的滞后性,在32~64 h内呈线性增长趋势,此时的菌株的形态、染色、生物活性都很典型,对外界环境因素的作用敏感,因此研究菌株的性状以此时期为最好[30]。56 h后进入平稳期,菌群的生长总数处于较平坦的阶段,酶活也在此段时间内达到最高值。接种72 h后为衰落期,酶活性也开始同步减小,故确定接种后培养64 h为最佳培养时间。
2.4 菌株的形态与鉴定
2.4.1 菌株的形态
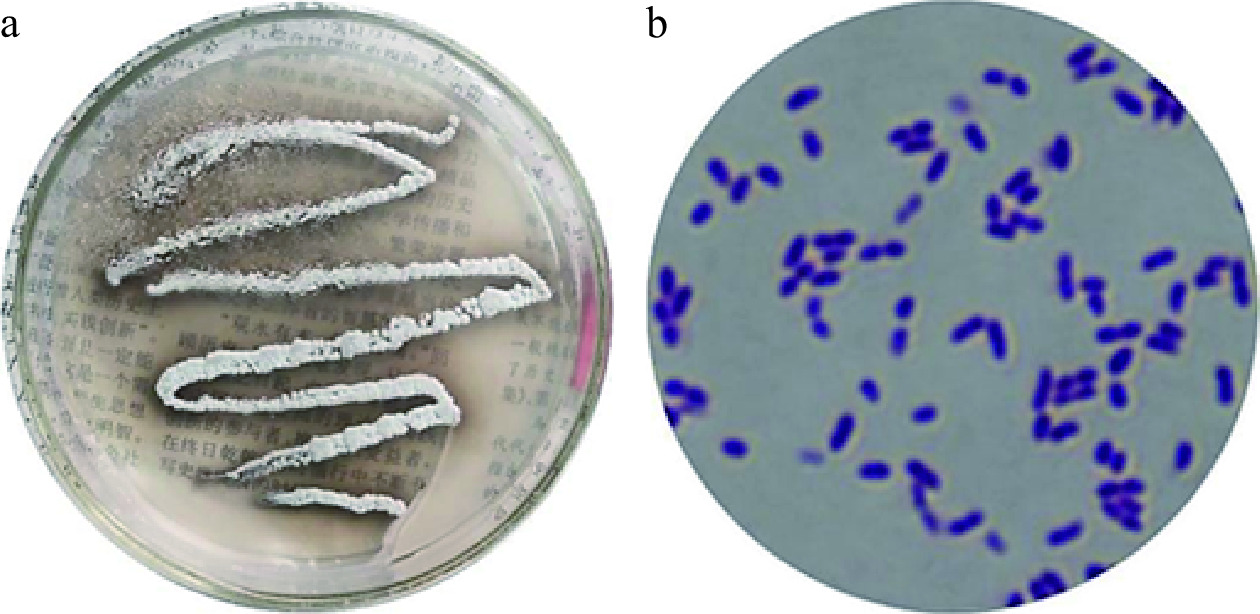
如图3a所示在固体种子培养基上培养的菌株LY-1,单菌落形态为点或圆形,边缘呈波状,颜色为浅白或乳白色,表面扁平,无光泽,无气味,表面干燥,不透明,菌落部分聚生,上似有一薄层“干粉”状物质,且菌株的革兰氏染色实验为阳性,可初步鉴定为放线菌。图3b为菌株LY-1的显微形态,可见单菌株多呈球形或者椭球形,其分布特点大致为多菌聚集状或单菌分散状。
2.4.2 LY-1号菌株生理生化鉴定
通过Biolog细菌自动鉴定仪对菌株的碳源利用率以及化学敏感程度进行检测,结果如表2所示,对比鉴定后初步判断该菌种为链霉菌属Streptomyces sp. LY-1,PROB值为0.929,Organism Type为革兰氏阳性链霉菌。
表 2 菌株LY-1碳源利用实验Table 2. Strain LY-1 carbon source utilisation experiments特征 结果 特征 结果 D-葡萄糖 + L-阿拉伯糖 + 柳醇 + D-果糖 + D-半乳糖 W L-鼠李糖 − D-甘露醇 + 松三糖 W 山梨醇 + D-麦芽糖 + D-木糖 + 棉子糖 − i-肌醇 + 海藻糖 − 淀粉 + 葡萄糖酸钠 + 蔗糖 − 酶氨基酸酶 + 果胶 + 琥珀酸钠 + 糖原 + 牛乳胨化 + 水杨苷 + 明胶液化 + L-苹果酸 + 硫化氢分解 − 核糖 + 纤维素分解 − 注:+为阳性;W为弱阳性;−为阴性。 用GenⅢ微孔板测试LY-1菌株碳源利用度以及相关酶学特征实验结果见表1。由表2可知,该菌株充分利用了D-葡萄糖、柳醇、i-肌醇、D-甘露醇、山梨醇、D-半乳糖、L-阿拉伯糖、D-果糖、果胶,也可以部分利用松三糖、D-半乳糖等碳源,而蔗糖、L-鼠李糖、棉子糖、海藻糖等其他碳源的利用率比较差。淀粉水解强,不产生硫化氢,不分解纤维素。明胶液化,牛奶凝固并胨化。
2.4.3 LY-1菌株16S rDNA序列分析与系统发育树的构建
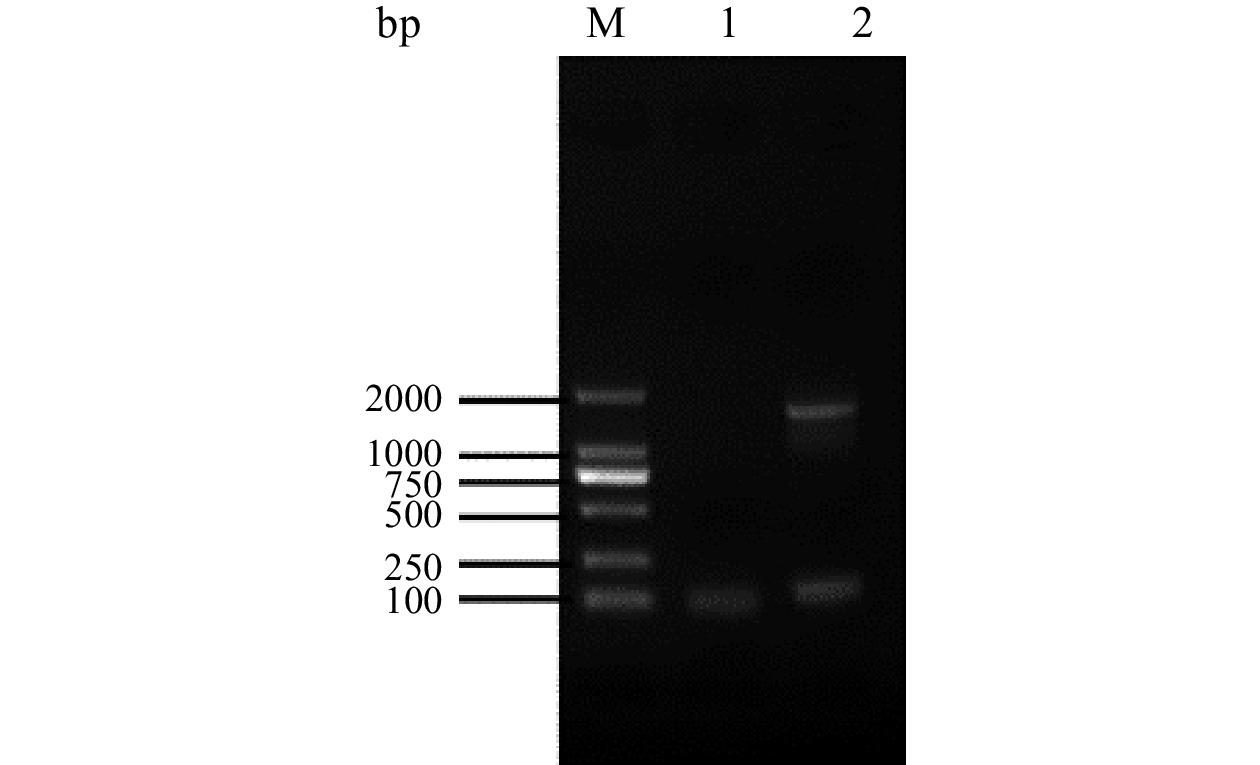
菌株LY-1的16S rDNA测序长度为1396 bp。如图4所示,在琼脂糖凝胶电泳图谱结果中可以看到扩增后的目的基因条带介于1000 bp和2000 bp之间,与16S rDNA测序结果相符。
通过菌落形态以及镜下特征可以初步鉴定出所得的菌株LY-1为放线菌,并结合其生理生化鉴定结果和培养特性的综合比较,最终确定菌株LY-1为链霉菌属。将获得的序列结果通过与Gen-Bank/DDBJ/EMBL数据库中的已知基因序列进行同源对比分析,发现菌株LY-1与放线菌橄榄灰链霉菌(Streptomyces olivogriseus)标准菌株AB184486.1的相似度达到99.79%,表明两者的亲缘关系最近,结合上述菌株的形态及生理生化特征可以鉴定LY-1为放线菌橄榄灰链霉菌,基于菌株16S rDNA基因构建的菌株LY-1的系统发育树如图5所示。
2.5 酶学特性
2.5.1 最适温度以及温度稳定性
如图6中a所示,菌株LY-1从低温至20 ℃区间酶活性呈上升趋势,在15~25 ℃区间内具有较高的酶活性,相对酶活高达90%以上,在20 ℃时菌株酶活达到最高值,故酶的最适反应温度在20 ℃左右,从20 ℃开始,随着温度的升高,酶活性开始缓慢下降,45 ℃以后,活性开始下降至80%以下。根据Marx等[31]的定义,通常把最适催化温度在30 ℃左右而在0 ℃仍然具有催化效率的酶称为低温酶。真菌来源果胶酶最适作用温度一般在30 ℃左右,如Sudeep等[32]发现的Aspergillus spp. Gm最适作用温度为30 ℃,细菌果胶酶最适温度相对于真菌果胶酶而言较高,能够达到50~60 ℃。而上述结果表明该菌株所产果胶酶的最适作用温度为20 ℃具有良好的低温耐受性并且对常温也有一定的抵抗能力;对酶的热稳定性研究如图6中b所示:当温度升至60 ℃时保存2 h其酶活性仍在70%以上,说明此酶对温度的适应性较强[32],更适合工业生产。
2.5.2 最适pH及pH稳定性
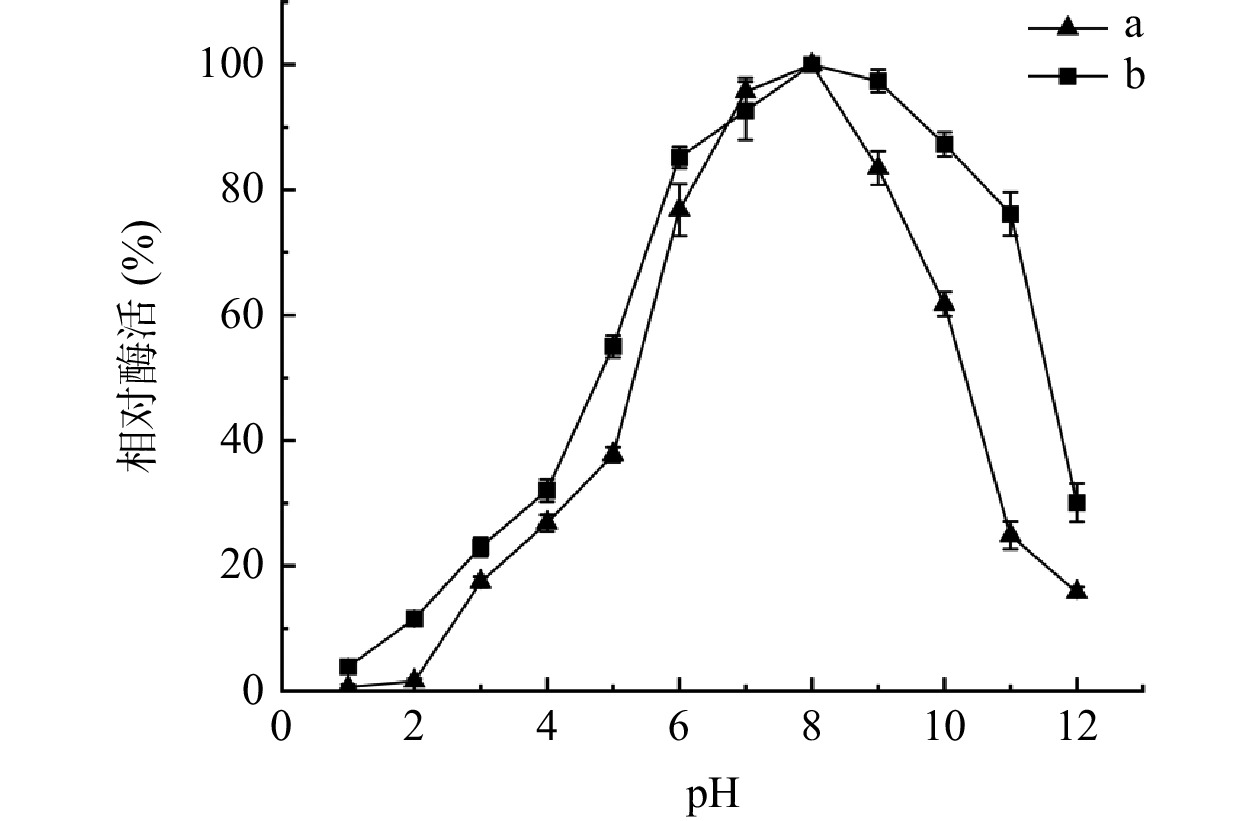
对酶的最适pH,pH稳定性分析,结果如图7中a所示,酸碱度会极大影响酶的的活性和稳定性,随着pH的逐步升高,酶活力逐步上升,当pH为8.0时,酶活达到最大,故此果胶酶的最适pH在8.0左右,即弱碱性环境下酶活达到最大,pH过高或者偏低的情况下,酶活较低,当pH小于7.0(大于9.0)时,酶活性下降的较快。如图7中b所示,果胶酶表现很高的pH稳定性,在pH为7.0~9.0范围内保温处理2 h,酶的残余活力均在90%以上,在碱性环境(pH为8.0~10.0)中随着pH逐步升高酶的稳定性在缓慢下降,但在pH为10的环境下仍能稳定在80%以上。说明该果胶酶在较宽的碱性范围内是非常稳定的。
2.5.3 金属离子对酶活的影响
不同金属离子对果胶酶酶活影响不同。如图8所示,在果胶酶酶解反应过程中加入不同金属离子,1和5 mmol/L的Cu2+、Ba2+、Mg2+、Ca2+、k+、Co2+处理组相对酶活(%)均显著大于对照组(P<0.001),对果胶酶起促进作用,Ba2+、Mg2+、K+和Ca2+在海洋中含量丰富,研究也表明其对海洋低温酶活性有显著促进作用。其中Cu2+、Ba2+最为显著(P<0.001)且高浓度下的促进作用较为明显,在浓度为5 mmol/L的条件下相对酶活达到了150%以上,可能是由于Ba2+、Cu2+与酶结合后改变了酶的空间结构,稳定了酶蛋白活性的构象,进而提高酶活力[33]。而Mn2+、Zn2+、Hg2+、Na+处理组相对酶活力(%)小于对照组(P<0.001),对果胶酶的酶活起抑制作用且高浓度下的抑制作用也较为明显。由于Hg2+具有氧化巯基抑制酶活的特性,说明该果胶酶活性中心附近可能有半胱氨酸残基[34]。而Mn2+、Zn2+抑制酶活性可能是由于这两种离子破坏了该酶的三维构象,使其更易发生失活所导致的,所以Mn2+、Zn2+、Hg2+对该果胶酶有显著的抑制作用。
3. 结论
以果胶为唯一碳源,利用透明圈法和DNS法从渤海湾底泥中筛出一株高产低温果胶酶的菌株LY-1,经过形态学、生理生化分析以及16S rDNA测序分析,并在NCBI等数据库中进行比对Mega构建系统发育树,最终确认为是橄榄灰链霉菌(Streptomyces olivogriseus)。经过酶学特性研究,发现此菌产果胶酶的最适温度为20 ℃,在4 ℃下仍能保持70%以上的酶活力,与大部分真菌、细菌等来源的果胶酶相比具有明显的低温酶特性及冷适应性,在60 ℃保存2 h酶活仍在70%以上,表明该低温酶也具有一定的热稳定性;最适酶反应pH为8.0,在pH为7.0~9.0处理2 h,其酶活力均可维持80%以上,表明该果胶酶的碱耐受性较好;金属离子Cu2+、Ba2+、Mg2+、Ca2+、K+、Co2+对果胶酶活性有促进作用,以Ba2+、Cu2+最为显著(0.0001<P<0.001),而金属离子Mn2+、Zn2+、Hg2+对果胶酶活性则有明显的抑制作用。后续研究中可对其进行基因克隆、酶蛋白修饰等从而进一步提高酶活性,为开发更高效、环境友好的生产工艺及低温碱性果胶酶在食品工业中的应用提供参考。
-
表 1 产果胶酶菌株初筛结果
Table 1 Results of the initial screening of pectinase-producing strains
菌株编号 水解圈直径Dp(mm) 菌落直径Dc(mm) Dp/Dc LY-1 10.30±0.56 2.20±0.20 4.72±0.67 LY-6 6.76±0.35 1.73±0.25 3.94±0.51 LY-7 9.76±0.61 3.13±0.55 3.15±0.35 LY-9 11.86±0.45 3.00±0.36 4.00±0.60 LY-11 12.67±0.45 2.40±0.10 5.28±0.35 LY-16 9.03±0.42 1.83±0.21 4.99±0.38 表 2 菌株LY-1碳源利用实验
Table 2 Strain LY-1 carbon source utilisation experiments
特征 结果 特征 结果 D-葡萄糖 + L-阿拉伯糖 + 柳醇 + D-果糖 + D-半乳糖 W L-鼠李糖 − D-甘露醇 + 松三糖 W 山梨醇 + D-麦芽糖 + D-木糖 + 棉子糖 − i-肌醇 + 海藻糖 − 淀粉 + 葡萄糖酸钠 + 蔗糖 − 酶氨基酸酶 + 果胶 + 琥珀酸钠 + 糖原 + 牛乳胨化 + 水杨苷 + 明胶液化 + L-苹果酸 + 硫化氢分解 − 核糖 + 纤维素分解 − 注:+为阳性;W为弱阳性;−为阴性。 -
[1] YU P, XU C C. Production optimization, purification and characterization of a heat-tolerant acidic pectinase from Bacillus sp. ZJ1407[J]. International Journal of Biological Macromolecules,2018,108:972−980. doi: 10.1016/j.ijbiomac.2017.11.012
[2] SHARMA N, RATHORE M, SHARMA M. Microbial pectinase:sources, characterization and applications[J]. Reviews in Environmental Science and Bio/Technology,2013,12(1):45−60. doi: 10.1007/s11157-012-9276-9
[3] ALQAHTANI Y S, MORE S S, R K, et al. Production and purification of pectinase from Bacillus subtilis 15A-B92 and its biotechnological applications[J]. Molecules (Basel, Switzerland),2022,27(13):4195. doi: 10.3390/molecules27134195
[4] HUANG D M, SONG Y Y, LIU Y L, et al. A new strain of Aspergillus tubingensis for high-activity pectinase production[J]. Brazilian Journal of Microbiology,2019,50(1):53−65. doi: 10.1007/s42770-018-0032-3
[5] AMIN F, BHATTI H N, BILAL M. Recent advances in the production strategies of microbial pectinases-A review[J]. International Journal of Biological Macromolecules,2019,122:1017−1026. doi: 10.1016/j.ijbiomac.2018.09.048
[6] 于平, 王欣馨, 任倩, 等. 产碱性果胶酶菌株的筛选和鉴定及其酶学性质[J]. 中国食品学报,2018,18(9):288−296. [YU Ping, WANG Xinxin, REN Qian, et al. Screening and identification of alkaline pectinase-producing strains and their enzymatic properties[J]. Chinese Journal of Food Science,2018,18(9):288−296.] YU Ping, WANG Xinxin, REN Qian, et al. Screening and identification of alkaline pectinase-producing strains and their enzymatic properties[J]. Chinese Journal of Food Science, 2018, 18(9): 288−296.
[7] ABDOLLAHZADEH R, PAZHANG M, NAJAVAND S, et al. Screening of pectinase-producing bacteria from farmlands and optimization of enzyme production from selected strain by RSM[J]. Folia Microbiologica,2020,65(4):705−719. doi: 10.1007/s12223-020-00776-7
[8] ZENI J, CENCE K, GRANDO C E, et al. Screening of pectinase-producing microorganisms with polygalacturonase activity[J]. Applied Biochemistry and Biotechnology,2011,163(3):383−392. doi: 10.1007/s12010-010-9046-5
[9] ZHANG W, XU P, ZHANG H. Pectin in cancer therapy:A review[J]. Trends in Food Science & Technology,2015,44(2):258−271.
[10] JIN M Y, LI M Y, HUANG R M, et al. Structural features and anti-inflammatory properties of pectic polysaccharides:A review[J]. Trends in Food Science & Technology,2021,107:284−298.
[11] KOHLI P, GUPTA R. Alkaline pectinases:A review[J]. Biocatalysis and Agricultural Biotechnology,2015,4(3):279−285. doi: 10.1016/j.bcab.2015.07.001
[12] BELDMAN G, ROMBOUTS F M, VORAGEN A G J, et al. Application of cellulase and pectinase from fungal origin for the liquefaction and saccharification of biomass[J]. Enzyme and Microbial Technology,1984,6(11):503−507. doi: 10.1016/0141-0229(84)90004-8
[13] HAILE S, AYELE A. Pectinase from microorganisms and its industrial applications[J]. The Scientific World Journal,2022,2022:1881305.
[14] HAILE S, MASI C, TAFESSE M. Isolation and characterization of pectinase-producing bacteria (Serratia marcescens) from avocado peel waste for juice clarification[J]. BMC Microbiology,2022,22(1):145. doi: 10.1186/s12866-022-02536-8
[15] SATAPATHY S, ROUT J R, KERRY R G, et al. Biochemical prospects of various microbial pectinase and pectin:An approachable concept in pharmaceutical bioprocessing[J]. Frontiers in Nutrition,2020,7:117. doi: 10.3389/fnut.2020.00117
[16] MAT JALIL M T, ZAKARIA N A, SALIKIN N H, et al. Assessment of cultivation parameters influencing pectinase production by Aspergillus niger LFP-1 in submerged fermentation[J]. Journal, Genetic Engineering & Biotechnology, 2023, 21(1):45.
[17] BHATTACHARYYA R, MUKHOPADHYAY D, NAGARAKSHITA V K, et al. Thermostable and organic solvent-tolerant acid pectinase from Aspergillus terreus FP6:Purification, characterization and evaluation of its phytopigment extraction potential[J]. 3 Biotech,2021,11(11):487. doi: 10.1007/s13205-021-03033-x
[18] SHRESTHA S, RAHMAN M S, QIN W. New insights in pectinase production development and industrial applications[J]. Applied Microbiology and Biotechnology,2021,105(24):9069−9087. doi: 10.1007/s00253-021-11705-0
[19] 卢晓华. 果胶酶产生菌的筛选鉴定、产酶条件优化及酶学性质研究[D]. 武汉:湖北工业大学, 2016. [LU Xiaohua. Screening and identification of pectinase-producing bacteria, optimization of enzyme-producing conditions and enzymatic properties[D]. Wuhan:Hubei University of Technology, 2016.] LU Xiaohua. Screening and identification of pectinase-producing bacteria, optimization of enzyme-producing conditions and enzymatic properties[D]. Wuhan: Hubei University of Technology, 2016.
[20] 昝梦华. 黑曲霉SH312-26-19产聚半乳糖醛酸酶的分离纯化及鉴定[D]. 太原:山西农业大学, 2016. [ZAN Menghua. Isolation, purification and identification of polygalactouronic enzyme producing by Aspergillus niger SH312-26-19[D]. Taiyuan:Shanxi Agricultural University, 2016.] ZAN Menghua. Isolation, purification and identification of polygalactouronic enzyme producing by Aspergillus niger SH312-26-19[D]. Taiyuan: Shanxi Agricultural University, 2016.
[21] 蓝丽精. 高产果胶酶菌株的筛选、发酵条件优化及其应用的研究[D]. 金华:浙江师范大学, 2012. [LAN Lijing. Screening, optimization of fermentation conditions and application of high-yielding pectinase strains[D]. Jinhua:Zhejiang Normal University, 2012.] LAN Lijing. Screening, optimization of fermentation conditions and application of high-yielding pectinase strains[D]. Jinhua: Zhejiang Normal University, 2012.
[22] JAYANI R S, SAXENA S, GUPTA R. Microbial pectinolytic enzymes:A review[J]. Process Biochemistry,2005,40(9):2931−2944. doi: 10.1016/j.procbio.2005.03.026
[23] IBRAHIM D, WELOOSAMY H, SHEH-HONG L. Potential use of nylon scouring pad cubes attachment method for pectinase production by Aspergillus niger HFD5A-1[J]. Process Biochemistry,2014,49(4):660−667. doi: 10.1016/j.procbio.2014.01.012
[24] 李碧婵, 肖国利, 黄星星, 等. 一株产果胶酶芦苇内生真菌的分离、鉴定及酶学性质研究[J]. 中国酿造,2021,40(6):92−96. [LI Bichan, XIAO Guoli, HUANG Xingxing, et al. Isolation, identification and enzymatic properties of a pectinase-producing reed endophytic fungus[J]. China Brewing,2021,40(6):92−96.] LI Bichan, XIAO Guoli, HUANG Xingxing, et al. Isolation, identification and enzymatic properties of a pectinase-producing reed endophytic fungus[J]. China Brewing, 2021, 40(6): 92−96.
[25] LI H, MCKEE L S. Measuring enzyme kinetics of glycoside hydrolases using the 3, 5-dinitrosalicylic acid assay[J]. Methods in Molecular Biology,2023,2657:15−25.
[26] 刘烨瑀, 张金平, 陈立功, 等. 产褐藻胶裂解酶菌株筛选、鉴定与酶学性质研究[J]. 食品科技,2022,47(9):8−14. [LIU Yeyi, ZHANG Jinping, CHEN Ligong, et al. Screening, identification and enzymatic properties of fucogen-producing lyase strains[J]. Food Science and Technology,2022,47(9):8−14.] LIU Yeyi, ZHANG Jinping, CHEN Ligong, et al. Screening, identification and enzymatic properties of fucogen-producing lyase strains[J]. Food Science and Technology, 2022, 47(9): 8−14.
[27] 刘均珠, 黄玉婷, 梁丽陈, 等. 产果胶酶菌株的筛选鉴定及产酶条件初步优化[J]. 饲料研究,2022,45(11):71−75. [LIU Junzhu, HUANG Yuting, LIANG Lichen, et al. Screening and identification of pectinase-producing strains and preliminary optimization of enzyme-producing conditions[J]. Feed Research,2022,45(11):71−75.] LIU Junzhu, HUANG Yuting, LIANG Lichen, et al. Screening and identification of pectinase-producing strains and preliminary optimization of enzyme-producing conditions[J]. Feed Research, 2022, 45(11): 71−75.
[28] 蒙锦, 张树竹, 赵桐桦, 等. 小粒咖啡湿法发酵中产果胶酶菌株的筛选鉴定及产酶条件优化[J]. 云南民族大学学报(自然科学版),2023,32(2):192−198. [MENG Jin, ZHANG Shuzhu, ZHAO Tonghua, et al. Screening and identification of pectinase-producing strains in wet fermentation of small coffee and optimization of enzyme-producing conditions[J]. Journal of Yunnan University for Nationalities (Natural Science Edition),2023,32(2):192−198.] MENG Jin, ZHANG Shuzhu, ZHAO Tonghua, et al. Screening and identification of pectinase-producing strains in wet fermentation of small coffee and optimization of enzyme-producing conditions[J]. Journal of Yunnan University for Nationalities (Natural Science Edition), 2023, 32(2): 192−198.
[29] 陈立功, 吴家葳, 张庆芳, 等. 产低温几丁质酶菌株的筛选、鉴定与产酶条件优化[J]. 食品工业科技,2020,41(23):85−90,98. [CHEN Ligong, WU Jiawei, ZHANG Qingfang, et al. Screening, Identification and optimization of enzyme-producing conditions of low-temperature chitinase-producing strains[J]. Science and Technology of Food Industry,2020,41(23):85−90,98.] CHEN Ligong, WU Jiawei, ZHANG Qingfang, et al. Screening, Identification and optimization of enzyme-producing conditions of low-temperature chitinase-producing strains[J]. Science and Technology of Food Industry, 2020, 41(23): 85−90,98.
[30] 袁宗胜, 刘芳, 穆景利, 等. 解淀粉芽孢杆菌JL-B05生物学特性及生理生化指标测定[J]. 安徽农业科学,2020,48(14):1−3. [YUAN Zongsheng, LIU Fang, MU Jingli, et al. Determination of biological characteristics and physiological and biochemical indexes of Bacillus amyllyticus JL-B05[J]. Journal of Anhui Agricultural Sciences,2020,48(14):1−3.] YUAN Zongsheng, LIU Fang, MU Jingli, et al. Determination of biological characteristics and physiological and biochemical indexes of Bacillus amyllyticus JL-B05[J]. Journal of Anhui Agricultural Sciences, 2020, 48(14): 1−3.
[31] MARX J C, COLLINS T, D’AMICO S, et al. Cold-adapted enzymes from marine Antarctic microorganisms[J]. Marine Biotechnology,2007,9(3):293−304. doi: 10.1007/s10126-006-6103-8
[32] SUDEEP K C, JITENDRA U, DEV R J, et al. Production, characterization, and industrial application of pectinase enzyme isolated from fungal strains[J]. Fermentation,2020,6(2):59. doi: 10.3390/fermentation6020059
[33] 张小丹, 赵赛赛, 林一, 等. 果胶酶产生菌Bacillus subtilis Z-5的筛选及酶学性质的研究[J]. 食品与发酵工业,2023,49(11):34−40. [ZHANG Xiaodan, ZHAO Saisai, LIN Yi, et al. Screening and enzymatic properties of Pectinase-producing bacteria Bacillus subtilis Z-5[J]. Food and Fermentation Industry,2023,49(11):34−40.] ZHANG Xiaodan, ZHAO Saisai, LIN Yi, et al. Screening and enzymatic properties of Pectinase-producing bacteria Bacillus subtilis Z-5[J]. Food and Fermentation Industry, 2023, 49(11): 34−40.
[34] MANDAL A, KAR S, DAS MOHAPATRA P K, et al. Purification and characterization of an endoxylanase from the culture broth of Bacillus cereus BSA1[J]. Prikladnaia Biokhimiia I Mikrobiologiia,2011,47(3):277−282.





 下载:
下载:



 下载:
下载:
