Determination of 30 Kinds of Antiparasitic Drugs in Animal-derived Foods by QuEChERS-UPLC-MS/MS
-
摘要: 目的:采用超高效液相色谱-串联质谱法,建立测定动物源性食品中30种抗寄生虫类药物残留的方法。方法:样品经乙腈、1%氨水乙酸乙酯提取,经QuEChERS净化。净化后采用Waters ACQUITY UPLCTM BEH C18色谱柱分离,10 mmol/L甲酸铵(含0.1%甲酸)水溶液-乙腈:甲醇(50:50,v:v)为流动相进行梯度洗脱,电喷雾离子源正负离子切换多反应监测(Multiple Reaction Monitoring,MRM)模式下进行检测,基质匹配外标法定量。结果:在优化的条件下,30种抗寄生虫类药物在各自的线性范围内线性良好,决定系数(r2)均大于0.99;回收率为70.1%~111%;相对标准偏差在0.10%~9.1%之间(n=6);方法检出限为0.001~0.3 μg/kg之间,方法定量限在0.004~1 μg/kg。结论:该方法灵敏、准确,具有良好的重复性和稳定性,可用于动物源性食品中多种抗寄生虫药物残留的检测。
-
关键词:
- 抗寄生虫药物 /
- 超高效液相色谱-串联质谱法 /
- QuEChERS /
- 动物源性食品 /
- 药物残留
Abstract: Objective: A method for determining the residues of 30 antiparasitic drugs in animal-derived food using ultra-high-performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS) was established. Methods: The samples were extracted with acetonitrile and 1% ammonia acetic ether and purified by QuEChERS. After purification, Waters ACQUITY UPLCTM BEH C18 column was used for separation, and a gradient elution of 10 mmol/L ammonium formate (containing 0.1% formic acid) aqueous solution, acetonitrile:methanol (50:50, v:v) was performed as the mobile phase. Detection was carried out using electrospray ionization (ESI) in both positive and negative ion modes using multiple reaction monitoring (MRM). Matrix-matched external standard quantification was used. Results: Under the optimized conditions, the 30 antiparasitic drugs showed good linearity within their respective linear ranges, with coefficient of determination (r2) greater than 0.99. The recoveries ranged from 70.1% to 111%, and the relative standard deviations were between 0.10% and 9.1% (n=6). The method detection limit ranged from 0.001 to 0.3 μg/kg, and the method quantification limit ranged from 0.004 to 1 μg/kg. Conclusion: The method is sensitive, accurate, and exhibits good repeatability and stability, making it suitable for detecting various antiparasitic drug residues in animal-derived food. -
动物在生长过程中由于食物和环境原因常会感染寄生虫病。寄生虫病是动物的主要疾病之一,导致动物生产性能下降甚至死亡,影响畜牧养殖业的健康发展和经济效益,甚至威胁人类的健康[1]。为了预防和治疗动物寄生虫病,大量抗寄生虫药物被应用于养殖过程。目前使用传统化学合成类药物居多,也有一些中草药被补充使用[2]。常规抗虫药作用时间有限,需要反复用药,也造成了其在动物体内的蓄积。食用抗寄生虫药物残留较多的畜禽产品会对机体健康产生危害,如引起人体的过敏反应或急性中毒,甚至可能致畸或致癌[3−4]。我国以及欧盟、美国、日本等国家都已将多种抗寄生虫类药物列入限制使用的兽药药物中,并制订出各种抗寄生虫类药物(包括其某些代谢物)在不同动物体内(包括肌肉、组织、奶等)的最高残留限量(maximum residue limit,MRL)[5]。中国于2019年9月6日发布了GB 31650-2019《食品安全国家标准食品中兽药最大残留限量》,其中对动物性食品有最大残留量规定的兽药共104种,而抗寄生虫药物达55种[6]。
目前检测分析抗寄生虫药物的方法主要包括高效液相色谱法[7−8]、液相色谱-串联质谱法[9−22]、酶联免疫吸附测定法(ELISA)[23−24]、免疫层析试纸法[25]、毛细管电泳法[26]等,其中液相色谱-串联质谱法相对于其他方法,具有准确性和灵敏度高,选择性和抗干扰性较强,可实现多目标组分同时分析等优势,被广泛应用于动物源性食品中兽药残留的分析测定。陈瑞等[9]采用超高效液相色谱-串联质谱法测定牛奶和奶粉中五种苯并咪唑类药物;温海滨等[10]和Xu等[11]采用超高效液相色谱-串联质谱法测定水产品中苯并咪唑类药物;张绍伟等[12]采用超高效液相色谱-串联质谱法测定牛奶中的三聚氰胺、环丙氨嗪、地昔尼尔;Zhao等[13]、奚照寿等[14]和Wang等[15]分别采用超高效液相色谱-串联质谱法测定牛肉、鸡肉、鸡蛋中的抗球虫药物;吴映璇等[17]采用高效液相色谱-串联质谱法测定乳制品中的莫奈太尔及其代谢物;张敏等[18]采用超高效液相色谱-串联质谱法测定牛乳中硝碘酚腈等6种兽药残留。可见近年来国内外对抗寄生虫类药物残留的研究大多是针对单个抗寄生虫药物、单一类别或者作用机制相似的几种药物进行分析,且适用的样品基质也比较单一。目前针对抗寄生虫药物残留的检测缺少一种可同时检测多种抗寄生虫药物且适用于多种样品基质的检测方法,难以满足现代分析技术快速、高效的要求。
本方法通过对仪器和前处理方法的优化,采用超高效液相色谱-串联质谱法,实现了动物源性食品(畜禽肉、水产品、牛奶、鸡蛋)中共计30种抗寄生虫类药物残留的检测。该方法具有高效、快速、检测成本低、灵敏度高的特点,是一种高通量的筛查方法,可为相关监管部门监控动物源性食品中的抗寄生虫药物残留提供技术支持。
1. 材料与方法
1.1 材料与仪器
动物源性食品 畜禽肉、水产品、牛奶、鸡蛋 均购自本地市场;氨丙啉、地昔尼尔、罗硝唑、双咪苯脲、左旋咪唑、噻苯达唑、奥芬达唑、常山酮、乙氧酰胺苯甲酯、奥苯达唑、甲苯咪唑、氟苯达唑、阿苯达唑、吡喹酮、氯苯胍、芬苯达唑、非班太尔、三氯苯达唑、癸氧喹酯、莫西克丁、米尔贝肟、莫能霉素、拉沙洛西、盐霉素、马杜霉素、甲基盐霉素、硝碘酚腈、硝唑尼特、莫奈太尔、氯氰碘柳胺 德国Dr. Ehrenstorfer公司;甲酸、乙腈、甲醇、甲酸铵、二甲亚砜 色谱纯,德国Merck公司;氨水、乙酸乙酯、无水硫酸钠、无水硫酸镁 分析纯,西陇科学股份有限公司;乙二胺-N-丙基甲硅烷(PSA,粒度4 μm)、十八烷基键合硅胶吸附剂(ODS-C18,粒度4 μm) 日本GL Sciences公司; Milli-Q 超纯水(电导率>18.2 mΩ) 美国Millipore公司;0.22 µm聚四氟乙烯(PTFE)滤膜 美国ASC公司。
LC-30AD超高效液相色谱仪、Shimadzu 8050三重四极杆-串联质谱仪 日本岛津公司;ACQUITY UPLCTM BEH C18色谱柱(2.1×100 mm,1.7 μm) 美国Waters公司;BT 224 S电子分析天平 德国Sartorius公司;Aanti J-E高速冷冻离心机 美国Beckman Coulter公司;Milli-Q超纯水纯化系统 美国Millipore公司;DS-8510 DTH超声波振荡器 上海分析超声仪器有限公司;MS 3 basic旋涡混均器 美国IKA公司;AUTO EVA-80 自动氮吹仪 中国睿科公司。
1.2 实验方法
1.2.1 标准溶液的配制
标准储备液:分别称取适量固体标准品,用合适的溶剂溶解并定容至10 mL容量瓶中,配制成约100 mg/L的储备液,−18 ℃避光密闭保存。(双咪苯脲、三氯苯达唑、氟苯达唑、甲苯咪唑、噻苯达唑、阿苯达唑、芬苯达唑、奥芬达唑、奥苯达唑、非班太尔用适量二甲亚砜溶解并用甲醇定容;其它药物标准品用甲醇溶解并定容)
混合标准中间液:分别移取一定量的各个标准储备液用乙腈定容至刻度线,配制成混合标准物质中间液(表1),4 ℃避光密闭保存。
表 1 30种抗寄生虫类药物浓度、线性方程、决定系数(r2)检出限及定量限Table 1. Concentration, regression equations, coefficient of determination (r2), LODs, LOQs of the 30 antiparasitic drugs化合物 中间液浓度(mg/L) 线性范围(μg/L) 线性回归方程 决定系数(r2) 检出限(μg/kg) 定量限(μg/kg) 氨丙啉 1.00 1.00~50.0 Y=118986X+298045 0.9983 0.02 0.06 地西尼尔 1.00 1.00~50.0 Y=4623.8X+12084 0.9995 0.2 0.8 罗硝唑 1.00 1.00~50.0 Y=31112X+66997 0.9999 0.02 0.06 双咪苯脲 1.00 1.00~50.0 Y=73074X+147955 0.9986 0.1 0.4 左旋咪唑 0.500 0.500~25.0 Y=43378X+70131 0.9970 0.03 0.1 噻苯达唑 0.200 0.200~10.0 Y=71640X+18772 0.9997 0.02 0.06 奥芬达唑 1.00 1.00~50.0 Y=27873X+90090 0.9964 0.04 0.1 常山酮 1.00 1.00~50.0 Y=8064.5X+18747 0.9990 0.04 0.1 乙氧酰胺苯甲酯 0.200 0.200~10.0 Y=91253X+52608 0.9985 0.004 0.01 奥苯达唑 0.0200 0.0200~1.00 Y=1E+06X+46316 0.9992 0.001 0.004 甲苯达唑 0.200 0.200~10.0 Y=167434X+76679 0.9996 0.01 0.04 氟苯达唑 0.200 0.200~10.0 Y=115535X+46360 0.9991 0.01 0.02 阿苯达唑 0.10 0.100~5.00 Y=391021X+113444 0.9979 0.003 0.01 吡喹酮 1.00 1.00~50.0 Y=50795X+95961 0.9996 0.05 0.2 氯苯胍 1.00 1.00~50.0 Y=28992X+65410 0.9980 0.1 0.4 芬苯达唑 0.100 0.100~5.00 Y=263625X+69199 0.9980 0.003 0.01 非班太尔 0.200 0.200~10.0 Y=83622X+29374 0.9991 0.004 0.01 三氯苯达唑 0.500 0.500~25.0 Y=43264X+37943 0.9992 0.02 0.05 癸氧喹酯 0.500 0.500~25.0 Y=60166X+41980 0.9980 0.01 0.03 莫昔克丁 10.0 10.0~500 Y=419.68X+5611.9 0.9993 0.1 0.4 米尔贝肟 10.0 10.0~500 Y=5987.1X+121343 0.9986 0.3 1 莫能霉素 1.00 1.00~50.0 Y=6001.4X−47.666 0.9999 0.02 0.07 拉沙洛西 1.00 1.00~50.0 Y=57948X+128990 0.9990 0.07 0.2 盐霉素 1.00 1.00~50.0 Y=13199X+29194 0.9994 0.04 0.1 马杜霉素 1.00 1.00~50.0 Y=36028X+54891 0.9997 0.02 0.05 甲基盐霉素 0.200 0.200~10.0 Y=126919X+53423 0.9994 0.003 0.01 硝碘酚腈 1.00 1.00~50.0 Y=4583.5X+15315 0.9987 0.05 0.2 硝唑尼特 1.00 1.00~50.0 Y=24664X+3629.8 0.9999 0.04 0.1 莫奈太尔 1.00 1.00~50.0 Y=4606.2X+14766 0.9978 0.02 0.07 氯氰碘柳胺 1.00 1.00~50.0 Y=6087.2X+63425 0.9984 0.08 0.3 基质匹配系列标准溶液:取适量体积的混合标准物质中间液,用空白基质提取液稀释成标准系列工作曲线溶液(表1),上机测试。
1.2.2 样品前处理
准确称取均质后的试样2 g(精确至 0.0001 g)于 50 mL 离心管中,加入5 g无水硫酸钠,加入5 mL乙腈,涡旋30 s,超声提取20 min,以4000 r/min 离心5 min,上清液转移至另一50 mL离心管中,残渣中加入5 mL1%氨水乙酸乙酯重复提取一次,离心,合并2次上清液,待净化。将提取液加入到含有200 mg无水硫酸镁、100 mg C18和100 mg PSA的离心管中,涡旋2 min,离心,取5 mL净化后的上清液,于40 ℃氮气吹至近干,用1.00 mL 50%乙腈-水溶液复溶,过PTFE滤膜,上机测试。
1.2.3 液相色谱-串联质谱条件
液相色谱条件:色谱柱:ACQUITY UPLCTM BEH C18(2.1×100 mm,1.7 μm);流动相:A为10 mmol/L甲酸铵(含0.1%甲酸)水溶液,B为乙腈:甲醇(50:50);流速:0.30 mL/min;柱温:40 ℃;进样量:2 μL;洗脱梯度:0~1.00 min,10% B;1.00~9.00 min,10%~95% B;9.00~12.00 min,95% B;12.01~14.00 min,10 % B。
质谱条件:电喷雾离子源正负离子切换模式;多反应监测模式;加热块温度:400 ℃;加热气流速:10.0 L/min;接口电压(ESI+:+4000 V,ESI−:−3000 V);雾化气流速:2.5 L/min;干燥气流速:10.0 L/min;脱溶剂温度:600 ℃;定性离子、定量离子及其他质谱参数见表2。
表 2 目标化合物的质谱参数Table 2. Mass parameters of analytes mass parameters of analytes序号 化合物名称 保留时间(min) 母离子(m/z) 子离子(m/z) 四级杆1电压(V) 碰撞电压(V) 四级杆3电压(V) ESI模式 1 氨丙啉 1.50 243.2 150.2*/94.2 22/22 13/11 19/16 + 2 地昔尼尔 2.27 191.1 150.1*/109.2 27/12 20/26 30/22 + 3 罗硝唑 2.93 201.1 140.1*/55.1 14/13 13/23 14/21 + 4 双咪苯脲 3.29 349.2 188.2*/162.2 12/12 28/24 21/18 + 5 左旋咪唑 3.50 205.0 178.2*/91.2 30/30 20/39 23/18 + 6 噻苯达唑 4.26 201.9 175.2*/131.2 30/29 24/31 20/14 + 7 奥芬达唑 5.46 316.1 159.1*/284.0 21/20 40/17 29/21 + 8 常山酮 5.53 415.6 120.2*/138.3 26/25 21/20 25/27 + 9 乙氧酰胺苯甲酯 5.56 237.8 206.2*/136.2 15/23 10/26 23/15 + 10 奥苯达唑 5.98 249.8 218.2*/176.2 30/16 18/26 24/20 + 11 甲苯咪唑 6.30 296.1 264.1*/105.1 10/14 24/34 28/20 + 12 氟苯达唑 6.50 314.1 282.1*/123.2 14/15 24/36 28/23 + 13 阿苯达唑 6.87 266.1 234.1*/191.0 12/12 20/33 16/19 + 14 吡喹酮 7.18 312.8 203.2*/174.2 20/20 17/29 23/19 + 15 氯苯胍 7.22 333.9 155.2*/138.2 20/20 21/26 29/27 + 16 芬苯达唑 7.32 299.9 268.1*/159.2 15/30 23/35 21/30 + 17 非班太尔 7.76 446.6 383.1*/415.1 28/30 20/13 28/30 + 18 三氯苯达唑 8.31 358.8 274.1*/198.1 22/23 34/27 30/22 + 19 癸氧喹酯 9.27 418.2 372.2*/204.1 20/20 25/44 20/21 + 20 莫西克丁 9.84 640.1 199.1*/528.2 22/40 27/11 23/40 + 21 米尔贝肟 9.92 556.1 167.2*/538.3 34/34 24/18 30/40 + 22 莫能霉素 9.95 693.6 461.3*/479.3 40/40 54/55 24/25 + 23 拉沙洛西 10.1 613.4 377.3*/359.3 28/20 39/37 28/27 + 24 盐霉素 10.1 773.6 431.3*/531.3 26/26 51/44 23/40 + 25 马杜霉素 10.3 935.5 877.5*/895.6 26/20 34/54 30/36 + 26 甲基盐霉素 10.6 787.6 431.2*/531.4 30/30 45/45 20/30 + 27 硝碘酚腈 5.57 288.8 127.1*/162.2 13/18 25/22 12/10 − 28 硝唑尼特 7.09 264.0 217.1*/144.2 24/30 14/17 23/28 − 29 莫奈太尔 8.13 471.9 186.2*/166.3 22/22 23/45 12/30 − 30 氯氰碘柳胺 9.10 660.9 315.1*/344.9 28/28 33/35 21/11 − 注:*为定量离子。 1.2.4 定性及定量处理
定性处理:在同样测试条件下,试样溶液中各目标物的保留时间与基质匹配标准溶液中相应目标物的保留时间,偏差在±2.5%以内,且检测到的相对离子丰度,应当与浓度相当的基质匹配标准溶液相对离子丰度一致。(相对离子丰度允许偏差应符合以下要求:当相对离子丰度>50%时,允许的最大偏差为±20%;当相对离子丰度介于20%~50%时,允许的最大偏差为±25%;当相对离子丰度介于10%~20%时,允许的最大偏差为±30%;当相对离子丰度≤10%时,允许的最大偏差为±50%。)
定量处理:按照1.2.3设定仪器条件,以基质匹配标准溶液浓度为横坐标,以峰面积为纵坐标,绘制标准工作曲线作多点校准,按外标法计算试样中药物的残留量。
1.3 数据处理
UPLC-MS/MS配有 LabSolutions 数据处理软件建立标准曲线、计算结果,采用 Microsoft Excel处理数据及绘制图表。谱图为 Origin 2018 做图软件绘制。
2. 结果与分析
2.1 质谱条件的优化
分别取适量储备液以50% 乙腈稀释成浓度约为1.0 mg/L的单个标准使用液进入质谱,分别选择正、负离子模式进行一级全扫描,确定各目标化合物的母离子。本研究涉及的大多数目标药物在正离子模式下离子强度更高,如阿咪唑类、聚醚类、化学合成抗球虫药等更易形成带正电荷的离子,如[M+H]+、[M+Na]+;小部分目标药物在负离子模式下离子响应更好,如硝碘酚腈、氯氰碘柳胺、硝唑尼特、莫奈太尔更易失去质子生成带负电荷的离子[M-H]−。将得到的母离子施加一定的碰撞能量进行 Product Ion(MS2)扫描,获得各自的二级碎片离子,选择 2个信号较强且干扰小的碎片离子与其母离子组成监测离子对。再将得到的母离子和碎片离子,采用多反应监测模式进行仪器自动优化各化合物的四级杆1电压、碰撞电压和四级杆3电压,定量和定性离子见表2。
2.2 色谱条件的优化
2.2.1 色谱柱的选择
本研究涉及的药物多为中等极性或弱极性的化合物,现有研究多采用C18及T3色谱柱进行检测。本研究考察了ACQUITY UPLCTM BEH C18(2.1 mm×100 mm,1.7 μm)、ACQUITY UPLCTM HSS T3(2.1 mm×150 mm,1.8 μm)的分离效果。结果表明,在相同液相条件下大多数化合物在T3柱及C18柱上的的峰形并无太大差异,但双咪苯脲、米尔贝肟、拉沙洛西在BEH C18柱上的峰形及响应优于T3柱。且T3柱对大多数化合物的保留比C18柱强,但部分弱极性物质保留过强,洗脱耗时更长。最终根据分离效果、峰型及保留时间的稳定性,本研究选择ACQUITY UPLCTM BEH C18色谱柱作为分析柱。
2.2.2 流动相的选择
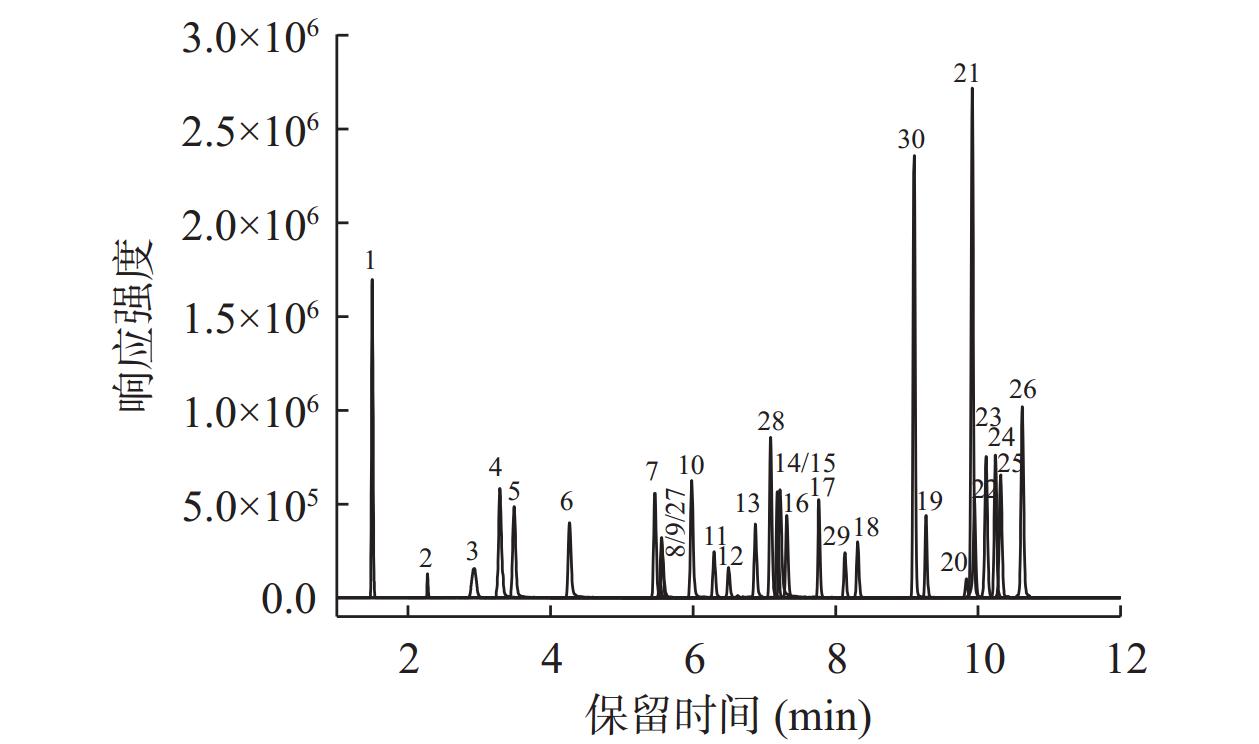
本研究比较了采用乙腈-水和甲醇-水作为流动时的分离效果与保留情况,结果表明乙腈洗脱能力更强,药物出峰时间更早也更密集,且洗脱时会产生较多杂峰。而使用甲醇为有机相时杂峰较少,但有部分极性较弱的聚醚类药物如拉沙洛西、马杜梅素、盐霉素等无法洗脱下来。故选择采用甲醇和乙睛的混合溶剂作为有机相。当甲醇和乙睛的比例为50:50时,各药物的分离度与保留时间较为合适。本研究的大部分目标药物采用ESI+模式进行检测,加入甲酸可以有效改善峰形,提高质子化能力,增强响应。但部分目标化合物如米尔贝肟、三氯苯达唑、莫西克丁、莫奈太尔、癸氧喹酯、盐霉素、甲基盐霉素等仍然出现不同程度的拖尾现象。加入甲酸铵,甲酸铵溶液中的NH4+可竞争性地与色谱柱中的硅羟基结合,从而减少色谱峰的拖尾现象[27]。经实验比对,最终采用10 mmol/L甲酸铵(含0.1%甲酸)水溶液-乙腈:甲醇(50:50)作为流动相,能够最大程度地兼顾全部目标化合物的峰形与响应。优化后得到的30种抗寄生虫类药物的总离子流色谱图见图1。
![]() 图 1 30种抗寄生虫药物总离子流色谱图(10 μg/L)注:图中1~30分别对应表1中1~30化合物。Figure 1. TIC chromatogram of the 30 antiparasitic drugs (10 μg/L)
图 1 30种抗寄生虫药物总离子流色谱图(10 μg/L)注:图中1~30分别对应表1中1~30化合物。Figure 1. TIC chromatogram of the 30 antiparasitic drugs (10 μg/L)2.3 提取溶剂的选择
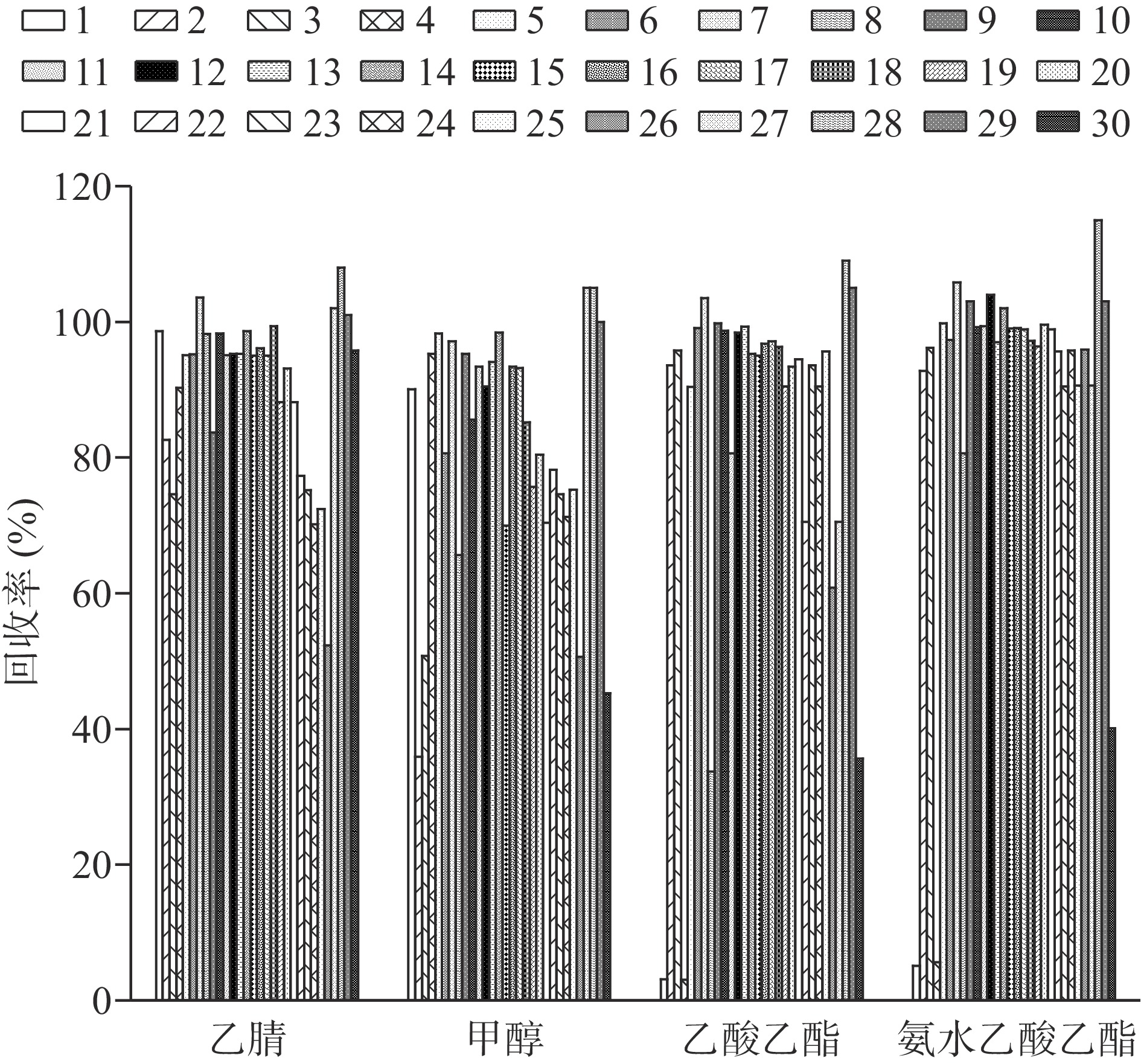
由于本研究涉及的药物种类较多,且各类药物性质差异较大。本研究选择了研究对象中具有代表性的4 种动物源性食品基质:猪肉、鱼肉、鸡蛋、牛奶,采用空白添加试验比较了乙腈、甲醇、乙酸乙酯、1%氨水乙酸乙酯的提取效果,添加水平为10 μg/kg。结果表明乙睛对大部分药物的回收率较好,尤其是对于极性较强的氨丙啉、常山酮、地昔尼尔、罗硝唑等化合物的提取效率明显优于其他提取溶剂,且乙腈沉淀蛋白效果较好,提取液比较清亮,杂质含量少。而1%氨水乙酸乙酯对聚醚类等极性较弱药物的回收率明显优于乙腈、甲醇。对氨丙啉、双咪苯脲、氯氰碘柳胺和部分聚醚类抗生素,乙腈和1%氨水乙酸乙酯表现出了互补的优势,图2为猪肉空白样品添加实验结果。为避免氨水对其他药物提取效率的影响,最终选择先用乙腈提取,再用1%氨水乙酸乙酯提取的方式进行复合提取。
2.4 净化方式的优化
本研究采用 QuEChERS 净化方式,常用的QuEChERS 净化剂有N-丙基乙二胺(PSA)、十八烷基键合硅胶(C18)、石墨碳化黑(GCB)、无水硫酸镁等。C18 能够去除脂肪、蛋白质、矿物质等化合物,石墨化碳黑(GCB)的作用是去除色素和甾醇类干扰,PSA 可以去除有机酸、色素、金属离子和酚类化合物,无水硫酸镁则主要利用其盐析和除水作用[28]。本研究对 C18、PSA、GCB以及无水硫酸镁的净化效果进行了考察。分别仅添加其中一种净化剂50 mg于5 mL空白(猪肉、鱼肉、鸡蛋、牛奶)添加提取液中进行净化。实验结果表明GCB对大多数强极性及中等极性化合物有较强的吸附作用,大部分化合物回收率低于30%;C18、PSA未发现明显的吸附现象。因此本研究选用C18、PSA以及无水硫酸镁作为净化剂。并对净化剂的用量进行考察,当无水硫酸镁为 200 mg,C18为 100 mg,PSA为 100 mg时,各目标物在猪肉、鱼肉、鸡蛋、牛奶基质中回收率和净化效果均为最优。
2.5 滤头和复溶液的选择
将不同乙腈比例的水溶液配制的标准品溶液分别过尼龙滤膜和PTFE滤膜后进行测定,当乙腈比例低于40%时,尼龙滤膜和PTFE滤膜都对多种弱极性化合物如聚醚类化合物有明显的吸附现象。而当乙腈比例大于40%,PTFE滤膜不再吸附任何目标化合物,但尼龙滤膜对奥芬达唑、常山酮、乙氧酰胺苯甲酯、芬苯达唑、拉沙洛西、硝唑尼特、氯氰碘柳胺仍存在不同程度的吸附,因此选择采用PTFE滤膜。测定不同比例乙腈水配制的标准溶液,结果表明当乙腈比例介于20%~60%时,各化合物的响应最优,当乙腈比例>70%后多数化合物响应有所下降。因此选择 50%乙腈水溶液作为样品复溶液,采用PTFE滤膜。
2.6 基质效应的评价
基质效应(matrix effect,ME)是由于待测液中的杂质和目标化合物在离子源端竞争离子化导致目标化合物的响应增强或者抑制的效应[10]。计算公式为 ME(%)=(基质匹配标准溶液曲线斜率/溶剂标准溶液曲线斜率‒1)×100%。当ME为正值时表示基质增强,反之则为基质抑制,绝对值越大则表示基质效应越强。本研究对猪肉、草鱼、鸡蛋和牛奶进行了基质效应评估,具体结果见表3、4。结果显示,猪肉基质效应介于−24.3%~19.0%;鱼肉基质效应介于−22.7%~4.39%;鸡蛋基质效介于−17.3%~15.0%;牛奶基质效介于−22.4%~18.2%,每种基质均出现部分化合物基质效应大于10%。因此本研究采用基质匹配曲线外标法定量。
表 3 猪肉和草鱼在不同加标水平下30种抗寄生虫类药物的加标回收率与精密度(n=6)Table 3. Recovery and precision of 30 antiparasitic drugs in pork and grass carp at different labeling levels (n=6)化合物 加标水平
(μg/kg)猪肉 草鱼 回收率(%) RSD(%) ME(%) 回收率(%) RSD(%) ME(%) 氨丙啉 2.00,5.00,10.0 75.6,88.5,88.4 6.1,3.5,5.7 −13.6 80.1,85.5,82.4 3.8,5.6,7.8 −15.2 地西尼尔 2.00,5.00,10.0 82.9,92.5,93.4 5.2,3.2,0.78 −19.3 83.0,93.5,93.2 3.5,4.4,2.7 −19.4 罗硝唑 2.00,5.00,10.0 85.4,92.0,95.4 4.3,3.2,4.2 −23.6 86.6,91.0,96.0 4.2,1.5,2.9 −18.7 双咪苯脲 2.00,5.00,10.0 71.3,73.5,72.4 8.0,4.9,1.7 19.0 75.5,78.0,79.0 7.6,5.1,3.2 1.98 左旋咪唑 1.00,2.50,5.00 87.3,97.5,104 4.7,3.3,3.5 −11.2 88.6,97.0,96.6 4.4,2.6,1.9 −17.8 噻苯达唑 0.400,1.00,2.00 92.8,96.5,100 2.6,2.6,1.9 −24.3 91.1,96.0,103 2.7,2.1,1.3 −21.1 奥芬达唑 2.00,5.00,10.0 105,103,105 3.7,4.7,3.8 15.0 102,103,99.6 1.3,2.7,3.3 −2.81 常山酮 2.00,5.00,10.0 82.1,90.0,97.8 7.2,2.9,4.2 −13.0 84.6,96.0,95.2 6.9,2.3,1.1 4.39 乙氧酰胺苯甲酯 0.400,1.00,2.00 95.3,100,106 5.0,3.1,1.9 −10.6 91.1,97.0,104 5.1,2.6,3.4 1.66 奥苯达唑 0.0400,0.100,0.200 90.1,92.5,95.4 3.6,3.9,3.0 −14.7 90.0,88.0,97.6 3.7,3.8,3.4 2.72 甲苯达唑 0.400,1.00,2.00 102,98.5,98.0 3.8,4.6,4.9 −10.1 98.0,98.0,99.4 3.6,3.4,1.6 2.95 氟苯达唑 0.400,1.00,2.00 100,95.0,96.4 3.4,3.6,1.7 −23.3 98.0,98.0,101 1.2,0.84,1.3 −2.96 阿苯达唑 0.200,0.500,1.00 89.0,91.0,94.2 3.4,4.5,3.5 −12.5 92.0,93.5,98.8 2.6,4.3,2.4 1.91 吡喹酮 2.00,5.00,10.0 97.0,93.0,99.2 4.3,3.7,4.5 −7.20 95.7,94.5,104 2.6,2.7,1.8 −8.36 氯苯胍 2.00,5.00,10.0 76.2,82.0,81.2 4.4,6.9,6.5 −14.3 75.1,80.5,82.6 5.5,3.1,2.4 −19.3 芬苯达唑 0.200,0.500,1.00 86.7,87.5,91.8 5.1,4.5,5.4 −8.70 85.1,86.5,89.8 1.6,2.6,0.89 −13.5 非班太尔 0.400,1.00,2.00 103,98.5,99.2 6.7,4.5,5.3 −9.50 97.2,103,103 2.1,3.6,2.7 −22.4 三氯苯达唑 1.00,2.50,5.00 84.2,82.5,89.4 5.4,6.8,4.3 −8.70 83.3,83.5,90.6 2.6,2.4,1.9 −22.7 癸氧喹酯 1.00,2.50,5.00 86.4,84.5,82.6 6.3,5.7,6.0 −15.4 90.1,93.5,99.2 3.3,2.1,2.8 −17.5 莫昔克丁 20.0,50.0,100 80.8,73.0,72.6 6.4,5.4,5.7 −24.1 75.3,75.0,73.8 5.0,2.6,3.0 −20.8 米尔贝肟 20.0,50.0,100 70.2,73.0,75.2 5.1,4.2,5.5 −17.6 72.2,75.5,72.6 4.4,2.3,2.9 −15.4 莫能霉素 2.00,5.00,10.0 78.0,91.0,87.6 8.1,4.1,7.3 −18.3 77.7,90.0,88.6 5.6,4.2,4.6 −12.1 拉沙洛西 2.00,5.00,10.0 70.9,72.5,72.2 2.4,3.4,3.6 −20.0 72.5,77.0,74.2 2.8,1.3,2.6 −19.0 盐霉素 2.00,5.00,10.0 72.1,75.0,78.8 5.1,2.9,2.5 −22.2 72.6,74.5,74.2 3.0,2.5,2.9 −15.0 马杜霉素 2.00,5.00,10.0 75.3,74.0,73.4 3.7,4.3,6.5 −19.6 76.2,79.0,75.8 3.1,2.7,2.3 −1.83 甲基盐霉素 0.400,1.00,2.00 77.8,71.0,83.2 7.7,7.9,5.1 −12.4 80.3,83.5,88.4 6.9,5.3,4.7 −14.8 硝碘酚腈 2.00,5.00,10.0 72.6,105,89.8 6.4,2.7,4.7 11.0 73.9,92.0,89.4 5.3,1.6,3.3 −21.1 硝唑尼特 2.00,5.00,10.0 110,108,109 5.9,5.5,4.8 12.0 106,105,105 2.9,3.1,2.6 −9.19 莫奈太尔 2.00,5.00,10.0 98.3,104,106 6.3,4.2,8.0 9.00 97.4,98.0,103 6.2,54,1.3 −6.59 氯氰碘柳胺 2.00,5.00,10.0 75.9,81.5,87.0 6.8,6.7,5.7 −7.90 74.6,78.0,88.4 5.6,2.3,5.3 −15.5 2.7 方法学验证
2.7.1 线性范围、检出限
选取不含目标化合物的空白猪肉样品,用 1.2.2 的前处理方法,得到空白基质提取液,制备基质标准系列溶液,上机测定。以定量离子对的峰面积作为Y轴,质量浓度(μg/L)作为X轴绘制标准曲线。中间液浓度、线性范围浓度、线性回归方程、检出限、定量限见表1。从表1可以看出,在各自的线性范围内30种抗寄生虫类药物线性关系较好,相关系数(r2)>0.99。此外,分别以空白猪猪肉、草鱼、鸡蛋和牛奶为基质,进行加标回收试验,以3倍信噪比和10倍信噪比确定检出限和定量限。30种化合物在不同基质中的检出限在0.001~0.3 μg/kg之间,定量限在0.004~1 μg/kg之间(表1),均低于文献检出限[10,13,19,28−30]。
2.7.2 准确度与精密度
在优化后的实验条件下,分别在不含目标物的猪肉、草鱼、鸡蛋、牛奶样品中做3个添加水平的加标回收试验,每个水平做6个平行,回收率和精密度结果见表3、4。在3个不同添加水平下,30种抗寄生虫药物的加标回收率为70.1%~111%,相对标准偏差(RSD)为0.10%~9.1%,表明方法的准确度和精密度均较好,适用于动物源性食品中抗寄生虫药物残留的定性定量分析。
表 4 鸡蛋和牛奶在不同加标水平下30种抗寄生虫类药物的加标回收率与精密度(n=6)Table 4. Recovery and precision of 30 antiparasitic drugs in egg and milk at different labeling levels (n=6)化合物 加标水平
(μg/kg)鸡蛋 牛奶 回收率(%) RSD(%) ME(%) 回收率(%) RSD(%) ME(%) 氨丙啉 2.00,5.00,10.0 91.4,84.0,98.6 7.2,4.9,6.0 −11.0 88.0,89.2,88.5 0.12,0.33,0.19 −18.6 地西尼尔 2.00,5.00,10.0 90.6,108,107 4.6,6.7,6.3 −13.0 93.9,03,102 6.4,3.5,3.4 −18.7 罗硝唑 2.00,5.00,10.0 108,106,109 3.9,3.2,3.7 2.00 103,107,100 4.3,1.62.2,1.9 4.1 双咪苯脲 2.00,5.00,10.0 70.6,75.5,75.6 4.8,7.2,2.2 7.00 76.2,80.7,74.0 0.45,1.8,3.5 17.9 左旋咪唑 1.00,2.50,5.00 106,107,105 5.3,5.3,5.7 −2.40 104,95.3,89.0 2.2,3.4,1.5 −6.5 噻苯达唑 0.400,1.00,2.00 105,106,104 6.2,3.0,5.3 −6.40 102,99.2,89.4 4.2,1.9,0.63 −11.0 奥芬达唑 2.00,5.00,10.0 104,103,106 5.2,2.4,4.5 −1.60 109,107,97.9 1.8,0.18,1.1 18.2 常山酮 2.00,5.00,10.0 72.2,71.5,73.9 7.8,7.3,6.9 −5.70 109,109,96.1 0.79,3.5,1.0 9.88 乙氧酰胺苯甲酯 0.400,1.00,2.00 106,103,106 2.7,3.4,5.0 3.00 109,109,102 0.95,2.1,0.12 −1.95 奥苯达唑 0.0400,0.100,0.200 99.2,101,103 4.5,4.4,6.9 −1.80 100,97.2,92.6 0.20,0.43,1.6 −13.9 甲苯达唑 0.400,1.00,2.00 104,98.8,99.9 2.4,2.9,6.5 −1.30 104,104,97.2 0.70,1.8,0.59 7.53 氟苯达唑 0.400,1.00,2.00 99.6,96.4.,96.7 3.9,2.9,5.7 1.00 107,107,96.0 0.33,0.54,0.36 12.9 阿苯达唑 0.200,0.500,1.00 101,98.0,96.9 3.2,5.0,5.1 −3.30 92.1,87.1,83.4 0.40,2.9,0.10 −21.0 吡喹酮 2.00,5.00,10.0 102,108,106 4.0,5.2,5.1 6.00 93.3,93.4,89.1 0.80,6.6,2.4 −20.8 氯苯胍 2.00,5.00,10.0 89.4,91.7,84.0 3.8,4.4,7.2 −10.0 91.3,81.2,84.6 6.5,0.74,5.8 −22.4 芬苯达唑 0.200,0.500,1.00 90.5,95.6,96.4 4.3,6.4,7.1 −5.50 98.1,101,93.8 5.5,1.6,0.69 −12.8 非班太尔 0.400,1.00,2.00 80.7,99.0,92.1 5.5,7.6,7.1 −7.30 84.4,90.6,88.1 1.8,6.7,2.9 −19.3 三氯苯达唑 1.00,2.50,5.00 75.4,70.1,73.2 6.7,6.6,6.5 −2.30 92.5,87.9,88.8 1.4,1.7,20 −15.9 癸氧喹酯 1.00,2.50,5.00 72.3,73.0,72.4 2.4,2.6,4.4 −15.1 103,108,101 3.2,7.0,3.6 −11.5 莫昔克丁 20.0,50.0,100 81.4,83.8,87.4 3.4,4.0,6.5 15.0 84.1,82.8,85.7 5.6,4.7,6.6 8.73 米尔贝肟 20.0,50.0,100 72.6,73.9,85.0 6.2,5.3,5.3 4.00 82.4,79.8,82.5 2.1,5.2,2.3 10.1 莫能霉素 2.00,5.00,10.0 75.6,81.5,81.2 9.1,4.0,5.5 −17.3 97.0,87.7,83.6 6.6,1.5,0.22 13.1 拉沙洛西 2.00,5.00,10.0 87.0,89.3,86.7 5.2,4.9,6.1 −8.30 73.3,80.3,78.3 0.40,4.6,4.2 −1.72 盐霉素 2.00,5.00,10.0 87.3,77.1,82.0 5.4,4.4,5.0 −15.8 75.1,74.0,76.4 3.8,4.2,1.3 −15.8 马杜霉素 2.00,5.00,10.0 89.6,95.4,98.0 4.6,1.3,2.8 9.00 82.2,71.8,78.9 6.7,3.7,2.5 −3.85 甲基盐霉素 0.400,1.00,2.00 85.1,79.7,74.4 2.8,5.1,6.7 14.0 82.1,72.1,72.4 8.2,3.5,1.5 −14.4 硝碘酚腈 2.00,5.00,10.0 89.6,92.4,96.9 3.3,7.1,1.1 1.00 101,111,95.9 0.90,0.73,0.42 1.05 硝唑尼特 2.00,5.00,10.0 103,108,108 5.3,6.8,2.3 6.00 106,109,107 3.2,2.9,1.3 2.42 莫奈太尔 2.00,5.00,10.0 84.5,97.5,99.4 7.1,5.4,1.8 2.00 99.5,109,96.1 4.3,2.5,1.2 3.20 氯氰碘柳胺 2.00,5.00,10.0 72.3,74.0,73.4 1.9,1.4,1.3 −2.80 96.3,102,99.2 2.2,1.3,1.0 −16.7 2.8 实际样品测定
本研究采用新建立的方法对市场上购买的猪肉、鸡鸭肉、牛羊肉、鱼肉、鸡蛋、牛奶共计150批次样品进行检测分析。检出了噻苯达唑、阿苯达唑、癸氧喹酯、莫能霉素、马杜霉素、甲基盐霉素等,共计29批次。8批次检出阿苯达唑,含量达到0.345~10.1 µg/kg;7批次检出癸氧喹酯,含量达到0.893~164 µg/kg;7批次检出马杜霉素,含量达到0.500~52.0 µg/kg;4批次检出莫能霉素,含量达到0.410~1.63 µg/kg;1批次检出噻苯达唑,含量为1.72 µg/kg;2批次检出甲基盐霉素,含量为0.545 µg/kg和0.638 µg/kg;其中包含16批次鸡肉,2批次猪肉,1批次鸭肉,6批次鸡蛋,整体检出率为16.7%,说明动物源食品中中确实有存在抗寄生虫类药物兽药残留的现象。
3. 结论
本文通过对质谱、色谱条件和前处理方法的优化,建立了QuEChERS-超高效液相色谱-串联质谱法测定动物源性食品中30种抗寄生虫类药物残留的方法。应用该方法检测了150批次市售样品,整体检出率为16.7%,表明目前市场上确实存在抗寄生虫类药物兽药残留的现象。本方法具有操作简单,试剂用量少、分析时间短、测定结果稳定、高通量等优点,可为畜禽肉、水产品、鸡蛋、牛奶中抗寄生虫药物残留快速筛查和定性定量分析提供技术支撑,有助于动物源性食品中抗寄生虫药物残留的市场监管。
-
图 1 30种抗寄生虫药物总离子流色谱图(10 μg/L)
注:图中1~30分别对应表1中1~30化合物。
Figure 1. TIC chromatogram of the 30 antiparasitic drugs (10 μg/L)
表 1 30种抗寄生虫类药物浓度、线性方程、决定系数(r2)检出限及定量限
Table 1 Concentration, regression equations, coefficient of determination (r2), LODs, LOQs of the 30 antiparasitic drugs
化合物 中间液浓度(mg/L) 线性范围(μg/L) 线性回归方程 决定系数(r2) 检出限(μg/kg) 定量限(μg/kg) 氨丙啉 1.00 1.00~50.0 Y=118986X+298045 0.9983 0.02 0.06 地西尼尔 1.00 1.00~50.0 Y=4623.8X+12084 0.9995 0.2 0.8 罗硝唑 1.00 1.00~50.0 Y=31112X+66997 0.9999 0.02 0.06 双咪苯脲 1.00 1.00~50.0 Y=73074X+147955 0.9986 0.1 0.4 左旋咪唑 0.500 0.500~25.0 Y=43378X+70131 0.9970 0.03 0.1 噻苯达唑 0.200 0.200~10.0 Y=71640X+18772 0.9997 0.02 0.06 奥芬达唑 1.00 1.00~50.0 Y=27873X+90090 0.9964 0.04 0.1 常山酮 1.00 1.00~50.0 Y=8064.5X+18747 0.9990 0.04 0.1 乙氧酰胺苯甲酯 0.200 0.200~10.0 Y=91253X+52608 0.9985 0.004 0.01 奥苯达唑 0.0200 0.0200~1.00 Y=1E+06X+46316 0.9992 0.001 0.004 甲苯达唑 0.200 0.200~10.0 Y=167434X+76679 0.9996 0.01 0.04 氟苯达唑 0.200 0.200~10.0 Y=115535X+46360 0.9991 0.01 0.02 阿苯达唑 0.10 0.100~5.00 Y=391021X+113444 0.9979 0.003 0.01 吡喹酮 1.00 1.00~50.0 Y=50795X+95961 0.9996 0.05 0.2 氯苯胍 1.00 1.00~50.0 Y=28992X+65410 0.9980 0.1 0.4 芬苯达唑 0.100 0.100~5.00 Y=263625X+69199 0.9980 0.003 0.01 非班太尔 0.200 0.200~10.0 Y=83622X+29374 0.9991 0.004 0.01 三氯苯达唑 0.500 0.500~25.0 Y=43264X+37943 0.9992 0.02 0.05 癸氧喹酯 0.500 0.500~25.0 Y=60166X+41980 0.9980 0.01 0.03 莫昔克丁 10.0 10.0~500 Y=419.68X+5611.9 0.9993 0.1 0.4 米尔贝肟 10.0 10.0~500 Y=5987.1X+121343 0.9986 0.3 1 莫能霉素 1.00 1.00~50.0 Y=6001.4X−47.666 0.9999 0.02 0.07 拉沙洛西 1.00 1.00~50.0 Y=57948X+128990 0.9990 0.07 0.2 盐霉素 1.00 1.00~50.0 Y=13199X+29194 0.9994 0.04 0.1 马杜霉素 1.00 1.00~50.0 Y=36028X+54891 0.9997 0.02 0.05 甲基盐霉素 0.200 0.200~10.0 Y=126919X+53423 0.9994 0.003 0.01 硝碘酚腈 1.00 1.00~50.0 Y=4583.5X+15315 0.9987 0.05 0.2 硝唑尼特 1.00 1.00~50.0 Y=24664X+3629.8 0.9999 0.04 0.1 莫奈太尔 1.00 1.00~50.0 Y=4606.2X+14766 0.9978 0.02 0.07 氯氰碘柳胺 1.00 1.00~50.0 Y=6087.2X+63425 0.9984 0.08 0.3 表 2 目标化合物的质谱参数
Table 2 Mass parameters of analytes mass parameters of analytes
序号 化合物名称 保留时间(min) 母离子(m/z) 子离子(m/z) 四级杆1电压(V) 碰撞电压(V) 四级杆3电压(V) ESI模式 1 氨丙啉 1.50 243.2 150.2*/94.2 22/22 13/11 19/16 + 2 地昔尼尔 2.27 191.1 150.1*/109.2 27/12 20/26 30/22 + 3 罗硝唑 2.93 201.1 140.1*/55.1 14/13 13/23 14/21 + 4 双咪苯脲 3.29 349.2 188.2*/162.2 12/12 28/24 21/18 + 5 左旋咪唑 3.50 205.0 178.2*/91.2 30/30 20/39 23/18 + 6 噻苯达唑 4.26 201.9 175.2*/131.2 30/29 24/31 20/14 + 7 奥芬达唑 5.46 316.1 159.1*/284.0 21/20 40/17 29/21 + 8 常山酮 5.53 415.6 120.2*/138.3 26/25 21/20 25/27 + 9 乙氧酰胺苯甲酯 5.56 237.8 206.2*/136.2 15/23 10/26 23/15 + 10 奥苯达唑 5.98 249.8 218.2*/176.2 30/16 18/26 24/20 + 11 甲苯咪唑 6.30 296.1 264.1*/105.1 10/14 24/34 28/20 + 12 氟苯达唑 6.50 314.1 282.1*/123.2 14/15 24/36 28/23 + 13 阿苯达唑 6.87 266.1 234.1*/191.0 12/12 20/33 16/19 + 14 吡喹酮 7.18 312.8 203.2*/174.2 20/20 17/29 23/19 + 15 氯苯胍 7.22 333.9 155.2*/138.2 20/20 21/26 29/27 + 16 芬苯达唑 7.32 299.9 268.1*/159.2 15/30 23/35 21/30 + 17 非班太尔 7.76 446.6 383.1*/415.1 28/30 20/13 28/30 + 18 三氯苯达唑 8.31 358.8 274.1*/198.1 22/23 34/27 30/22 + 19 癸氧喹酯 9.27 418.2 372.2*/204.1 20/20 25/44 20/21 + 20 莫西克丁 9.84 640.1 199.1*/528.2 22/40 27/11 23/40 + 21 米尔贝肟 9.92 556.1 167.2*/538.3 34/34 24/18 30/40 + 22 莫能霉素 9.95 693.6 461.3*/479.3 40/40 54/55 24/25 + 23 拉沙洛西 10.1 613.4 377.3*/359.3 28/20 39/37 28/27 + 24 盐霉素 10.1 773.6 431.3*/531.3 26/26 51/44 23/40 + 25 马杜霉素 10.3 935.5 877.5*/895.6 26/20 34/54 30/36 + 26 甲基盐霉素 10.6 787.6 431.2*/531.4 30/30 45/45 20/30 + 27 硝碘酚腈 5.57 288.8 127.1*/162.2 13/18 25/22 12/10 − 28 硝唑尼特 7.09 264.0 217.1*/144.2 24/30 14/17 23/28 − 29 莫奈太尔 8.13 471.9 186.2*/166.3 22/22 23/45 12/30 − 30 氯氰碘柳胺 9.10 660.9 315.1*/344.9 28/28 33/35 21/11 − 注:*为定量离子。 表 3 猪肉和草鱼在不同加标水平下30种抗寄生虫类药物的加标回收率与精密度(n=6)
Table 3 Recovery and precision of 30 antiparasitic drugs in pork and grass carp at different labeling levels (n=6)
化合物 加标水平
(μg/kg)猪肉 草鱼 回收率(%) RSD(%) ME(%) 回收率(%) RSD(%) ME(%) 氨丙啉 2.00,5.00,10.0 75.6,88.5,88.4 6.1,3.5,5.7 −13.6 80.1,85.5,82.4 3.8,5.6,7.8 −15.2 地西尼尔 2.00,5.00,10.0 82.9,92.5,93.4 5.2,3.2,0.78 −19.3 83.0,93.5,93.2 3.5,4.4,2.7 −19.4 罗硝唑 2.00,5.00,10.0 85.4,92.0,95.4 4.3,3.2,4.2 −23.6 86.6,91.0,96.0 4.2,1.5,2.9 −18.7 双咪苯脲 2.00,5.00,10.0 71.3,73.5,72.4 8.0,4.9,1.7 19.0 75.5,78.0,79.0 7.6,5.1,3.2 1.98 左旋咪唑 1.00,2.50,5.00 87.3,97.5,104 4.7,3.3,3.5 −11.2 88.6,97.0,96.6 4.4,2.6,1.9 −17.8 噻苯达唑 0.400,1.00,2.00 92.8,96.5,100 2.6,2.6,1.9 −24.3 91.1,96.0,103 2.7,2.1,1.3 −21.1 奥芬达唑 2.00,5.00,10.0 105,103,105 3.7,4.7,3.8 15.0 102,103,99.6 1.3,2.7,3.3 −2.81 常山酮 2.00,5.00,10.0 82.1,90.0,97.8 7.2,2.9,4.2 −13.0 84.6,96.0,95.2 6.9,2.3,1.1 4.39 乙氧酰胺苯甲酯 0.400,1.00,2.00 95.3,100,106 5.0,3.1,1.9 −10.6 91.1,97.0,104 5.1,2.6,3.4 1.66 奥苯达唑 0.0400,0.100,0.200 90.1,92.5,95.4 3.6,3.9,3.0 −14.7 90.0,88.0,97.6 3.7,3.8,3.4 2.72 甲苯达唑 0.400,1.00,2.00 102,98.5,98.0 3.8,4.6,4.9 −10.1 98.0,98.0,99.4 3.6,3.4,1.6 2.95 氟苯达唑 0.400,1.00,2.00 100,95.0,96.4 3.4,3.6,1.7 −23.3 98.0,98.0,101 1.2,0.84,1.3 −2.96 阿苯达唑 0.200,0.500,1.00 89.0,91.0,94.2 3.4,4.5,3.5 −12.5 92.0,93.5,98.8 2.6,4.3,2.4 1.91 吡喹酮 2.00,5.00,10.0 97.0,93.0,99.2 4.3,3.7,4.5 −7.20 95.7,94.5,104 2.6,2.7,1.8 −8.36 氯苯胍 2.00,5.00,10.0 76.2,82.0,81.2 4.4,6.9,6.5 −14.3 75.1,80.5,82.6 5.5,3.1,2.4 −19.3 芬苯达唑 0.200,0.500,1.00 86.7,87.5,91.8 5.1,4.5,5.4 −8.70 85.1,86.5,89.8 1.6,2.6,0.89 −13.5 非班太尔 0.400,1.00,2.00 103,98.5,99.2 6.7,4.5,5.3 −9.50 97.2,103,103 2.1,3.6,2.7 −22.4 三氯苯达唑 1.00,2.50,5.00 84.2,82.5,89.4 5.4,6.8,4.3 −8.70 83.3,83.5,90.6 2.6,2.4,1.9 −22.7 癸氧喹酯 1.00,2.50,5.00 86.4,84.5,82.6 6.3,5.7,6.0 −15.4 90.1,93.5,99.2 3.3,2.1,2.8 −17.5 莫昔克丁 20.0,50.0,100 80.8,73.0,72.6 6.4,5.4,5.7 −24.1 75.3,75.0,73.8 5.0,2.6,3.0 −20.8 米尔贝肟 20.0,50.0,100 70.2,73.0,75.2 5.1,4.2,5.5 −17.6 72.2,75.5,72.6 4.4,2.3,2.9 −15.4 莫能霉素 2.00,5.00,10.0 78.0,91.0,87.6 8.1,4.1,7.3 −18.3 77.7,90.0,88.6 5.6,4.2,4.6 −12.1 拉沙洛西 2.00,5.00,10.0 70.9,72.5,72.2 2.4,3.4,3.6 −20.0 72.5,77.0,74.2 2.8,1.3,2.6 −19.0 盐霉素 2.00,5.00,10.0 72.1,75.0,78.8 5.1,2.9,2.5 −22.2 72.6,74.5,74.2 3.0,2.5,2.9 −15.0 马杜霉素 2.00,5.00,10.0 75.3,74.0,73.4 3.7,4.3,6.5 −19.6 76.2,79.0,75.8 3.1,2.7,2.3 −1.83 甲基盐霉素 0.400,1.00,2.00 77.8,71.0,83.2 7.7,7.9,5.1 −12.4 80.3,83.5,88.4 6.9,5.3,4.7 −14.8 硝碘酚腈 2.00,5.00,10.0 72.6,105,89.8 6.4,2.7,4.7 11.0 73.9,92.0,89.4 5.3,1.6,3.3 −21.1 硝唑尼特 2.00,5.00,10.0 110,108,109 5.9,5.5,4.8 12.0 106,105,105 2.9,3.1,2.6 −9.19 莫奈太尔 2.00,5.00,10.0 98.3,104,106 6.3,4.2,8.0 9.00 97.4,98.0,103 6.2,54,1.3 −6.59 氯氰碘柳胺 2.00,5.00,10.0 75.9,81.5,87.0 6.8,6.7,5.7 −7.90 74.6,78.0,88.4 5.6,2.3,5.3 −15.5 表 4 鸡蛋和牛奶在不同加标水平下30种抗寄生虫类药物的加标回收率与精密度(n=6)
Table 4 Recovery and precision of 30 antiparasitic drugs in egg and milk at different labeling levels (n=6)
化合物 加标水平
(μg/kg)鸡蛋 牛奶 回收率(%) RSD(%) ME(%) 回收率(%) RSD(%) ME(%) 氨丙啉 2.00,5.00,10.0 91.4,84.0,98.6 7.2,4.9,6.0 −11.0 88.0,89.2,88.5 0.12,0.33,0.19 −18.6 地西尼尔 2.00,5.00,10.0 90.6,108,107 4.6,6.7,6.3 −13.0 93.9,03,102 6.4,3.5,3.4 −18.7 罗硝唑 2.00,5.00,10.0 108,106,109 3.9,3.2,3.7 2.00 103,107,100 4.3,1.62.2,1.9 4.1 双咪苯脲 2.00,5.00,10.0 70.6,75.5,75.6 4.8,7.2,2.2 7.00 76.2,80.7,74.0 0.45,1.8,3.5 17.9 左旋咪唑 1.00,2.50,5.00 106,107,105 5.3,5.3,5.7 −2.40 104,95.3,89.0 2.2,3.4,1.5 −6.5 噻苯达唑 0.400,1.00,2.00 105,106,104 6.2,3.0,5.3 −6.40 102,99.2,89.4 4.2,1.9,0.63 −11.0 奥芬达唑 2.00,5.00,10.0 104,103,106 5.2,2.4,4.5 −1.60 109,107,97.9 1.8,0.18,1.1 18.2 常山酮 2.00,5.00,10.0 72.2,71.5,73.9 7.8,7.3,6.9 −5.70 109,109,96.1 0.79,3.5,1.0 9.88 乙氧酰胺苯甲酯 0.400,1.00,2.00 106,103,106 2.7,3.4,5.0 3.00 109,109,102 0.95,2.1,0.12 −1.95 奥苯达唑 0.0400,0.100,0.200 99.2,101,103 4.5,4.4,6.9 −1.80 100,97.2,92.6 0.20,0.43,1.6 −13.9 甲苯达唑 0.400,1.00,2.00 104,98.8,99.9 2.4,2.9,6.5 −1.30 104,104,97.2 0.70,1.8,0.59 7.53 氟苯达唑 0.400,1.00,2.00 99.6,96.4.,96.7 3.9,2.9,5.7 1.00 107,107,96.0 0.33,0.54,0.36 12.9 阿苯达唑 0.200,0.500,1.00 101,98.0,96.9 3.2,5.0,5.1 −3.30 92.1,87.1,83.4 0.40,2.9,0.10 −21.0 吡喹酮 2.00,5.00,10.0 102,108,106 4.0,5.2,5.1 6.00 93.3,93.4,89.1 0.80,6.6,2.4 −20.8 氯苯胍 2.00,5.00,10.0 89.4,91.7,84.0 3.8,4.4,7.2 −10.0 91.3,81.2,84.6 6.5,0.74,5.8 −22.4 芬苯达唑 0.200,0.500,1.00 90.5,95.6,96.4 4.3,6.4,7.1 −5.50 98.1,101,93.8 5.5,1.6,0.69 −12.8 非班太尔 0.400,1.00,2.00 80.7,99.0,92.1 5.5,7.6,7.1 −7.30 84.4,90.6,88.1 1.8,6.7,2.9 −19.3 三氯苯达唑 1.00,2.50,5.00 75.4,70.1,73.2 6.7,6.6,6.5 −2.30 92.5,87.9,88.8 1.4,1.7,20 −15.9 癸氧喹酯 1.00,2.50,5.00 72.3,73.0,72.4 2.4,2.6,4.4 −15.1 103,108,101 3.2,7.0,3.6 −11.5 莫昔克丁 20.0,50.0,100 81.4,83.8,87.4 3.4,4.0,6.5 15.0 84.1,82.8,85.7 5.6,4.7,6.6 8.73 米尔贝肟 20.0,50.0,100 72.6,73.9,85.0 6.2,5.3,5.3 4.00 82.4,79.8,82.5 2.1,5.2,2.3 10.1 莫能霉素 2.00,5.00,10.0 75.6,81.5,81.2 9.1,4.0,5.5 −17.3 97.0,87.7,83.6 6.6,1.5,0.22 13.1 拉沙洛西 2.00,5.00,10.0 87.0,89.3,86.7 5.2,4.9,6.1 −8.30 73.3,80.3,78.3 0.40,4.6,4.2 −1.72 盐霉素 2.00,5.00,10.0 87.3,77.1,82.0 5.4,4.4,5.0 −15.8 75.1,74.0,76.4 3.8,4.2,1.3 −15.8 马杜霉素 2.00,5.00,10.0 89.6,95.4,98.0 4.6,1.3,2.8 9.00 82.2,71.8,78.9 6.7,3.7,2.5 −3.85 甲基盐霉素 0.400,1.00,2.00 85.1,79.7,74.4 2.8,5.1,6.7 14.0 82.1,72.1,72.4 8.2,3.5,1.5 −14.4 硝碘酚腈 2.00,5.00,10.0 89.6,92.4,96.9 3.3,7.1,1.1 1.00 101,111,95.9 0.90,0.73,0.42 1.05 硝唑尼特 2.00,5.00,10.0 103,108,108 5.3,6.8,2.3 6.00 106,109,107 3.2,2.9,1.3 2.42 莫奈太尔 2.00,5.00,10.0 84.5,97.5,99.4 7.1,5.4,1.8 2.00 99.5,109,96.1 4.3,2.5,1.2 3.20 氯氰碘柳胺 2.00,5.00,10.0 72.3,74.0,73.4 1.9,1.4,1.3 −2.80 96.3,102,99.2 2.2,1.3,1.0 −16.7 -
[1] 陈杖榴. 兽医药理学[M]. 北京:中国农业出版社, 2007:265−298. [CHEN Z L. Veterinary pharmacology[M]. Beijing:China Agricultural Press, 2007:265−298.] CHEN Z L. Veterinary pharmacology[M]. Beijing: China Agricultural Press, 2007: 265−298.
[2] 唐仁勇, 蔡婧, 郭秀兰, 等. 抗寄生虫药物在畜禽产品中的残留危害及安全控制对策[J]. 黑龙江农业科学,2021,43(8):123−128. [TANG R Y, CAI J, GUO X L, et al. The residual hazards and safety control strategies of antiparasitic drugs in livestock and poultry products[J]. Heilongjiang Agricultural Sciences,2021,43(8):123−128.] TANG R Y, CAI J, GUO X L, et al . The residual hazards and safety control strategies of antiparasitic drugs in livestock and poultry products[J]. Heilongjiang Agricultural Sciences,2021 ,43 (8 ):123 −128 .[3] BAYNES R E, DEDONDER K, KISSELL L, et al. Health concerns and management of select veterinary drug residues[J]. Food and Chemical Toxicology,2016,88:112−122. doi: 10.1016/j.fct.2015.12.020
[4] 胡京枝, 尚兵, 刘进玺, 等. 抗球虫药检测技术研究进展[J]. 食品安全质量检测学报,2022,13(9):2825−2833. [HU J Z, SHANG B, LIU J X, et al. Advance of the coccidiostat detection methods[J]. Journal of Food Safety and Quality,2022,13(9):2825−2833.] HU J Z, SHANG B, LIU J X, et al . Advance of the coccidiostat detection methods[J]. Journal of Food Safety and Quality,2022 ,13 (9 ):2825 −2833 .[5] 孙星雅, 李强, 王战辉, 等. 中国与欧盟和美国禽肉、禽蛋中兽药残留限量标准的对比研究[J]. 中国畜牧兽医,2022,49(6):2362−2375. [SUN X Y, LI Q, WANG Z H, et al. Comparative study on veterinary drug residue limit standards for poultry meat and eggs in China, EU and USA[J]. China Animal Husbandry & Veterinary Medicine,2022,49(6):2362−2375.] SUN X Y, LI Q, WANG Z H, et al . Comparative study on veterinary drug residue limit standards for poultry meat and eggs in China, EU and USA[J]. China Animal Husbandry & Veterinary Medicine,2022 ,49 (6 ):2362 −2375 .[6] 中华人民共和国农村农业部, 中华人民共和国国家卫生健康委员会, 国家市场监督管理总局. GB 31650-2019食品中兽药最大残留限量[S]. 北京:中国标准出版社, 2019. [Ministry of agriculture and rural affairs of the People's Republic of China, National Health Commission of the People's Republic of China, State Administration for Market Regulation. GB 31650-2019 Maximum residue limits for veterinary drugs in foods[S]. Beijing:Standards Press of China, 2019.] Ministry of agriculture and rural affairs of the People's Republic of China, National Health Commission of the People's Republic of China, State Administration for Market Regulation. GB 31650-2019 Maximum residue limits for veterinary drugs in foods[S]. Beijing: Standards Press of China, 2019.
[7] 李丹, 吴翠玲, 张聪聪, 等. 亲水作用色谱柱-高效液相色谱法测定鸡蛋中氨丙啉的残留量[J]. 食品安全质量检测学报,2019,10(17):5648−5652. [LI D, WU C L, ZHANG C C, et al. Determination of amprolium residues in egg by hydrop interaction liquid chromatography column-high performance liquid chromatography[J]. Journal of Food Safety & Quality,2019,10(17):5648−5652.] LI D, WU C L, ZHANG C C, et al . Determination of amprolium residues in egg by hydrop interaction liquid chromatography column-high performance liquid chromatography[J]. Journal of Food Safety & Quality,2019 ,10 (17 ):5648 −5652 .[8] 邹游, 邵琳智, 吴映璇. 高效液相色谱法测定鸡组织中苯并咪唑类药物残留标志物[J]. 色谱,2019,37(10):1112−1117. [ZOU Y, SHAO L Z, WU Y X. Determination of benzimidazoles residue markers in chicken tissue by high performance liquid chromatography[J]. Chinese Journal of Chromatography,2019,37(10):1112−1117.] doi: 10.3724/SP.J.1123.2019.03031 ZOU Y, SHAO L Z, WU Y X . Determination of benzimidazoles residue markers in chicken tissue by high performance liquid chromatography[J]. Chinese Journal of Chromatography,2019 ,37 (10 ):1112 −1117 . doi: 10.3724/SP.J.1123.2019.03031[9] 陈瑞, 杨志伟, 朱凤妹, 等. 超高效液相色谱-串联质谱法测定牛奶和奶粉中五种苯并咪唑类药物[J]. 核农学报,2020,34(8):1776−1784. [CHEN R, YANG Z W, ZHU F M, et al. Determination of five benzimidazoles in milk and milk powder by UPLC-MS-MS[J]. Journal of Nuclear Agricultural Sciences,2020,34(8):1776−1784.] CHEN R, YANG Z W, ZHU F M, et al . Determination of five benzimidazoles in milk and milk powder by UPLC-MS-MS[J]. Journal of Nuclear Agricultural Sciences,2020 ,34 (8 ):1776 −1784 .[10] 温海滨, 林洁纯, 叶靖怡, 等. QuEChERS-超高效液相色谱-串联质谱法同时测定水产品中20种苯并咪唑类药物及其代谢物残留[J]. 食品安全质量检测学报,2021,12(18):7214−7221. [WEN H B, LIN J C, YE J Y, et al. Simultaneous determination of 20 kinds of benzimidazoles and their metabolites residues in aquatic products by QuEChERS-ultra performance liquid chromatography-tandem mass spectrometry[J]. Journal of Food Safety and Quality,2021,12(18):7214−7221.] WEN H B, LIN J C, YE J Y, et al . Simultaneous determination of 20 kinds of benzimidazoles and their metabolites residues in aquatic products by QuEChERS-ultra performance liquid chromatography-tandem mass spectrometry[J]. Journal of Food Safety and Quality,2021 ,12 (18 ):7214 −7221 .[11] XU N, DONG J, YANG Y B, et al. Development of a liquid chromatography-tandem mass spectrometry method with modified QuEChERS extraction for the quantification of mebendazole and its metabolites, albendazole and its metabolites, and levamisole in edible tissues of aquatic animals[J]. Food Chemistry,2018,269:442−449. doi: 10.1016/j.foodchem.2018.07.017
[12] 张绍伟, 贾媛媛, 侯晓林. 牛奶中三聚氰胺、环丙氨嗪、地昔尼尔的高效液相色谱-串联质谱检测方法的建立[J]. 北京农学院学报,2018,33(3):61−65. [ZHANG S W, JIA Y Y, HOU X L. Study on the determination of melamine, cyromazine and dicyclanil in milk by HPLC-MS/MS[J]. Journal of Beijing University of Agriculture,2018,33(3):61−65.] ZHANG S W, JIA Y Y, HOU X L . Study on the determination of melamine, cyromazine and dicyclanil in milk by HPLC-MS/MS[J]. Journal of Beijing University of Agriculture,2018 ,33 (3 ):61 −65 .[13] ZHAO X, WANG B, XIE K Z, et al. Development and comparison of HPLC-MS/MS and UPLC-MS/MS methods for determining eight coccidiostats in beef[J]. Journal of Chromatography B,2018,1087-1088:98−107. doi: 10.1016/j.jchromb.2018.04.044
[14] 奚照寿, 赵霞, 袁华根, 等. 超高效液相色谱-串联质谱法检测鸡肌肉中8种抗球虫药物的残留[J]. 中国兽医学报,2018,38(10):1938−1947. [[XI Z S, ZHAO X, YUAN H G, et al. Determination of eight coccidiostats residues in chicken muscle by ultra performance liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Veterinary Science,2018,38(10):1938−1947.] [XI Z S, ZHAO X, YUAN H G, et al . Determination of eight coccidiostats residues in chicken muscle by ultra performance liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Veterinary Science,2018 ,38 (10 ):1938 −1947 .[15] WANG B, LIU J Y, ZHAO X, et al. Determination of eight coccidiostats in eggs by liquid-liquid extraction-solid-phase extraction and liquid chromatography-tandem mass spectrometry[J]. Molecules,2020,25(4):987. doi: 10.3390/molecules25040987
[16] DANIELA H, SOMPHOU S, JENNIFER K. Development and validation of an LC-MS/MS method for the quantification of the anthelmintic drug moxidectin in a volumetric absorptive microsample, blood, and plasma:Application to a pharmacokinetic study of adults infected with Strongyloides stercoralis in Laos[J]. Journal of Chromatogr B,2021,1166:122556. doi: 10.1016/j.jchromb.2021.122556
[17] 吴映璇, 林峰, 陈思敏. 高效液相色谱-串联质谱法测定乳制品中的莫奈太尔及其代谢物[J]. 食品科学,2019,40(10):325−330. [WU Y X, LIN F, CHEN S M. Determination of monepantel and its metabolite residues in dairy products by high performance liquid chromatography-tandem mass spectrometry[J]. Food Science,2019,40(10):325−330.] WU Y X, LIN F, CHEN S M . Determination of monepantel and its metabolite residues in dairy products by high performance liquid chromatography-tandem mass spectrometry[J]. Food Science,2019 ,40 (10 ):325 −330 .[18] 张敏, 王鸽, 马晓冲, 等. 超高效液相色谱-串联质谱法测定牛乳中6种兽药残留[J]. 食品工业科技,2022,43(5):255−261. [ZHANG M, WANG G, MA X C, et al. Determination of 6 kinds of veterinary drug residues in milk by ultra performance liquid chromatography-tandem mass spectrometry[J]. Science and Technology of Food Industry,2022,43(5):255−261.] ZHANG M, WANG G, MA X C, et al . Determination of 6 kinds of veterinary drug residues in milk by ultra performance liquid chromatography-tandem mass spectrometry[J]. Science and Technology of Food Industry,2022 ,43 (5 ):255 −261 .[19] 魏慧敏. 兽用抗寄生虫药物残留高效液相色谱-串联质谱筛选法研究[D]. 武汉:华中农业大学, 2013. [WEI H M. Multi-residues screening of veterinary antiparasite drugs by liquid chromatography tandem mass spectrometry (LC-MS/MS) [D]. Wu Han, Huazhong Agricultural University, 2013.] WEI H M. Multi-residues screening of veterinary antiparasite drugs by liquid chromatography tandem mass spectrometry (LC-MS/MS) [D]. Wu Han, Huazhong Agricultural University, 2013.
[20] 郑幸果, 郭灵安, 赵珊, 等. UPLC-MS/MS法测定动物源性食品中氯苯胍及其代谢物残留[J]. 中国畜牧兽医,2020,47(6):1961−1970. [ZHENG X G, GUO L A, ZHAO S, et al. Determination of robenidine and its metabolites in animal derived food by UPLC-MS/MS[J]. China Animal Husbandry & Veterinary Medicine,2020,47(6):1961−1970.] ZHENG X G, GUO L A, ZHAO S, et al . Determination of robenidine and its metabolites in animal derived food by UPLC-MS/MS[J]. China Animal Husbandry & Veterinary Medicine,2020 ,47 (6 ):1961 −1970 .[21] 孙晓娟, 梁雪燕, 郝祖慧, 等. 鸡组织中氢溴酸常山酮残留的UPLC-MS/MS检测法及其消除规律[J]. 中国农业大学学报,2019,24(3):72−77. [SUN X J, LIANG X Y, HAO Z H, et al. Determination of halofuginone residue and its depletion in chicken tissue by UPLC-MS/MS[J]. Journal of China Agricultural University,2019,24(3):72−77.] SUN X J, LIANG X Y, HAO Z H, et al . Determination of halofuginone residue and its depletion in chicken tissue by UPLC-MS/MS[J]. Journal of China Agricultural University,2019 ,24 (3 ):72 −77 .[22] TANG Y X, YU N, LIU C S, et al. Residue depletion of imidocarb in bovine tissues by UPLC-MS/MS[J]. Animals, 2022, 13(1):104.
[23] ZHANG Y F, LI S F, PENG T, et al. One-step icELISA developed with novel antibody for rapid and specific detection of diclazuril residue in animal-origin foods[J]. Food Additives & Contaminants, Part A. 2020, 37(10):1633−1639.
[24] BAI Y C, WANG Y H, LI Q, et al. Binding affinity-guided design of a highly sensitive noncompetitive immunoassay for small molecule detection[J]. Food Chemistry,2021,351:129270. doi: 10.1016/j.foodchem.2021.129270
[25] XU X X, LIU L Q, WU X L, et al. Ultrasensitive immunochromatographic strips for fast screening of the nicarbazin marker in chicken breast and liver samples based on monoclonal antibodies[J]. Analytical Methods,2020,12(16):2143−2151. doi: 10.1039/D0AY00414F
[26] BOL’SHAKOV D S, AMELIN V G, TRET’YAKOV A V. Determination of polar pesticides in soil by micellar electrokinetic chromatography using QuEChERS sample preparation[J]. Journal of Analytical Chemistry,2014,69(1):89−97. doi: 10.1134/S1061934814010055
[27] 周鹏, 黄芊, 欧阳立群. 超高效液相色谱-串联质谱法测定茶叶中9种天然植物源农药残留量[J]. 质谱学报,2020,41(5):490−501. [ZHOU P, HUANG Q, OUYANG L Q. Determination of nine botanical pesticide residues in tea by UHPLC-MS/MS[J]. Journal of Chinese Mass Spectrometry Society,2020,41(5):490−501.] ZHOU P, HUANG Q, OUYANG L Q . Determination of nine botanical pesticide residues in tea by UHPLC-MS/MS[J]. Journal of Chinese Mass Spectrometry Society,2020 ,41 (5 ):490 −501 .[28] 彭树德. 鸡蛋中 26 种抗球虫药残留 UPLC-MS/MS方法的建立及应用[D]. 秦皇岛:河北科技师范学院, 2022. [PENG S D. Establishment and application of UPLC-MS/MS method for 26 coccidiostats residues in eggs[D]. Qinhuangdao:Hebei Normal University of Science & Technology, 2022.] PENG S D. Establishment and application of UPLC-MS/MS method for 26 coccidiostats residues in eggs[D]. Qinhuangdao: Hebei Normal University of Science & Technology, 2022.
[29] 邵丽, 董耀, 王晓, 等. QuEChERS-高效液相色谱-串联质谱法快速测定鸡肉中36种兽药残留[J]. 食品安全质量检测学报, 2021, 12(14):5561−5567. [SHAO L, DONG Y, WANG X, et al. Rapid detection of 36 kinds of veterinary drug residues in chicken by QuEChERS-high performance liquid chromatographytandem mass spectrometry[J]. Journal of Food Safety and Quality, 2021, 12(14):5561−5567.] SHAO L, DONG Y, WANG X, et al. Rapid detection of 36 kinds of veterinary drug residues in chicken by QuEChERS-high performance liquid chromatographytandem mass spectrometry[J]. Journal of Food Safety and Quality, 2021, 12(14): 5561−5567.
[30] 赵颖, 李典典, 张大卫, 等. QuEChERS试剂盒-高效液相色谱法检测鸡蛋中阿散酸和洛克沙砷残留[J]. 食品工业科技,2021,42(7):252−257. [ZHAO Y, LI D D, ZHANG D W, et al. Determination of arsanilic acid and roxarsone residues in eggs by QuEChERS kit -high performance liquid chromatography[J]. Science and Technology of Food Industry,2021,42(7):252−257.] ZHAO Y, LI D D, ZHANG D W, et al . Determination of arsanilic acid and roxarsone residues in eggs by QuEChERS kit -high performance liquid chromatography[J]. Science and Technology of Food Industry,2021 ,42 (7 ):252 −257 .





 下载:
下载:
 下载:
下载:
