Research Progress on Methionine Sulfoxide Reductase and Its Regulation on the Adversity Stress of Fruit and Vegetable
-
摘要: 甲硫氨酸亚砜还原酶(methionine sulfoxide reductase,Msr)是一类可以清除自由基、修复已氧化蛋白的抗氧化酶类,其可以将甲硫氨酸亚砜还原为有活性的甲硫氨酸,在调控果蔬成熟衰老及逆境胁迫抗性中发挥着重要作用。本文总结了Msr的分类,并针对果蔬作物中Msr的作用底物、基因家族以及Msr在调控果蔬代谢及逆境胁迫响应中的研究进展进行了综述。本文为进一步深入研究果蔬作物中Msr的种类及功能,以及通过基因工程手段改善果蔬的品质、提高抗逆性提供理论参考。Abstract: Methionine sulfoxide reductase (Msr) is a kind of antioxidant enzyme that can scavenge free radicals and repair oxidized proteins by reducing methionine sulfoxide to active methionine. Studies have shown that Msr play an important role in regulating ripening, senescence, and stress resistance of fruit and vegetable. In this paper, the classification of Msr is summarized. In addition, the research progresses on the substrates of Msr, gene families encoding Msr, and its role in regulating fruit and vegetable metabolism and stress response are reviewed. This paper would provide theoretical references for further studying the types and functions of Msr in fruit and vegetable crops, as well as improving the quality and stress resistance of fruit and vegetables by genetic engineering.
-
甲硫氨酸亚砜还原酶(methionine sulfoxide reductase,Msr)是广泛存在于动植物及微生物体内的一种氧化还原调节酶,在生物代谢过程中参与细胞防御和抗衰老过程,是细胞内重要的抗氧化酶。它可以通过两方面保护细胞免受氧化损伤,一方面可以修复因甲硫氨酸(methionine,Met)氧化而失活的蛋白[1]。Met是构成生物体内多肽和蛋白质的重要氨基酸,但Met易被H2O2及羟自由基等活性氧(reactive oxygen species,ROS)氧化成为甲硫氨酸亚砜(methionine sulfoxide,MetSO),导致含Met的蛋白质的生物学活性降低或丧失。而Msr可以将生物体内的MetSO还原为Met,使蛋白质重新恢复活性[1-2]。另一方面Msr可以在细胞中发挥抗氧化修复因子的作用,清除细胞中的ROS[1]。
果蔬在逆境胁迫下以及采后衰老过程中,机体内ROS的平衡体系会破坏,使得大量的O2−.、H2O2等在体内积累,导致氧化损伤,如改变细胞内生物大分子(蛋白质、DNA等)的结构和功能,造成蛋白质失活、DNA断裂,细胞膜的过氧化等[3-6],进而导致果蔬衰老以及病害的发生。据报道,全球果蔬浪费损失高达45%,造成巨大的经济损失[7]。但Msr可以通过恢复蛋白活性、维持清除ROS的能力等增强果蔬对胁迫的抗性,减少损害,保持果蔬品质[4,8]。本文就Msr的分类、作用底物、编码基因的研究进展以及其在果蔬衰老及逆境胁迫响应中的作用及机制进行了综述,以期为Msr在果蔬代谢调控方面的进一步研究和利用提供参考。
1. Msr的分类
Met是含硫氨基酸之一,其中的硫原子极易被氧化[9],硫原子的手性被氧化后形成S型和R型两种非对映异构体的MetSO,分为甲硫氨酸-S-亚砜(Met-S-SO)和甲硫氨酸-R-亚砜(Met-R-SO),二者共存且等量[9]。对应的有两种特异性Msr将MetSO还原为Met,分别为MsrA和MsrB[10]。MsrA特异性催化游离态和蛋白质中Met-S-SO还原为Met;MsrB特异性催化游离态和蛋白质中Met-R-SO还原为Met,但相比于MsrA催化游离态的能力,MsrB催化游离态Met-R-SO的能力很弱[11-12]。2007年,研究人员在大肠杆菌中发现了一种新的、可以特异性高效催化游离态Met-R-SO的酶,命名为fRMsr[10]。
MsrA[13]、MsrB[14]最早均在大肠杆菌中被发现,广泛存在于细菌、酵母、植物和哺乳动物等生物体中。MsrA与MsrB的蛋白结构不同[15],但两个亚家族各自具有相似的结构。通过对MsrA的序列研究发现,MsrA在催化过程中半胱氨酸(cysteine,Cys)残基在位置和数目上具有相似性和特异性,大致可以分为三类:含有3个保守的Cys残基,分别位于Cys51、Cys198、Cys206(数字代表大肠杆菌Msr序列中氨基酸残基位置,下同),植物中的Msr大体属于Cys51类,只有Cys51位于“GCFWG”保守序列,其中“GCFW”广泛存在于MsrA中,是鉴定MsrA的主要依据[16];含有两个保守的Cys残基,其中Cys51也位于“GCFWG”保守序列,第二个Cys位于“GYCH”或“GYXCH”中;仅由两个Cys残基且同时位于保守结构域“GCFWC”中[17]。MsrB分为两类:含有两个额外的“CxxC”保守基序,由4个保守的Cys残基构成,可以结合Zn2+,若保守Cys残基突变,则酶的活性全部丧失,植物中的MsrB大体属于这一类;相较于前者少一个“CxxC”保守基序,不能结合Zn2+[7,16]。fRMsr只存在于单细胞生物,多细胞生物中不存在[10],也分为两类:含有三个保守Cys残基;含有两个保守的Cys残基[17]。
不同Msr的催化过程会有差异,也会受到不同反应的调控[18],这可能会影响Msr在果蔬逆境胁迫中的调控能力。此外,Msr分类的细化,说明Msr的类别可能在Msr的调控机制中具有重要的地位[16]。
2. 果蔬Msr的作用底物
在动物和微生物中的研究发现,HIV-2蛋白酶、钙调素(calmodulin,CaM)、Ca2+/CaM依赖的蛋白激酶II(CaMKII)、载脂蛋白A-I、转录因子HypT等已经被鉴定为Msr的底物[19-20]。在植物中,最早发现的Msr底物是小分子热激蛋白sHSP21[20];CaM作为细胞调节分子可以间接调控钙调素结合蛋白发挥作用,研究发现CaM不仅是动物和微生物体内Msr的底物,同时也是果蔬中Msr的底物[19, 21-22]。另外,近年来研究发现,在果蔬中Msr还可以与抗氧化酶、转录因子、信号分子、蛋白激酶等多种类型的蛋白相互作用(表1)。如,在香蕉中研究发现,MaMsrB2可与抗坏血酸过氧化物酶1(ascorbate peroxidase 1,APX1)[23]及转录因子MaNAC42[24]相互作用,均可通过还原MetSO为Met,恢复蛋白的活性;Sun等[25]发现在大豆幼苗中,GsMsrB5a可以与Ca2+/CaM依赖的激酶GsCBRLK相互作用,并激活碳酸盐胁迫下幼苗中的活性氧信号[25]。除蛋白质外,一些多肽、氨基酸衍生物等也可以作为Msr的底物。比如,白菜中BpPMsr3可以通过与谷胱甘肽作用,恢复谷胱甘肽的活性[26]。果蔬中Msr还可以与外源生物蛋白相互作用,Gao等[27]发现Papaya ringspot virus(PRSV)中的核内涵体蛋白a蛋白酶(nuclear inclusion protein a protease,NIa-pro)可以与宿主番木瓜中的PaMsrB1相互作用,阻止PaMsrB1进入叶绿体发挥功能。
表 1 果蔬Msr的种类及作用底物/研究机制Table 1. Types and substrates/research mechanisms of Msr in fruits and vegetables果蔬种类 作用底物/调控机制 Msr类别 亚细胞定位 参考文献 香蕉 与MaCaM1互作介导果实抗氧化反应和类胡萝卜素生物合成相关基因的转录 MaPMsrA1、MaPMsrB1、MaMsrB5 细胞核 [23−24,35] MaPMsrA3、MaPMsrA4 叶绿体、细胞核 MaMsrA7* − 与MaAPX1、MaNAC42互作通过与氧化应激及成熟相关基因的启动子结合,参与果实成熟调控 MaPMsrA5 线粒体 [22] MaMsrB2* − 猕猴桃 通过还原Met为乙烯的合成提供原料 AdMsrB1 细胞核 [42] 桃 与PpCaM互作介导的抗冷相关基因的表达 PpMsr* 细胞质、细胞核 [21,52,62] PpMsrA1、PpMsrB1 细胞核 PpMsrA5 叶绿体、线粒体 PpMsrB5 叶绿体、细胞核 荔枝 与LcCaM1互作抑制衰老相关转录因子LcNAC13和LcWRKY1的活性 LcMsrA1* 细胞质、细胞核 [19] LcMsrA2 叶绿体、细胞核 LcMsrB1*、LcMsrB2 细胞核 龙眼 恢复谷胱甘肽、抗坏血酸等抗氧化酶活性,清除ROS DlMsrA5*、DlMsrB2* − [8] 番木瓜 恢复cpSRP43活性,促进光合作用,清除ROS PaPMsr、PaPMsrA 叶绿体、细胞核 [27] PaPMsrA1、PaMsrB1*、PaPMsrA5 叶绿体、细胞质、线粒体 PaPMsrB5 细胞核 番茄 与NOR互作启动成熟相关基因的转录 SlMsrA* 叶绿体、细胞质、细胞核 [39,42] SlMsrA3、SlPMsrB1、SlPMsrB5 细胞核 SlMsrA4 叶绿体、细胞核 SlPMsrA5 叶绿体 SlPMsrB2* − 白菜 恢复谷胱甘肽等抗氧化酶活性,清除ROS BpPMsr3* − [26] 芥菜 上调抗氧化酶的表达,清除ROS BjPMsr-like protein* − [53] 胡萝卜 上调抗氧化酶的表达,清除ROS DcPMsrA3、DcPMsrB、DcPMsrB1、DcPMsrB5* 细胞核 [54] DcPMsrA5 叶绿体 DcPMsrB9L* − 辣椒 响应SA、MeJA、乙烯的调控,CaMsrB2表达下调,引发HR CaPMsr 叶绿体、细胞质、细胞核 [34] CaPMsrA1、CaPMsrA4、CaPMsrB 细胞核 CaPMsrA5、CaPMsrB1、CaPMsrB5 叶绿体、细胞核 CaPMsrB2* 细胞核、高尔基体 草莓 与SlMsrA功能类似,调控果实成熟,上调抗氧化酶的表达,清除ROS FaMsrA* 细胞质、细胞核 [45] FaPMsr1 细胞核 可被外源生长素抑制激活表达 FaPMsr* 细胞质、细胞核 [32] 平菇 上调抗氧化酶的表达,清除ROS PoMsr、PoPMsr、PoPMsrB2 细胞核 [38] PoMsrA* − 注:“*”表示有相应参考文献支持作用底物/调控机制的Msr。 Msr与底物的相互作用是其参与调控果蔬逆境胁迫的重要机制,由上述可知,果蔬中Msr的作用底物类型多样,因此Msr在果蔬的各种胁迫反应中可能发挥重要作用。但目前对于果蔬中Msr作用底物的研究仍非常有限,加大对Msr作用底物的研究力度,有助于进一步揭示Msr的作用机制。
3. 果蔬Msr基因家族
Msr基因家族具有很高的序列同源性,但MsrA和MsrB两个亚家族的基因基本不存在序列相似性。目前已知在番茄中存在5种MsrA(分别为SlMsrA(E4)、SlMsrA2~A4、SlPMsrA5)基因和3种MsrB(SlPMsrB1、SlMsrB2、SlPMsrB5)基因。亚细胞定位预测了下列蛋白质的位置(表1),分析显示SlMsrA预测定位于叶绿体、细胞质和细胞核中[28-29],SlMsrA3在细胞核中,SlMsrA4定位于叶绿体和细胞核,SlPMsrA5主要在叶绿体中,SlPMsrB1在细胞膜和细胞核中[30-31],SlPMsrB5有两个可变剪切体,SlPMsrB5.1和SlPMsrB5.2,它们表达的蛋白均定位在细胞核中。在草莓中,目前已发现了3种Msr基因(FaMsrA、FaPMsr、FaPMsr1),其中,FaMsrA编码的蛋白质与番茄中的SlMsrA编码的蛋白质具有相似的功能。蛋白质FaMsrA和FaPMsr预测定位在细胞质和细胞核中,而FaPMsr1定位于细胞核中。在马铃薯中,已知有7种Msr编码基因(StPMsr、StPMsrA1、StPMsrA3、StPMsrA5、StPMsrB、StPMsrB1、StPMsrB5),其中StPMsr、StPMsrA3、StPMsrB、StPMsrB5均定位于细胞核中,StPMsrA1定位于细胞壁、细胞核和叶绿体中,而StPMsrA5定位于叶绿体中;StPMsrB1有两种可变剪切体为StPMsrB1.1、StPMsrB1.2,两者表达的蛋白均定位于细胞核中。
由此可知,在果蔬作物中存在多个Msr基因家族及编码基因。进一步研究发现,不同的Msr亚型的基因在果蔬作物中的表达模式也有较大的差异。番茄中SlMsrA的表达受乙烯诱导,而且仅在成熟果实中表达,其他器官中不表达[30-31];而SlMsrA2在所有器官中均有表达,但在红熟期果实中表达量最高;SlMsrA3和SlMsrA4在叶和花中的表达量更高,而SlMsrA5在根、叶、茎和红色果实中几乎不表达,但在花中有相对较高的表达[28];SlMsrB1在叶、花和红熟期的番茄果实中均有较高的表达[31]。草莓中也有一种FaPMsr只在红色成熟果实中表达[32];在茄子果实发育过程中,SmMsrA的表达水平在开花日最高[33]。另外,Oh等[34]研究表明,通常胞质型Msr在根中被特异性表达,而质体型Msr则主要在发生光合作用的光合器官中被表达,如CaMsrB2在辣椒的叶、花和茎中的转录水平远远高于根。上述研究表明,Msr基因在果蔬作物生长发育的不同阶段特异性表达,可能与它们功能的发挥密切相关,随着果蔬的生长发育发挥相应功能,以促进果蔬作物的正常生长[35]。
4. Msr在果蔬代谢及逆境胁迫中的调控作用
4.1 Msr在果蔬成熟衰老中的调控作用
根据衰老的自由基理论,有氧呼吸导致ROS的产生,ROS引起蛋白质、脂类、DNA等大分子的氧化损伤,从而促进衰老过程,抗氧化应激和降低氧化损伤(即消除ROS和修复氧化蛋白)是维持蛋白质功能和调节衰老的关键[36]。在一些细胞、组织和生物体中,过表达Msr可能会延长寿命或增加抗氧化应激能力,而缺失或突变的Msr则会缩短寿命或降低抗氧化应激能力[37]。例如在平菇中,与野生型相比,过表达PoMsrA的菌株对H2O2耐受能力显著增强,菌丝生长速度明显提高,菇体的衰老速度明显下降[38]。
Msr参与调控果蔬成熟衰老的机制比较复杂,可以通过与成熟相关的转录因子相互调控,参与各种成熟相关的反应。例如,在番茄中研究表明SlMsrA的表达受乙烯的强烈诱导[29];并且对转录因子NOR氧化损伤有明显的修复作用,可以逆转因NOR亚砜化导致的番茄成熟相关基因转录活性的降低[39]。另外,SlMsrA和SlMsrB2的转录活性也受NOR的调控[40],Skelly[41]研究表明,NOR可以与SlMsrA和SlMsrB2启动子中的TATA盒结合并激活它们的表达,促进果实的成熟[39]。而在猕猴桃采后贮藏过程中,乙烯会通过诱导转录因子AdNAC2和AdNAC72靶向激活AdMsrB1的表达,而且AdMsrB1的超表达也可以增加乙烯合成的直接前体ACC的含量,或者发挥酶活性将MetSO还原为Met补充乙烯合成过程中的前体,维持乙烯的高效合成[42]。
Msr还可以通过酶促系统、蛋白质的氧化还原修饰、激素等多种方式间接调控果蔬成熟[24]。APX是一种重要的抗氧化酶,可以与抗氧化酶系统相偶联调节ROS的水平,参与植物多种发育生理过程和应激反应。在香蕉中的研究发现,MaMsrB2可还原MaAPX1中被氧化的Met残基,恢复MaAPX1的活性,调节果实的成熟衰老过程[23]。另外,Jiang等[22]通过转录组分析发现,在香蕉成熟衰老过程中MaMsrA7与MaCaM1的表达均快速上调,而且MaMsrA7可修复MaCaM1的亚砜化修饰,从而促进了MaCaM1介导的果实抗氧化反应和类胡萝卜素生物合成相关基因的转录。在荔枝中,被氧化的LcCaM1可以与衰老相关转录因子LcNAC13和LcWRKY1相互作用增强这两个转录因子结合DNA的活性,而LcMsrA1和LcMsrB1还原LcCaM1中被氧化的Met残基,从而抑制衰老进程[19]。
Msr也受外源物质的调控,参与外源物质介导果蔬抗衰老的过程。例如,褪黑素及α-硫辛酸处理延缓荔枝果实的衰老或果皮的褐变也与LcMsrs表达的上调密切相关[43-44];L-盐酸半胱氨酸可以通过维持龙眼果实中DlMsr、DlMsrA5和DlMsrB2的表达水平减缓果实衰老进程[9]。另外,植物磺肽素延缓草莓果实的衰老和腐烂也与诱导Msr和过氧化物酶基因的表达、维持抗氧化相关酶的活性密切相关[45]。茄子中SmMsrA可以调控多胺的含量进而影响茄子单性结实[46-47]。这表明,Msr在果蔬的生长、成熟、衰老的各个阶段均发挥重要作用。
4.2 Msr在果蔬非生物胁迫响应中的调控作用
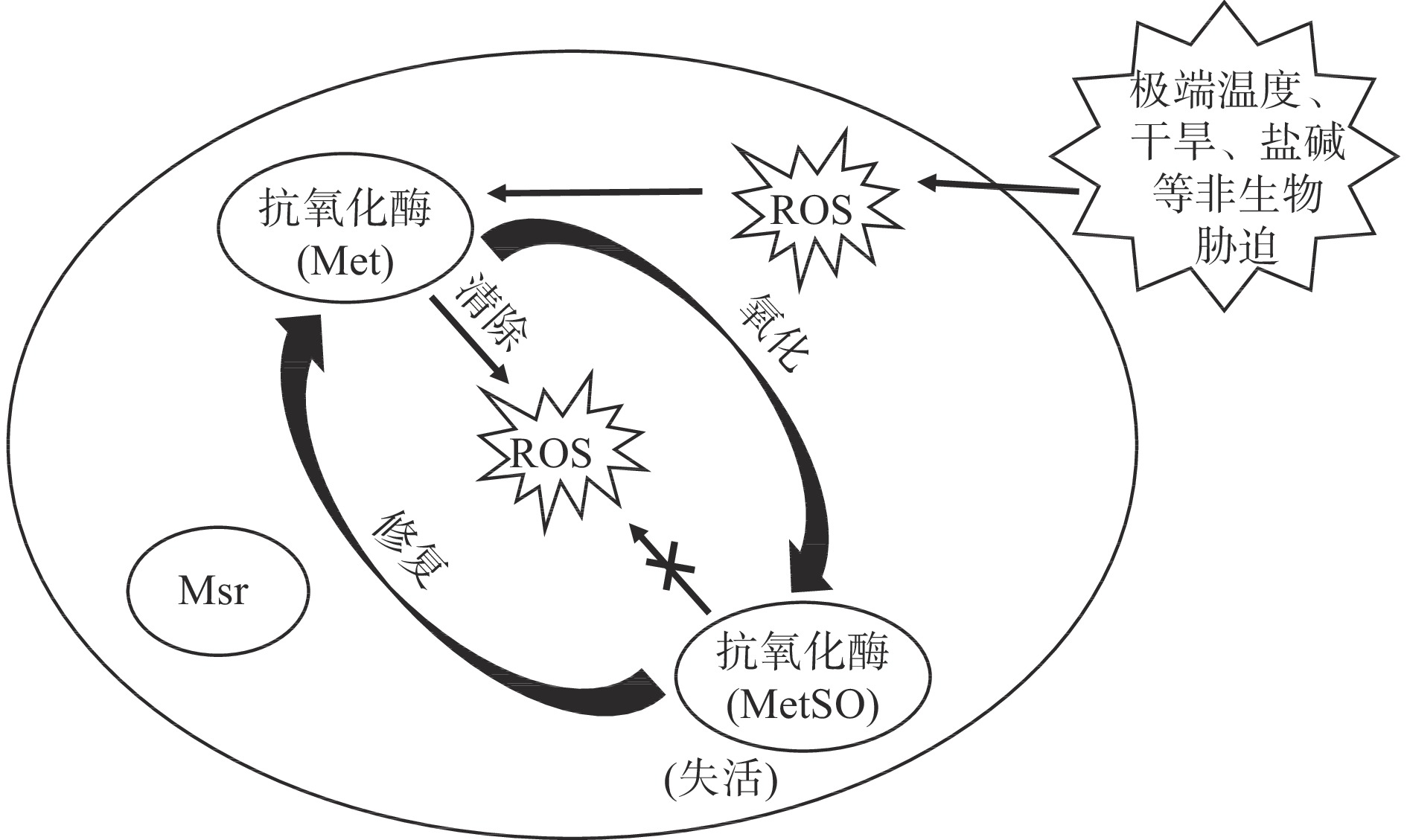
果蔬在生长发育过程中会遇到多种非生物胁迫(极端温度、干旱、盐碱、洪涝、辐照、化学物质等)因素的影响[48]。研究发现,逆境胁迫会诱导果蔬体内多种Msr基因的表达,有助于清除大量产生的ROS,在调控果蔬非生物胁迫抗性中发挥重要作用[7](图1)。异源表达拟南芥基因AtMsrB7、AtMsrB8、AtMsrB9的番茄叶片,抵抗甲基精紫(methyl viologen,MV)氧化胁迫的能力明显增强,表明Msr在植株响应MV胁迫中发挥重要作用[49]。响应于H2O2处理,番茄SlMsrA表达量显著升高,维持了番茄幼苗的抗氧化能力[50]。
干旱和盐碱严重限制果蔬的存活能力。利用甘露醇和氯化钠模拟干旱和高盐胁迫处理番茄幼苗[50]和平菇[38],检测到SlMsrA和PoMsrA表达量均显著增加;SlMsrB2可以通过修复核酮糖-1,5-二磷酸羧化酶小亚基3B和过氧化氢酶2来提高叶绿素含量和清除ROS以增强抗旱能力[51],表明Msr在果蔬响应干旱和盐胁迫中也发挥了重要作用。
极端温度是影响果蔬作物生长发育和果实品质的重要环境因素之一,Msr在植物低温胁迫响应中也发挥重要作用。桃果实遭遇低温胁迫时,激酶[21]、赤霉素[52]均可以提高PpMsrs的表达量,抵抗低温胁迫造成的氧化损伤[21,52];在平菇中,32 ℃高温处理会显著增强PoMsrA的表达,增强菇体的抗热性和抗氧化能力[38]。
随着现代工业的发展,金属离子对果蔬伤害的机率日益增加。根据蛋白质组学分析发现,铜和镉胁迫会导致芥菜细胞质中BjMsrA2的表达明显增加[53];胡萝卜中镉胁迫会上调Msr的表达以应对镉胁迫导致的氧化损伤[54];异源表达大白菜BpPMsr3的拟南芥幼苗在镉胁迫下的存活率也显著上升[26]。在其他类型植物中存在Msr与铜离子螯合的方式来增强铜胁迫的抗性[55],推测果蔬中可能也存在类似的机制。
4.3 Msr在果蔬生物胁迫响应中的调控作用
果蔬作物生长发育过程中也经常遭受细菌、真菌、病毒或害虫的侵害,Msr在调控果蔬作物响应这些生物胁迫中也发挥了重要作用。由Xanthomonas axonopodis pv Vesicatoria(Xav)导致的细菌斑点病是甜椒的重要病害之一,利用病毒诱导基因沉默(virus-induced gene silencing,VIGS)技术沉默CaMsrB2会降低病程相关蛋白(pathogenesis-related proteins,PR)基因CaPR4和CaPR10的表达,增加甜椒对Xav的敏感性[34];而在番茄中超表达CaMsrB2会促进防御相关基因SlP1、SlPR-1b和SlP23等的表达,增强植株的抗病性[34]。Dai等[28]发现SlMsrA2-5的表达可被水杨酸(salicylic acid,SA)处理明显诱导,推测SlMsrAs可能参与了番茄的病害防御过程。
Msr作为一种重要的ROS调节酶,可调节防御蛋白中Met的氧化还原状态和细胞的氧化状态,是果蔬防御体系的重要因子[34]。因此,Msr也成为病毒或细菌等病原体防御机制攻击的靶点。NIa-Pro是PRSV中的一种多功能病毒非结构蛋白,在PRSV侵染番木瓜后NIa-Pro可以与PaMsrB1直接互作,干扰PaMsrB1进入叶绿体发挥清除ROS和修复叶绿体受损蛋白的功能[27,56]。
4.4 Msr参与信号分子介导果蔬代谢
Msr在多种信号分子[ROS、活性氮(reactive nitrogen species,RNS)、激酶、植物激素]介导的果蔬生长发育和防御过程中也发挥了重要作用[57]。
ROS在植物体内具有双重作用,高浓度的ROS会导致细胞氧化损伤,丧失正常的生理功能;而低浓度的ROS可作为信号分子调控抗性基因和防卫基因的表达,在果蔬的生长发育及逆境响应中发挥积极作用[34]。例如,在桃果实中,ROS增加线粒体蛋白质羰基化进程[58],同时也诱导相关Msr的表达,延缓果实衰老、增加抗氧化能力。在辣椒中研究表明,CaMsrB2可调控辣椒防御反应期间ROS的产生,而该ROS在由不相容病原体引起的超敏反应(hypersensitivity,HR)中发挥重要作用。另外,胁迫产生的ROS也可诱导多种果蔬作物体内Msr基因的表达,还原抗氧化蛋白中被氧化的Met,进而恢复清除ROS的能力[35]。
RNS是另一种与ROS紧密相关的氧化剂分子,如一氧化氮(nitric oxide,NO)与超氧化物反应产生的过氧亚硝酸盐,高浓度下也会氧化破坏生物大分子,但在基础水平上,可作为改变细胞氧化还原稳态的信号,通过提高Msr的表达、抗氧化酶的活性以及抗氧化物质的含量,抑止脂质过氧化作用,清除部分ROS[4,59],在果蔬的发育及逆环境胁迫的反应中发挥重要的调控作用[35]。
激酶也可以调控Msr的表达,桃果实中糖原合成酶激酶3(GSK-3)可以上调包括Msr在内的抗氧化酶基因的表达,增强果实抗冷性[21]。肌醇1,4,5-三磷酸(IP3) [60]、γ-氨基丁酸[61]等可以调控Ca2+介导的信号通路或者增强Msr-Trx系统提高Msr等抗氧化酶基因的表达,增强抗氧化能力。
植物激素对Msr的调控具有双面性,一部分植物激素可以显著提高Msr的表达。如番茄幼苗响应于外源脱落酸和SA处理,SlMsrA表达量显著升高,表明SlMsrA可能参与了SA介导番茄幼苗抗病过程[28,54]。另外,有研究表明激素也会通过抑制Msr的表达,调控果蔬作物的生长。如正常情况下,草莓的FaPMsr只在红熟期果实的花托中表达,在其它组织中均检测不到;但当未熟的绿果在花托上被摘除时,果实中FaPMsr的表达可被显著激活,而外源应用生长素(如萘乙酸)可抑制此激活过程[32]。在辣椒中,响应于SA、茉莉酸甲酯(methyl jasmonate,MeJA)和乙烯处理,CaMsrB2的表达明显下调,加速ROS的积累,从而在病害位置引起HR,表明CaMsrB2积极响应防御信号[34]。
综上所述,果蔬在成熟衰老及遭受各种生物和非生物胁迫过程中会产生大量ROS,一方面会导致果蔬发生氧化损伤;另一方面,ROS也可诱导Msr等果蔬体内防御机制的启动。Msr可以通过还原被氧化的Met修复各种蛋白质,其中包括抗氧化酶、转录因子、钙调蛋白等,维持蛋白质在各自的代谢网络中发挥相应的功能;另外,Msr也可以参与NO、GA、SA以及乙烯等多种信号分子介导的果蔬代谢过程,是信号分子调控果蔬代谢的重要机制之一(表1)。
5. 结语与展望
尽管近年来对于果蔬中Msr蛋白的结构、生理功能、作用底物以及基因表达模式等已开展了大量的研究工作,但相较于动物、微生物及模式植物中Msr的研究还有较大的差距。如,许多果蔬作物中Msr的编码基因还没得到鉴定、多数果蔬中Msr蛋白的具体作用机制仍未研究透彻、果蔬中Msr底物的研究仍然不足,对于庞大的信号网络的交互知之甚少。另外,关于Msr具体如何协调酶促系统和非酶促系统清除ROS也有待更深入的研究。鉴于Msr家族在果蔬各种代谢途径中的重要作用,其在实际应用中的价值也有待开发,如Msr活性的增加可以增强果蔬抵抗低温、盐碱、干旱等逆境胁迫,是否可以通过转基因技术应用到其他经济作物中,或通过育种筛选具有优良Msr基因的果蔬等。随着分子生物学技术的发展,对果蔬Msr的研究带来很大的帮助,今后可借助VIGS技术、CRISPR/Cas9基因编辑技术及组学技术等更广泛的鉴定果蔬作物中未知的Msr,揭示其编码基因的序列,深入挖掘其生理功能及作用机制,为果蔬作物品质的改良、逆境抗性的调控奠定理论基础。
-
表 1 果蔬Msr的种类及作用底物/研究机制
Table 1 Types and substrates/research mechanisms of Msr in fruits and vegetables
果蔬种类 作用底物/调控机制 Msr类别 亚细胞定位 参考文献 香蕉 与MaCaM1互作介导果实抗氧化反应和类胡萝卜素生物合成相关基因的转录 MaPMsrA1、MaPMsrB1、MaMsrB5 细胞核 [23−24,35] MaPMsrA3、MaPMsrA4 叶绿体、细胞核 MaMsrA7* − 与MaAPX1、MaNAC42互作通过与氧化应激及成熟相关基因的启动子结合,参与果实成熟调控 MaPMsrA5 线粒体 [22] MaMsrB2* − 猕猴桃 通过还原Met为乙烯的合成提供原料 AdMsrB1 细胞核 [42] 桃 与PpCaM互作介导的抗冷相关基因的表达 PpMsr* 细胞质、细胞核 [21,52,62] PpMsrA1、PpMsrB1 细胞核 PpMsrA5 叶绿体、线粒体 PpMsrB5 叶绿体、细胞核 荔枝 与LcCaM1互作抑制衰老相关转录因子LcNAC13和LcWRKY1的活性 LcMsrA1* 细胞质、细胞核 [19] LcMsrA2 叶绿体、细胞核 LcMsrB1*、LcMsrB2 细胞核 龙眼 恢复谷胱甘肽、抗坏血酸等抗氧化酶活性,清除ROS DlMsrA5*、DlMsrB2* − [8] 番木瓜 恢复cpSRP43活性,促进光合作用,清除ROS PaPMsr、PaPMsrA 叶绿体、细胞核 [27] PaPMsrA1、PaMsrB1*、PaPMsrA5 叶绿体、细胞质、线粒体 PaPMsrB5 细胞核 番茄 与NOR互作启动成熟相关基因的转录 SlMsrA* 叶绿体、细胞质、细胞核 [39,42] SlMsrA3、SlPMsrB1、SlPMsrB5 细胞核 SlMsrA4 叶绿体、细胞核 SlPMsrA5 叶绿体 SlPMsrB2* − 白菜 恢复谷胱甘肽等抗氧化酶活性,清除ROS BpPMsr3* − [26] 芥菜 上调抗氧化酶的表达,清除ROS BjPMsr-like protein* − [53] 胡萝卜 上调抗氧化酶的表达,清除ROS DcPMsrA3、DcPMsrB、DcPMsrB1、DcPMsrB5* 细胞核 [54] DcPMsrA5 叶绿体 DcPMsrB9L* − 辣椒 响应SA、MeJA、乙烯的调控,CaMsrB2表达下调,引发HR CaPMsr 叶绿体、细胞质、细胞核 [34] CaPMsrA1、CaPMsrA4、CaPMsrB 细胞核 CaPMsrA5、CaPMsrB1、CaPMsrB5 叶绿体、细胞核 CaPMsrB2* 细胞核、高尔基体 草莓 与SlMsrA功能类似,调控果实成熟,上调抗氧化酶的表达,清除ROS FaMsrA* 细胞质、细胞核 [45] FaPMsr1 细胞核 可被外源生长素抑制激活表达 FaPMsr* 细胞质、细胞核 [32] 平菇 上调抗氧化酶的表达,清除ROS PoMsr、PoPMsr、PoPMsrB2 细胞核 [38] PoMsrA* − 注:“*”表示有相应参考文献支持作用底物/调控机制的Msr。 -
[1] GAO Y, ZHU J, DING P, et al. The Brachypodium distachyon methionine sulfoxide reductase gene family[J]. Genes Genom,2017,39(9):975−985. doi: 10.1007/s13258-017-0561-4
[2] DING P, GAO Y, ZHU J, et al. Wheat methionine sulfoxide reductase genes and their response to abiotic stress[J]. Molecular Breeding,2016,36(12):169. doi: 10.1007/s11032-016-0597-1
[3] KAKESHPOUR T, TAMANG T M, MOTOLAI G, et al. CGFS-type glutaredoxin mutations reduce tolerance to multiple abiotic stresses in tomato[J]. Physiologia Plantarum,2021,173(3):1263−1279. doi: 10.1111/ppl.13522
[4] WANI K I, NAEEM M, CASTROVERDE C D M, et al. Molecular mechanisms of nitric oxide (NO) signaling and reactive oxygen species (ROS) homeostasis during abiotic stresses in plants[J]. International Journal of Molecular Sciences,2021,22(17):9656. doi: 10.3390/ijms22179656
[5] SACHDEV S, ANSARI S A, ANSARI M I, et al. Abiotic stress and reactive oxygen species: Generation, signaling, and defense mechanisms[J]. Antioxidants,2021,10(2):277. doi: 10.3390/antiox10020277
[6] WOJCIECHOWSKA N, BAGNIEWSKA-ZADWORNA A, MINICKA J, et al. Localization and dynamics of the methionine sulfoxide reductases MsrB1 and MsrB2 in beech seeds[J]. International Journal of Molecular Sciences,2021,22(1):402. doi: 10.3390/ijms22010402
[7] HUANG X, REN J, LI P, et al. Potential of microbial endophytes to enhance the resistance to postharvest diseases of fruit and vegetables[J]. Journal of Food and Agriculture,2021,101(5):1744−1757. doi: 10.1002/jsfa.10829
[8] ZHU J, DING P, LI Q, et al. Molecular characterization and expression profile of methionine sulfoxide reductase gene family in maize (Zea mays) under abiotic stresses[J]. Gene,2015,562(2):159−168. doi: 10.1016/j.gene.2015.02.066
[9] LI T, WU Q, ZHOU Y, et al. L-cysteine hydrochloride delays senescence of harvested longan fruit in relation to modification of redox status[J]. Postharvest Biology and Technology,2018,143:35−42. doi: 10.1016/j.postharvbio.2018.04.011
[10] LE D T, NGUYEN K L, CHU H D, et al. Function of the evolutionarily conserved plant methionine-S-sulfoxide reductase without the catalytic residue[J]. Protoplasma,2018,255(6):1741−1750. doi: 10.1007/s00709-018-1266-5
[11] AUSSEL L, EZRATY B. Methionine redox homeostasis in protein quality control[J]. Frontiers in Molecular Biosciences,2021,8:665492. doi: 10.3389/fmolb.2021.665492
[12] JIANG B, ADAMS Z, MOONAH S, et al. The antioxidant enzyme methionine sulfoxide reductase A (MsrA) interacts with Jab1/CSN5 and regulates its function[J]. Antioxidants, 2020, 9(5): 452.
[13] 王海波, 邹竹荣, 龚明. 小桐子甲硫氨酸亚砜还原酶A的基因克隆及生物信息学分析[J]. 基因组学与应用生物学,2015,34(4):821−829. [WANG H B, ZOU Z R, GONG M. Gene cloning and bioinformatic analysis of the methionine sulfoxide reductase a from jatropha curcas[J]. Genomics and Applied Biology,2015,34(4):821−829. [14] 韩宗强, 崔宗杰. 信号蛋白中甲硫氨酸残基的可逆性氧化和甲硫氨酸亚砜还原酶[J]. 生物物理学报,2010,26(10):861−879. [HAN Z Q, CUI Z J. Reversible methionine residue oxidation in signalling proteins and methionine sulfoxide reductases[J]. Acta Biophysica Sinica,2010,26(10):861−879. [15] KALEMBA E M, STOLARSKA E. Regulation of gene expression of methionine sulfoxide reductases and their new putative roles in plants[J]. International Journal of Molecular Sciences,2019,20(6):1309. doi: 10.3390/ijms20061309
[16] 黄舒, 李刚, 朱建堂, 等. 植物Msr (methionine sulfoxide reductase)基因家族的研究进展[J]. 生命的化学,2015,35(3):313−319. [HUANG S, LI G, ZHU J T, et al. Research progress of plant Msr (methionine sulfoxide reductase) gene family[J]. Chemistry of Life,2015,35(3):313−319. [17] KWAK G H, KIM M J, KIM H Y. Cysteine-125 is the catalytic residue of Saccharomyces cerevisiae free methionine-R-sulfoxide reductase[J]. Biochemical and Biophysical Research Communications,2010,395(3):412−415. doi: 10.1016/j.bbrc.2010.04.036
[18] TARRAGO L, LAUGIER E, ZAFFAGNINI M, et al. Regeneration mechanisms of Arabidopsis thaliana methionine sulfoxide reductases B by glutaredoxins and thioredoxins[J]. Journal of Biological Chemistry,2009,284(28):18963−18971. doi: 10.1074/jbc.M109.015487
[19] JIANG G, XIAO L, YAN H, et al. Redox regulation of methionine in calmodulin affects the activity levels of senescence-related transcription factors in litchi[J]. Biochimica et Biophysica Acta (BBA)-General Subjects,2017,1861(5 Pt A):1140−1151.
[20] DRAZIC A, MIURA H, PESCHEK J, et al. Methionine oxidation activates a transcription factor in response to oxidative stress[J]. Proceedings of the National Academy of Sciences,2013,110(23):9493−9498. doi: 10.1073/pnas.1300578110
[21] JIAO C, DUAN Y. The role of glycogen synthase kinase-3 in gibberellic acid-induced chilling tolerance and defense response in postharvest peach fruit[J]. Food and Bioprocess Technology,2019,12(10):1733−1740. doi: 10.1007/s11947-019-02338-3
[22] JIANG J X, WU H W, LI Z W, et al. Sulfoxidation regulation of Musa acuminata calmodulin (MaCaM) influences the functions of MaCaM-binding proteins[J]. Plant and Cell Physiology,2018,59(6):1214−1224. doi: 10.1093/pcp/pcy057
[23] XIAO L, JIANG G, YAN H, et al. Methionine sulfoxide reductase B regulates the activity of ascorbate peroxidase of banana fruit[J]. Antioxidants,2021,10(2):310. doi: 10.3390/antiox10020310
[24] YAN H L, JIANG G X, WU F W, et al. Sulfoxidation regulation of transcription factor NAC42 influences its functions in relation to stress-induced fruit ripening in banana[J]. Journal of Experimental Botany,2021,72(2):682−699. doi: 10.1093/jxb/eraa474
[25] SUN X, SUN M, JIA B, et al. A Glycine soja methionine sulfoxide reductase B5a interacts with the Ca2+/CAM-binding kinase GsCBRLK and activates ROS signaling under carbonate alkaline stress[J]. The Plant Journal,2016,86(6):514−529. doi: 10.1111/tpj.13187
[26] HAN Y Y, DU Y L, WANG J W, et al. Overexpression of Chinese flowering cabbage BpPMSR3 enhances the tolerance of Arabidopsis thaliana to cadmium[J]. Journal of Plant Nutrition and Soil Science,2018,181(5):787−794. doi: 10.1002/jpln.201700352
[27] GAO L, SHEN W T, YAN P, et al. NIa-pro of Papaya ringspot virus interacts with papaya methionine sulfoxide reductase B1[J]. Virology,2012,434(1):78−87. doi: 10.1016/j.virol.2012.09.007
[28] DAI C, WANG M H. Characterization and functional analysis of methionine sulfoxide reductase A gene family in tomato[J]. Molecular Biology Reports,2012,39(5):6297−6308. doi: 10.1007/s11033-012-1451-0
[29] DAI C, HAN W, WANG M H. Two highly homologous methionine sulfoxide reductase a from tomato (Solanum lycopersicum), exhibit distinct catalytic properties[J]. The Protein Journal,2012,31(4):285−292. doi: 10.1007/s10930-012-9403-z
[30] AOKI K, YANO K, SUZUKI A, et al. Large-scale analysis of full-length cDNAs from the tomato (Solanum lycopersicum) cultivar Micro-Tom, a reference system for the Solanaceae genomics[J]. BMC Genomics, 2010, 11(1): 210.
[31] DAI C, LIU L, WANG M H. Characterization of a methionine sulfoxide reductase B from tomato (Solanum lycopersicum), and its protecting role in saccharomyces cerevisiae[J]. The Protein Journal,2013,32(1):39−47. doi: 10.1007/s10930-012-9457-y
[32] LOPZE A P, PORTALES R B, LO´ PZE-RA´ EZ J A, et al. Characterization of a strawberry late-expressed and fruit-specific peptide methionine sulphoxide reductase[J]. Physiologia Plantarum,2006,126(1):129−139. doi: 10.1111/j.1399-3054.2005.00580.x
[33] SADANANDOM A, POGHOSYAN Z, FAIRBAIRN D J, et al. Differential regulation of plastidial and cytosolic isoforms of peptide methionine sulfoxide reductase in arabidopsis[J]. Plant Physiology,2000,123(1):255−264. doi: 10.1104/pp.123.1.255
[34] OH S K, BAEK K H, SEONG E S, et al. CaMsrB2, Pepper methionine sulfoxide reductase B2, is a novel defense regulator against oxidative stress and pathogen attack[J]. Plant Physiology,2010,154(1):245−261. doi: 10.1104/pp.110.162339
[35] REY P, TARRAGO L. Physiological roles of plant methionine sulfoxide reductases in redox homeostasis and signaling[J]. Antioxidants,2018,7(9):114. doi: 10.3390/antiox7090114
[36] WANG P, LI X, WANG Y, et al. Redox proteomic analysis reveals the involvement of oxidative post-translational modification in tomato fruit ripening[J]. Postharvest Biology and Technology,2021,178:111556. doi: 10.1016/j.postharvbio.2021.111556
[37] KIM J I, NOH M R, KIM K Y, et al. Methionine sulfoxide reductase A deficiency exacerbates progression of kidney fibrosis induced by unilateral ureteral obstruction[J]. Free Radical Biology and Medicine,2015,89:201−208. doi: 10.1016/j.freeradbiomed.2015.07.018
[38] YIN C, ZHENG L, ZHU J, et al. Enhancing stress tolerance by overexpression of a methionine sulfoxide reductase A (MsrA) gene in Pleurotus ostreatus[J]. Applied Microbiology and Biotechnology,2015,99(7):3115−3126. doi: 10.1007/s00253-014-6365-4
[39] JIANG G, ZENG J, LI Z, et al. Redox regulation of the nor transcription factor is involved in the regulation of fruit ripening in tomato[J]. Plant Physiology,2020,183(2):671−685. doi: 10.1104/pp.20.00070
[40] LIU G S, LI H L, GRIERSON D, et al. NAC transcription factor family regulation of fruit ripening and quality: A review[J]. Cells,2022,11(3):525. doi: 10.3390/cells11030525
[41] SKELLY M J. Ripened by redox: Sulfoxidation of NOR regulates tomato ripening[J]. Plant Physiology,2020,183(2):431−432. doi: 10.1104/pp.20.00457
[42] FU B L, WANG W Q, LIU X F, et al. An ethylene-hypersensitive methionine sulfoxide reductase regulated by NAC transcription factors increases methionine pool size and ethylene production during kiwifruit ripening[J]. New Phytologist,2021,232(1):237−251. doi: 10.1111/nph.17560
[43] ZHANG Y Y, HUBER D J, HU M J, et al. Delay of postharvest browning in litchi fruit by melatonin via the enhancing of antioxidative processes and oxidation repair[J]. Journal of Agricultural and Food Chemistry,2018,66(28):7475−7484. doi: 10.1021/acs.jafc.8b01922
[44] HE M Y, WU Y F, HONG M, et al. α-Lipoic acid treatment alleviates postharvest pericarp browning of litchi fruit by regulating antioxidant ability and energy metabolism[J]. Postharvest Biology and Technology,2021,180:111629. doi: 10.1016/j.postharvbio.2021.111629
[45] AGHDAM M S, FLORES F B, SEDAGHATI B. Exogenous phytosulfokine α (PSKα) application delays senescence and relieves decay in strawberry fruit during cold storage by triggering extracellular ATP signaling and improving ROS scavenging system activity[J]. Scientia Horticulturae,2021,279:109906. doi: 10.1016/j.scienta.2021.109906
[46] 张映, 陈钰辉, 张振贤, 等. 茄子甲硫氨酸亚砜还原酶(SmMsrA)基因cDNA全长的克隆和分析[J]. 园艺学报,2011,38(8):1469−1478. [ZHANG Y, CHENG Y H, ZHANG Z X, et al. cDNA cloning and characterization of a eggplant peptide methionine sulfoxide reductase (SmMsrA)[J]. Acta Horticulturae Sinica,2011,38(8):1469−1478. doi: 10.16420/j.issn.0513-353x.2011.08.007 [47] 张映, 刘富中, 李香景, 等. 茄子单性结实候选基因的表达分析[J]. 中国蔬菜,2011(16):20−26. [ZHANG Y, LIU F Z, LI X J, et al. Expression analysis of eggplant parthenocarpic candidate genes[J]. China Vegetables,2011(16):20−26. [48] DING P, FANG L, HUANG S, et al. Wheat plastidial methionine sulfoxide reductase MSRB3.1 interacts with haem oxygenase 1 to improve osmotic stress tolerance in wheat seedlings[J]. Environmental and Experimental Botany,2021,188:104528. doi: 10.1016/j.envexpbot.2021.104528
[49] LI C W, LEE S H, CHAN M T. Utilization of the plant methionine sulfoxide reductase B genes as selectable markers in Arabidopsis and tomato transformation[J]. Plant Cell, Tissue and Organ Culture (PCTOC),2013,113(3):555−563. doi: 10.1007/s11240-013-0296-0
[50] DAI C. Expression pattern of a peptide methionine sulfoxide reductase gene from tomato (Solanum lycopersicum) in response to abiotic and oxidative stresses[J]. Journal of the Korean Society for Applied Biological Chemistry,2010,53(2):127−132. doi: 10.3839/jksabc.2010.022
[51] CUI L, ZHENG F, ZHANG D, et al. Tomato methionine sulfoxide reductase B2 functions in drought tolerance by promoting ROS scavenging and chlorophyll accumulation through interaction with Catalase 2 and RBCS3B[J]. Plant Science, 2022, 318: 111206.
[52] JIAO C F, DUAN Y Q. Guanosine 3',5'-cyclic monophosphate mediates gibberellic acid-induced chilling tolerance and defense response in postharvest peach fruit[J]. Postharvest Biology and Technology,2019,155:80−85. doi: 10.1016/j.postharvbio.2019.04.018
[53] ALVAREZ S, BERLA B M, SHEFFIELD J, et al. Comprehensive analysis of the Brassica juncea root proteome in response to cadmium exposure by complementary proteomic approaches[J]. Proteomics,2009,9(9):2419−2431. doi: 10.1002/pmic.200800478
[54] LI X, CHEN D, YANG Y, et al. Comparative transcriptomics analysis reveals differential Cd response processes in roots of two turnip landraces with different Cd accumulation capacities[J]. Ecotoxicology and Environmental Safety,2021:220.
[55] XIAO T, MI M, WANG C, et al. A methionine-R-sulfoxide reductase, OsMSRB5, is required for rice defense against copper toxicity[J]. Environmental and Experimental Botany,2018,153:45−53. doi: 10.1016/j.envexpbot.2018.04.006
[56] 张列, 庹德财, 沈文涛, 等. 番木瓜蛋氨酸亚砜还原酶B1(PaMsrB1)的真核表达及其活性检测[J]. 分子植物育种,2015,13(5):1067−1071. [ZHANG L, XI D C, SGEN W T, et al. Expression and activity analysis of papaya methionine sulfoxide reductase B1 (PaMsrB1) in pichia pastoris[J]. Molecular Plant Breeding,2015,13(5):1067−1071. [57] 徐玉林, 刘春荣. 蛋氨酸亚砜/蛋氨酸亚砜还原酶荧光检测研究进展[J]. 应用化学,2018,35(1):21−27. [XU Y L, LIU C R. Research progress on fluorescence detection of methionine sulfoxide/methionine sulfoxide reductases[J]. Chinese Journal of Applied Chemistry,2018,35(1):21−27. doi: 10.11944/j.issn.1000-0518.2018.01.170338 [58] QIN G Z, MENG X H, WANG Q, et al. Oxidative damage of mitochondrial proteins contributes to fruit senescence: A redox proteomics analysis[J]. Journal of Proteome Research,2009,8(5):2449−2462. doi: 10.1021/pr801046m
[59] MENDEZ A A, PENA L B, BENAVIDES M P, et al. Priming with NO controls redox state and prevents cadmium-induced general up-regulation of methionine sulfoxide reductase gene family in Arabidopsis[J]. Biochimie,2016,131:128−136. doi: 10.1016/j.biochi.2016.09.021
[60] JIAO C, CHAI Y, DUAN Y. Inositol 1,4,5-trisphosphate mediates nitric-oxide-induced chilling tolerance and defense response in postharvest peach fruit[J]. Journal of Agricultural and Food Chemistry,2019,67(17):4764−4773. doi: 10.1021/acs.jafc.9b00153
[61] JIAO C. γ-Aminobutyric acid boosts chilling tolerance by promoting the methionine sulfoxide reductase-thioredoxin reductase system in peach fruit[J]. Horticulture, Environment, and Biotechnology,2022, 63:353−361.
[62] TANG M, XU C, CAO H, et al. Tomato calmodulin-like protein SlCML37 is a calcium (Ca2+) sensor that interacts with proteasome maturation factor SlUMP1 and plays a role in tomato fruit chilling stress tolerance[J]. Journal of Plant Physiology,2021:258−259.





 下载:
下载:
 下载:
下载:
