Hypoglycemic Effects of Polysaccharide from Dolichos lablab L. via Hypothalamic-Pituitary-Adrenal Axis
-
摘要: 本文研究了白扁豆多糖(polysaccharide from Dolichos lablab L.,WHBP)对II型糖尿病大鼠高血糖和下丘脑-垂体-肾上腺(Hypothalamic-Pituitary-Adrenal, HPA)轴的影响。实验通过高脂高糖饮食结合尾静脉注射STZ(30 mg/kg bw)建立II型糖尿病大鼠模型,分别采用WHBP高(WHBPH组,100 mg/kg bw)、中(WHBPM组,50 mg/kg bw)和低(WHBPL组,25 mg/kg bw)三剂量,灌胃剂量为1.5 mL。4周后,测定体重,空腹血糖(Fasting blood-glucose, FBG)、血清胰岛素(Insulin, INS)、促肾上腺皮质激素释放激素(Corticotropin-releasing hormone,CRH)、促肾上腺皮质激素(Adrenocorticotropic hormone,ACTH)和皮质酮(Corticosterone, CORT)含量及SGLT1 mRNA水平。结果显示,WHBP能够显著降低II型糖尿病大鼠FBG水平和血清INS含量(P<0.05),抑制II型糖尿病大鼠体重下降但无统计学意义(P>0.05);WHBP高剂量组能够显著降低II型糖尿病大鼠血清CRH、ACTH和CORT含量(P<0.05),抑制HPA轴亢进。同时,WHBP所有剂量组都能显著抑制小肠组织中的高血糖介导的SGLT1 mRNA高表达水平(P<0.05)。因此,WHBP可通过抑制高血糖介导的HPA轴亢进和小肠组织SGLT1的高表达,减少葡萄糖吸收入血,改善II型糖尿病大鼠胰岛素抵抗水平,发挥降血糖作用。
-
关键词:
- 白扁豆多糖 /
- Ⅱ型糖尿病 /
- 降血糖作用 /
- 下丘脑-垂体-肾上腺轴
Abstract: The present study aimed to investigate hypoglycemic effect of polysaccharide from Dolichos lablab L.(named WHBP) involved in hypothalamic-pituitary-adrenal (HPA) axis in a type II diabetic rat model. In this work, Type II diabetic rat model was established by high fat and high sugar diet combined with the tail vein injection of STZ (30 mg/kg BW), and then these rats were received 1.5 mL of WHBP referring to high (100 mg/kg bw), medium (50 mg/kg bw) and low (25 mg/kg bw) dose of WHBP, respectively. Administration for 4 weeks, the main parameters were examined including body weight, fasting blood glucose (FBG), the serum contents of insulin (INS), corticotropin-releasing hormone (CRH), adrenocorticotropic hormone (ACTH) and corticosterone (CORT). Additionally, the levels of sodium-glucose cotransporter 1 (SGLT1)mRNA was also determined in this work. The results showed that WHBP significantly reduced the levels of FBG and serum INS in type II diabetic rats(P<0.05). Meanwhile, WHBP prevention could inhibit the weight loss in type II diabetic rats, but no significance(P>0.05). Furthermore, high-dose WHBP significantly reduced serum CRH, ACTH and CORT contents in type II diabetic rats(P<0.05), suggesting that the activation of HPA axis was attenuated in the atype II diabetic rats by the treatment of WHBP. Moreover, treatment of the WHBP remarkable decreased the levels of SGLT1 mRNA in type II diabetic rats(P<0.05). Collectively, these results suggested that WHBP treatment could improve hypoglycemic effects through via attenuation of insulin resistance, and HPA axis activation and SGLT1 mRNA expression. -
目前,II型糖尿病在全球范围内蔓延,已成为继肿瘤、心脑血管疾病之后的第三位重大疾病。据不完全统计,截止2019年,我国糖尿病患者人数高达1.164亿人,位列世界第一,在整个糖尿病群体中,II型糖尿病人数占比达90%以上。预计到2030年,我国糖尿病人将达1.54亿,平均每年的医疗费用将达到280亿美元[1-2],严重威胁了人类的生命健康和生活质量。最近研究发现,血液中葡萄糖稳态与神经内分泌免疫网络关系密切。下丘脑在遗传和环境因素共同作用下,可产生“下丘脑唤醒综合征”,激活下丘脑-垂体-肾上腺(hypothalamic-pituitary-adrenal axis, HPA)轴和中枢交感神经系统,引发内分泌系统紊乱和代谢综合征的发生[3-4]。生理水平下,HPA轴参与体内物质代谢、抗炎、抗感染和免疫调节作用等生物学效应,从而维持机体稳态。当机体处于应激或病理情况下,容易诱发HPA轴功能过高,血中皮质激素水平上升,介导蛋白分解氨基酸,促进葡萄糖生成,阻碍胰岛素正常生理功能。肝脏中,皮质激素,通过增强糖异生,导致糖原分解成葡萄糖入血和高血糖的发生与发展[5-6]。因此,尽管目前在糖尿病防治的研究中,有关HPA轴功能的研究较少,但是以HPA轴为靶点,关于神经激素、神经递质及细胞因子的研究已成为以II型糖尿病为典型的代谢综合征研究的一个新方向。
白扁豆又称藊豆、白藊豆、南扁豆,属于豆科类植物,是药食同源的新资源食品。已有动物实验和临床数据显示,白扁豆具有降血糖的作用,可作为糖尿病病人饮食的优先选用食物之一。最近,研究证实白扁豆等组成的复方可通过调节神经系统,发挥抗糖尿病病变的作用[7-8]。白扁豆多糖(polysaccharide from Dolichos lablab L.,WHBP)是从白扁豆成熟种子中提取纯化出的一种主要活性组分。近年来,前期研究发现白扁豆多糖具有降血糖作用,可抑制大脑神经细胞缺氧性凋亡,具有脑保护作用[9]。鉴于此,本研究拟以HPA轴为切入点研究WHBP对Ⅱ型糖尿病大鼠高血糖和下丘脑-垂体-肾上腺轴的影响,基于神经内分泌免疫网络,探讨WHBP降血糖作用机理。
1. 材料与方法
1.1 材料与仪器
白扁豆 中国安徽济顺中药饮片有限公司;链脲佐菌素(streptozocin,STZ) 美国Sigma公司;胰岛素(INS)、促肾上腺皮质激素释放激素(CRH)、促肾上腺皮质激素(ACTH)、皮质酮(CORT)测定试剂盒 中国南京建成生物工程研究所;钠-葡萄糖协同转运蛋白1(SGLT1)引物 中国华大基因科技服务有限公司;Wistar雄性大鼠 体重180~220 g,由北京维通利华实验动物技术有限公司提供,清洁级:SCXK(京)2016-0006。
ACCU-CHEK Performa血糖仪 德国Roche公司;Dimension RXLMAX型全自动生化分析仪 美国德灵诊断产品有限公司;METTLER TOLEDO AL104电子天平 上海梅特勒-托利多仪器有限公司;Millipore超纯水机 美国Millipore公司;3K15-冷冻离心机 美国Sigma公司;Thermo 3001 Varioskan Flash全波长多功能酶标仪 美国Thermo公司。
1.2 实验方法
1.2.1 白扁豆多糖制备
参照文献[10]制备白扁豆多糖,将白扁豆实体进行粉碎后,加入95%乙醇溶液,室温浸泡过夜,过滤液体,收集滤渣,晾干,1:20加入超纯水,100 ℃热水浸提4 h,重复1次,过滤,合并滤液,浓缩,离心,冷冻干燥,结合淀粉酶以及Se-vage法去除淀粉和蛋白质、透析、浓缩、冻干。制备得到的多糖平均分子量约为2.3×105 Da,由葡萄糖、鼠李糖、半乳糖酸、半乳糖、木糖和阿拉伯糖组成[11]。
1.2.2 大鼠的高脂高糖饲养
清洁级Wistar雄性大鼠饲养于清洁卫生的环境,自由饮食饮水。适应性喂养一周后,选取8只大鼠作为正常组(CN组),喂以基础饲料(组成:玉米、豆粕、啤酒酵母粉、进口鱼粉、面粉、氯化钠、豆油、磷酸氢钙、石粉、复合维生素、微量元素、氨基酸等),32只大鼠作为实验组,喂以高糖高脂饲料(66.5%基础饲料、10%猪油、20%蔗糖、2.5%胆固醇、1%胆酸钠)。8周后,所有组大鼠禁食12 h,实验组大鼠尾静脉注射30 mg/kg bwSTZ(溶解在0.1 mol/L柠檬酸-柠檬酸钠缓冲液中,pH为4.4),CN组大鼠注射同等剂量柠檬酸-柠檬酸钠缓冲液。一周后测定空腹血糖(fasting blood glucose,FBG),FBG连续两次超过11.1 mmol/L即造模成功[11-12]。
1.2.3 实验分组
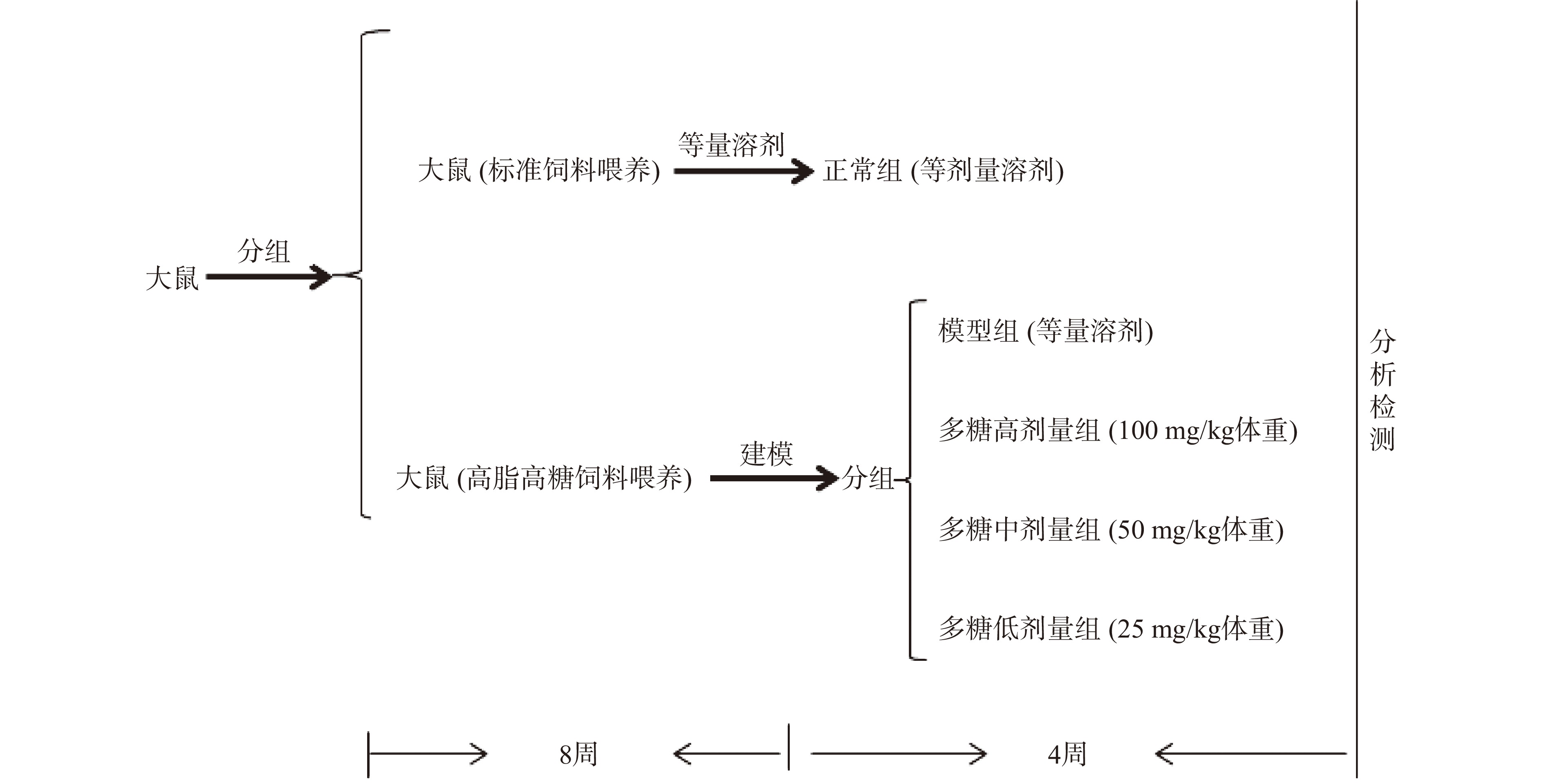
实验总共分为5组,正常饲养的大鼠为CN组。接着,将Ⅱ型糖尿病大鼠随机分为4组:模型组(DM组)、WHBP低剂量组(WHBPL组,WHBP 25 mg/kg bw)、中剂量组(WHBPM组,WHBP 50 mg/kg bw)和高剂量组(WHBPH组,WHBP 100 mg/kg bw),每组8只,将WHBP溶于超纯水中,每日灌胃一次,CN组和DM组给予同等体积超纯水(如图1),记录每周大鼠体重变化。
1.2.4 动物的处理与样本收集
WHBP干预第4周后,所有大鼠禁食12 h后,大鼠进行眼底静脉取血、处死、解剖。收集大鼠血液,小肠组织样品,血液静置2 h后,4 ℃,3500 r/min离心10 min,分离血清,保存在−80 ℃备用。
1.2.5 生化检测
采用全自动生化分析仪检测空腹血糖(FBG),严格按照INS、CRH、ACTH和CORT测定试剂盒说明书检测大鼠血清中的INS、CRH、ACTH和CORT水平。
1.2.6 小肠组织SGLT1 mRNA含量检测
收取小肠组织用RT-PCR检测组织中SGLT1 mRNA含量。冰上分离组织约绿豆大小,加入液氮,快速研磨,Trizol法提取总RNA,紫外分光光度计结合琼脂糖电泳检测RNA质量。SGLT1和β-actin引物序列:正向引物(5’~3’)TGTTGTCCCTGTATGCCTCT,反向引物(3’~5’)TAATGTCACGCACGATTTCC。β-actin引物序列正向引物CAATGAACCGGGAGCCCTTCT,反向引物ACGACGCTGATAGCGAAGAG。应用引物将RNA逆转录后的cDNA实施PCR扩增,收集RT-PCR扩增产物4~6 μL用于琼脂糖凝胶电泳,检测SGLT1和β-actin的mRNA表达[13]。
1.3 数据处理
采用SPSS 21.0软件进行方差齐性检验、单因素方差分析(One-way ANOVA),所有实验数据以平均数±标准差表示。P<0.05表示差异显著,P<0.01表示差异极显著。
2. 结果与分析
2.1 WHBP对II型糖尿病大鼠体重的影响
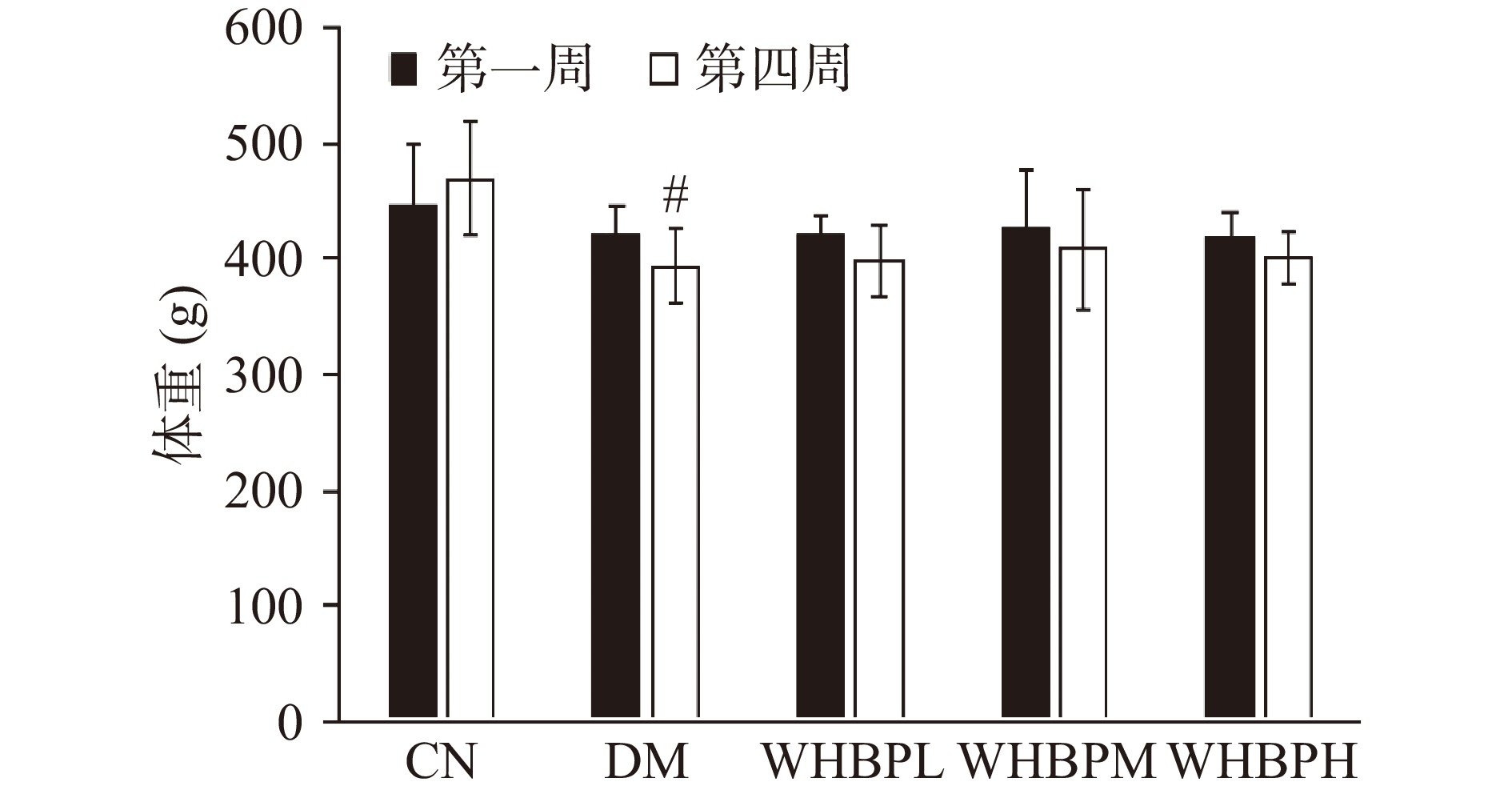
本实验对II型糖尿病大鼠的体重进行了记录,结果如图2所示。CN组大鼠每周体重逐渐上升,相比之下,DM组每周体重一直下降,持续到第四周,而WHBPL组、WHBPM组和WHBPH组体重虽有下降,但相比DM组降幅均有不同程度的减小,且与DM组相比差异不显著(P>0.05)。结果表明WHBP可以改善II型糖尿病大鼠的消瘦程度,但无统计学意义。
2.2 WHBP对II型糖尿病大鼠FBG的影响
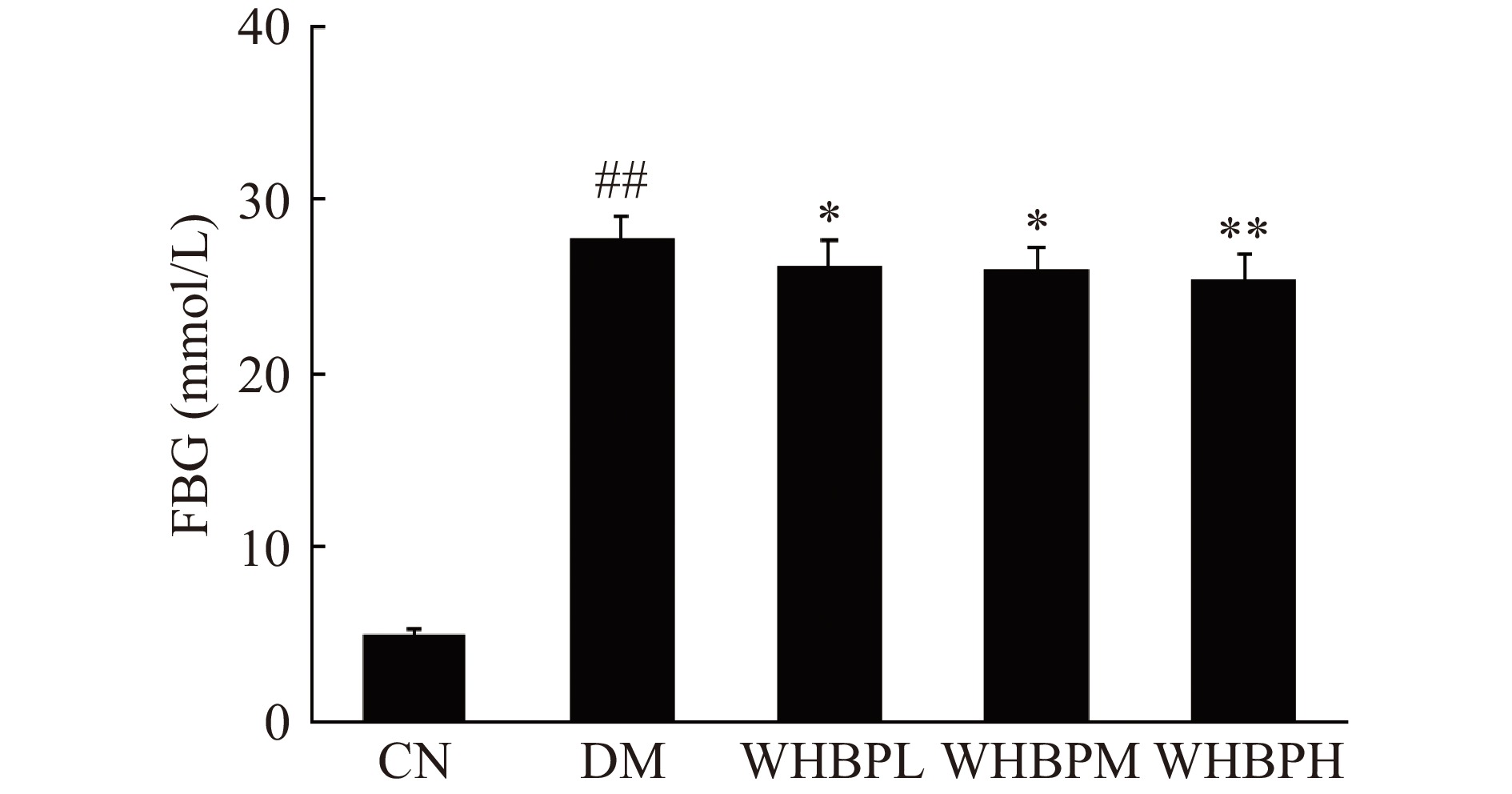
本实验通过FBG指标评价Ⅱ型糖尿病大鼠建模情况及WHBP对Ⅱ型糖尿病大鼠血糖的影响,各组FBG水平如图3所示。数据显示与CN组大鼠相比,DM组大鼠FBG水平极显著增加(P<0.01),大于25 mmol/L,表明糖尿病大鼠血糖水平极高;糖尿病大鼠进行WHBP灌胃干预4周后,WHBPL组和WHBPM组大鼠FBG显著降低(P<0.05),WHBPH组大鼠FBG下降幅度最大,与DM组相比差异极显著(P<0.01)。这些数据表明WHBP对Ⅱ型糖尿病大鼠具有一定的降血糖作用。
2.3 WHBP对II型糖尿病大鼠血清胰岛素INS的影响
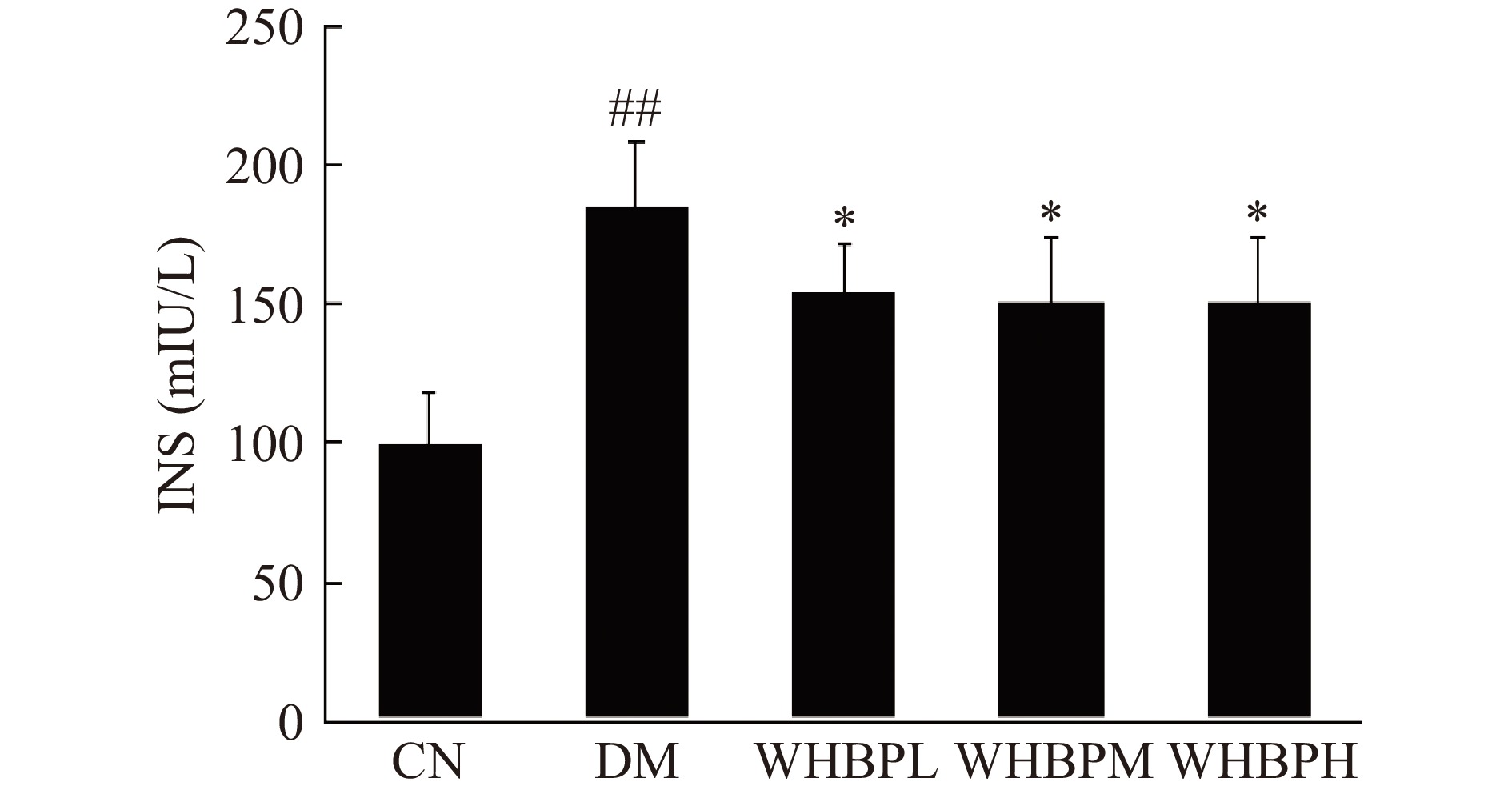
高血糖与INS分泌相对或绝对不足有密切联系,发病初期,持续的高血糖机体出现INS生物效应降低,为了降低血糖,体内出现代偿性高水平分泌INS,然而长期持续的高血糖,机体进入失代偿期,INS出现低水平[5,8]。但机体代偿性的分泌过多INS,以维持血糖的稳定,使靶组织细胞对INS的敏感性降低导致正常量的INS产生的生物学效应低于正常水平、INS促进的葡萄糖摄取和利用效率下降,产生胰岛素抵抗(insulin resistance,IR)。本实验结果(图4)显示,糖尿病建模4周后,与正常组相比,INS分泌水平极显著性增加(P<0.01),表明模型组中呈现高胰岛素血症,提示持续的高血糖机体的体内出现胰岛素敏感性下降,代偿性高水平分泌INS[14-15]。相比之下,灌胃给予WHBP后,与DM组相比,高、中、低剂量组均能显著性(P<0.05)降低糖尿病大鼠血清INS水平,表明WHBP可降低Ⅱ型糖尿病大鼠血清INS水平,抑制IR,抑制血糖紊乱,改善高血糖。
2.4 WHBP对II型糖尿病大鼠HPA轴的影响
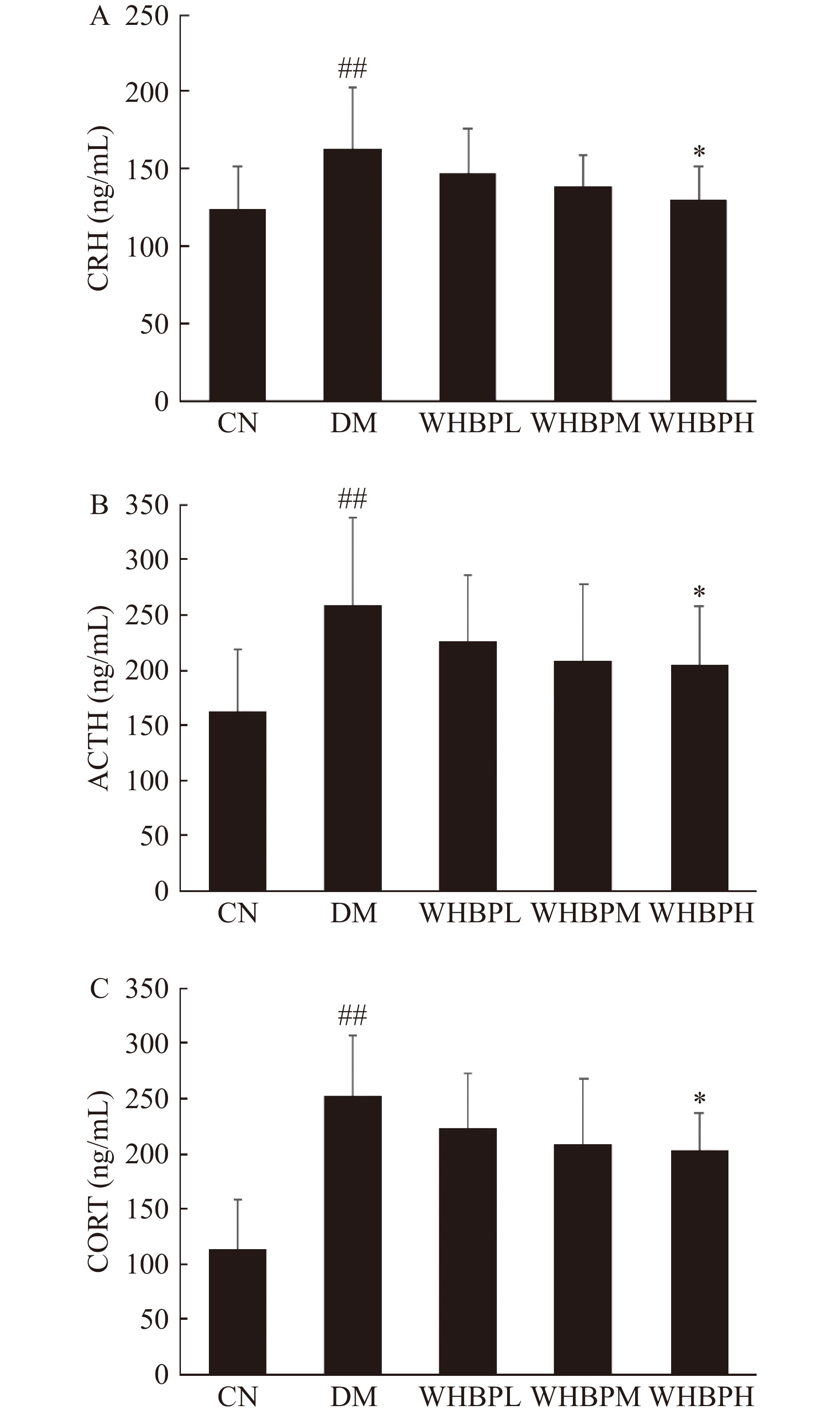
HPA轴的功能活性过高是糖尿病的重要特征和持续性血糖紊乱的重要因素[16]。本实验通过检测CRH、ACTH和CORT水平,评价WHPB对II型糖尿病大鼠HPA轴的影响。本实验结果(图5)显示,与CN相比,II型糖尿病大鼠血清中CRH、ACTH和CORT的含量增加,数据结果具有极显著性差异(P<0.01)。与DM组相比,糖尿病大鼠灌胃给予WHBP 4周后,血清中CRH、ACTH和CORTD的含量呈现下降的趋势,其中WHBPH组中下降趋势最大,具有显著性差异(P<0.05)。结果表明WHBP的降血糖作用,伴随着抑制II型糖尿病大鼠HPA轴的功能过高。
2.5 WHBP对小肠组织SGLT1的影响
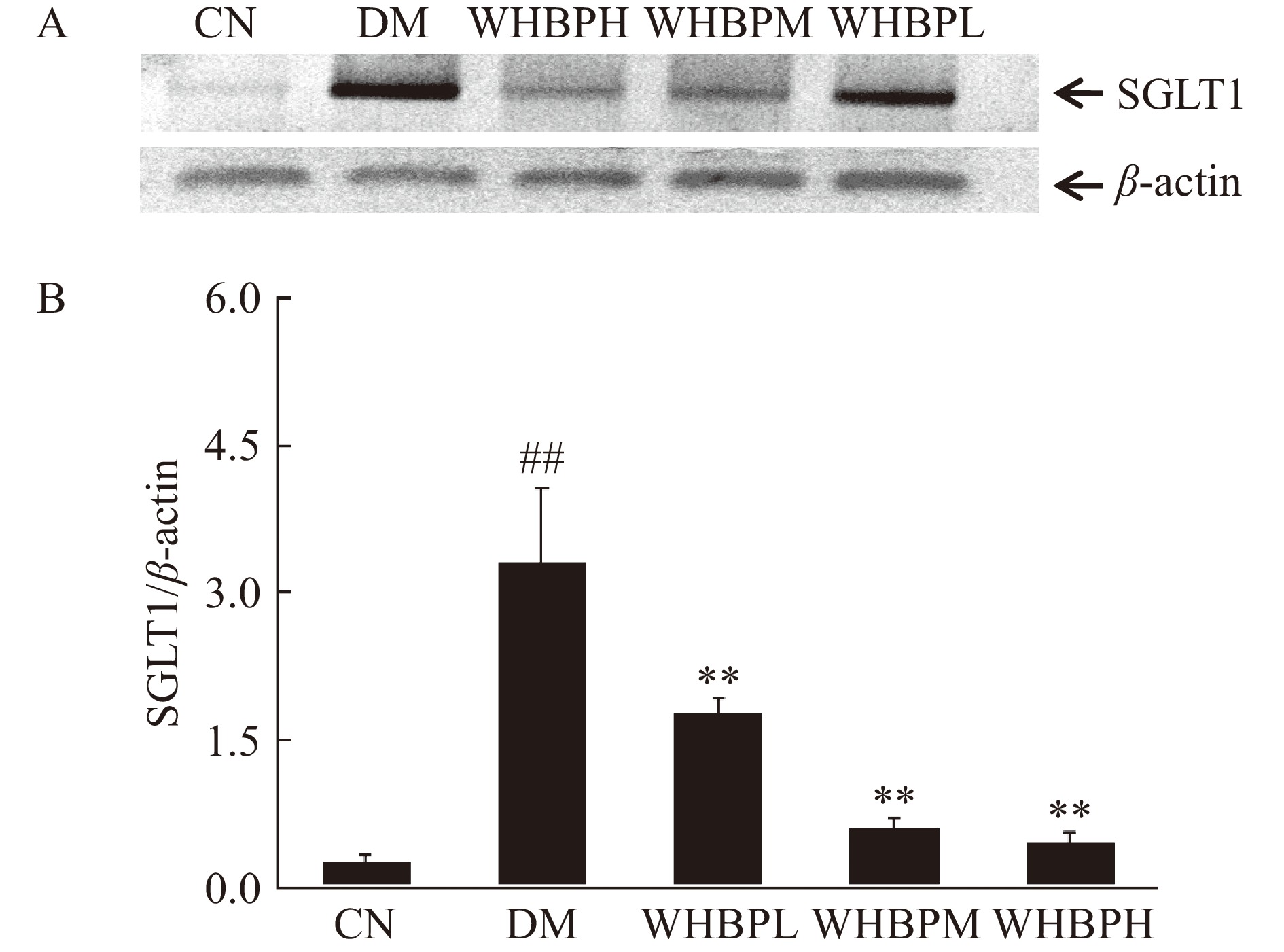
本实验的数据显示(图6),WHBP对II型糖尿病大鼠小肠组织中SGLT1 mRNA表达有影响,通过RT-PCR分析发现,与CN组相比,DM组中SGLT1的mRNA表达水平极显著(P<0.01)增加,WHBP可抑制SGLT1 mRNA的表达。结果表明WHBP能够极显著(P<0.01)抑制SGLT1 mRNA在II型糖尿病大鼠小肠组织的表达。
3. 讨论与结论
碳水化合物是日常主要膳食组成,含有C、H和O,也称糖类化合物。研究已经证实,等量碳水化物被机体消化吸收后血糖反应不同:淀粉类精细碳水化合物是升血糖主要元凶,然而一些复杂的碳水化合物具有降血糖作用[17]。许多干豆富含多糖类复杂碳水化合物,具有降血糖作用,王彤等[18]以馒头作为标准参照食物,观察了Ⅱ型糖尿病患者进食不同干豆后的血糖变化,结果显示进食白扁豆患者的血糖指数显著降低。本实验以来源于白扁豆的WHBP为研究对象,构建Ⅱ型糖尿病大鼠实验动物模型,与白扁豆研究结果相似,WHBP具有降血糖作用。
“三多一少”是II型糖尿病典型的临床症状,“三多”即多饮、多食、多尿,该症状产生的主要原因在于患者无法充分利用葡萄糖,血液中富集的糖分只能依靠尿液排出,导致机体长期处于半饥饿和缺水状态;“一少”即体重减轻,是由于患者糖代谢紊乱,机体主动分解脂肪和蛋白质供能导致日渐消瘦[19]。本实验数据显示,与正常组的体重相比,糖尿病组大鼠的体重显著降低。与之比较,灌胃给予WHBP后,体重下降的降幅有一定的减少,但对体重的改善作用未显示统计学意义。INS分泌障碍是Ⅱ型糖尿病重要病理机制之一,不仅是其发生的驱动因素,而且贯穿于整个病情的发展。发病初期,患者出现INS生物效应降低,此时机体会代偿性分泌更多的INS以维持血糖平衡,但随着病情的发展,患者胰腺组织和胰岛功能逐渐病变,最终出现INS分泌障碍,导致FBG骤升[14,20-21]。胡吉蕾等[14]研究报道,赶黄草水提物可提高Ⅱ型糖尿病大鼠的葡萄糖吸收率和利用率,显著降低INS水平。与前人研究一致,糖尿病大鼠中出现INS分泌障碍,INS水平极显著增加,灌胃给予WHBP后,可降低Ⅱ型糖尿病大鼠血清INS水平,改善IR程度。这些数据表明WHBP能通过抑制INS分泌障碍,发挥降血糖作用。
1977年Besedovsky等[22]提出了神经内分泌免疫调节(NIM)学说,其含义是机体的神经系统、内分泌系统与免疫系统相互作用、相互协调、相互制约,共同调节机体的各项机能活动,以保持内环境平衡与稳定。HPA轴是神经内分泌系统的重要组成部分,主要负责调节机体糖、脂、蛋白质和水盐代谢,通过HPA轴调控血糖稳态的研究为以II型糖尿病为典型的代谢综合征防治研究提供了全新视角。研究显示大多II型糖尿病患者存在HPA轴亢进,主要表现为高CORT血症和ACTH昼夜节律紊乱[23-25]。丁曦等[26]实验发现II型糖尿病大鼠经黄芪多糖干预后,血液CRH、ACTH和CORT含量分别降低了8.08%、21.40%和16.27%。本实验结果显示,糖尿病大鼠中出现CRH、ACTH和CORT水平极显著增加,表明糖尿病大鼠呈现出HPA轴失调。在此基础上灌胃给予WHBP后,可降低血液中CRH、ACTH和CORT水平,这些结果提示,WHBP的降血糖作用与其抑制HPA轴异常有关。
近年来研究发现,大脑与肠道之间可通过血液循环系统、内分泌系统和神经系统,进行相互反馈的“对话”的现象,HPA轴是肠道和中枢神经系统间信息双向交流的重要反馈调节通路,参与并调控生理和病理过程。肠道是人体重要的消化器官,营养物质在肠道中内水解为小分子,小分子通过肠上皮细胞转运进入血液循环,进行生物转化[27-29]。膳食碳水化合物在小肠内水解为以葡萄糖为主的单糖。单糖如葡萄糖作为一种极性分子,在体内需要借助两类特异性载体相互结合,而进入血液循环被人体吸收。SGLT1主要表达于小肠黏膜上皮细胞的刷状缘,是小肠上皮细胞吸收葡萄糖的最主要载体,可在小肠内协助完成葡萄糖的吸收[30-31]。实验结果显示,糖尿病大鼠出现小肠组织中SGLT1表达水平增加。在此基础上灌胃给予WHBP后,可降低肠道组织中SGLT1表达水平,这些结果表明WHBP的降血糖作用与其通过抑制SGLT1表达,减少葡萄糖入血有关。有研究发现,HPA轴的亢进和肠道功能异常是“肠-脑对话”异常的体现[32],本研究显示高血糖介导的HPA轴亢进,伴随着肠上皮葡萄糖转运载体SGLT1表达异常,提示糖尿病的血糖紊乱与“肠-脑对话”异常相关,WHBP可通过抑制HPA轴亢进和肠道中SGLT1高表达,促进正常的“肠-脑对话”,发挥抗糖尿病作用。
总之,本研究采用高脂高糖饮食结合尾静脉注射STZ建立II型糖尿病大鼠模型,实验结果发现WHBP能够缓解II型糖尿病大鼠体重减轻和IR症状,降低FBG水平,验证了WHBP对II型糖尿病大鼠具有一定的降血糖作用。血清CRH、ACTH和CORT数据显示,WHBP还可降低II型糖尿病大鼠血清中CRH、ACTH和CORT含量,对HPA轴功能稳定具有保护作用,进一步SGLT1的mRNA表达数据显示,WHBP可以抑制小肠组织葡萄糖转运载体SGLT1的表达。因此,WHBP的抗糖尿病作用,与其抑制高血糖介导的HPA轴亢进和小肠组织SGLT1的高表达有关。现代医学提出,肠作为一个重要的消化器官之外,生物学界将其定义为人体的“第二大脑”,肠和脑之间通过神经回路,存在复杂的“对话”现象。本研究发现白扁豆多糖的降血糖作用与其抑制HPA轴亢进及减少肠道转运葡萄糖有关,提示的白扁豆降血糖作用模式,存在大脑与肠道相互反馈“对话”的可能,需要进一步研究。
-
-
[1] 甘婷. 糖尿病发生影响因素及其分子机制研究[D]. 兰州: 兰州大学, 2020. GAN T. A study on risk factors and molecular mechanism of diabetes mellitus[D]. Lanzhou: Lanzhou University, 2020.
[2] 孙天慧. 2型糖尿病慢性并发症的临床特点及其影响因素分析[D]. 合肥: 安徽医科大学, 2020. SUN T H. Study of risk factors in type 2 diabetes mellitus (T2DM) with chronic complications[D]. Hefei: Medical University of Anhui, 2020.
[3] FARHANGI M A, JAVID A Z, SARMADI B, et al. A randomized controlled trial on the efficacy of resistant dextrin, as functional food, in women with type 2 diabetes: Targeting the hypothalamic-pituitary-adrenal axis and immune system[J]. Clinical Nutrition,2018,37(4):1216−1223. doi: 10.1016/j.clnu.2017.06.005
[4] BUBLITZ M H, MONTEIRO J F, CARAGANIS A, et al. Obstructive sleep apnea in gestational diabetes: A pilot study of the role of the hypothalamic-pituitary-adrenal axis[J]. Journal of Clinical Sleep Medicine,2018,14(1):87−93. doi: 10.5664/jcsm.6888
[5] 高阳. 超重/肥胖2型糠尿病患者伴焦虑抑郁状态HPA轴功能变化及与中医证型的相关性研究[D]. 成都: 成都中医药大学, 2019. GAO Y. Relationship among functional changes of HPA in overweight/obese patients with type 2 diabetes mellitus with anxiety and depression and its correlation with TCM syndromes[D]. Chengdu: Chengdu University of Chinese Medicine, 2019.
[6] HEPSEN S, SENCAR E, SAKIZ D, et al. Serum cortisol level after low dose dexamethasone suppression test may be predictive for diabetes mellitus and hypertension presence in obese patients: A retrospective study[J]. Diabetes Research and Clinical Practice,2020,161:108081−108089. doi: 10.1016/j.diabres.2020.108081
[7] ZHAOE Y, WEN C, FENG Y, et al. Effects of ultrasound-assisted extraction on the structural, functional and antioxidant properties of Dolichos lablab L. protein[J]. Process Biochemistry,2021,101:274−284. doi: 10.1016/j.procbio.2020.11.027
[8] 易泳鑫. 林兰教授治疗糖尿病周围神经病变经验探讨[D]. 北京: 北京中医药大学, 2016. YI Y X. Professor Linlan's experience in treating diabetic peripheral neuropathy[D]. Beijing: Beijing University of Chinese Medicine, 2016.
[9] 张贤益, 李文娟, 钟亮, 等. 白扁豆多糖对神经细胞缺氧性凋亡的保护机制[J]. 食品科学,2018,39(3):222−228. [ZHANG X Y, LI W J, ZHONG L, et al. Protective mechanism of polysaccharides from Dolichos bean seeds (Dolichos lablab L. ) on hypoxia-induced neuronal apoptosis[J]. Food Science,2018,39(3):222−228. [10] 付王威, 吴睿婷, 万敏, 等. 白扁豆多糖对Ⅱ型糖尿病大鼠的降血糖降血脂作用[J/OL]. 现代食品科技: 1−8[2021-06-12]. https://doi.org/10.13982/j.mfst.1673-9078.2021.8.1201. FU W W, WU R T, WAN M, et al. Hypoglycemic and antihyperlipidemic effects of non-starch polysaccharide from Dolichos lablab L. in type II diabetic rats[J/OL]. Modern Food Science and Technology: 1−8[2021-06-12].https://doi.org/10.13982/j.mfst.1673-9078.2021.8.1201.
[11] 尹术华, 吴文英, 宋也好, 等. 白扁豆非淀粉多糖的理化性质、抗氧化活性及其抑菌性能[J]. 食品工业科技,2020,41(19):39−44. [YIN S H, WU W Y, SONG Y H, et al. Physicochemical properties, antioxidant and antibacterial capacities of non-starch polysaccharide from Dolichos lablab L.[J]. Science and Technology of Food Industy,2020,41(19):39−44. [12] BAI Z, MENG J, HUANG X, et al. Comparative study on antidiabetic function of six legume crude polysaccharides[J]. International Journal of Biological Macromolecules,2020,154:25−30. doi: 10.1016/j.ijbiomac.2020.03.072
[13] 李青. AE2蛋白在高糖诱导内皮细胞凋亡中的作用[D]. 南昌: 南昌大学, 2007. LI Q. Role of anion exchanger-2(AE2) in apoptosis of endothelial cells induced by hyperglucose[D]. Nanchang: Nanchang University, 2007.
[14] 胡吉蕾, 郑乐愉, 唐薇, 等. 赶黄草水提物对高脂饮食联合STZ诱导的Ⅱ型糖尿病大鼠的降血糖作用[J]. 现代食品科技,2020,36(2):25−31. [HU J L, ZHENG L Y, TANG W, et al. Hypoglycemic effects of extracts of Penthorum chinense Pursh in high fat diet and streptozotocin-induced type Ⅱ diabetic rats[J]. Modern Food Science and Technology,2020,36(2):25−31. [15] CHEN Z, WANG C, PAN Y, et al. Hypoglycemic and hypolipidemic effects of anthocyanins extract from black soybean seed coat in high fat diet and streptozotocin-induced diabetic mice[J]. Food & Function,2018,9(1):426−439.
[16] SHIN W Y, AN M J, IM N G, et al. Changes in blood glucose level after steroid injection for musculoskeletal pain in patients with diabetes[J]. Annals of Rehabilitation Medicine,2020,44(2):117. doi: 10.5535/arm.2020.44.2.117
[17] 李露, 张贤益, 汤小芳, 等. 膳食中碳水化合物与代谢综合征的研究进展[J]. 食品科学,2019,40(7):268−273. [LI L, ZHANG X Y, TANG X F, et al. Advances in understanding dietary carbohydrates and metabolic syndrome[J]. Food Science,2019,40(7):268−273. doi: 10.7506/spkx1002-6630-20171210-117 [18] 王彤, 何志谦, 梁奕铨. 干豆对糖尿病患者血糖指数和C肽的影响[J]. 营养学报,1998(4):44−49. [WANG T, HE Z Q, LIANG Y Q. Effects of dried beans on glycemic index and C peptide in patients with diabetes mellitus[J]. Journal of Nutrition,1998(4):44−49. [19] 舒丹阳, 熊犍, 刘鹏展, 等. 沙棘籽蛋白肽对db/db小鼠降血糖活性及肾脏保护作用[J]. 食品工业科技,2020,41(21):317−321. [SHU D Y, XIONG J, LIU Z P, et al. Hypoglycemic activity and renal protection effect of seabuckthorn seed protein peptide in db/db mice[J]. Science and Technology of Food Industy,2020,41(21):317−321. [20] 姜少磊, 刘兵峰, 刘钟栋. 食用索马甜对小鼠血糖及血脂的影响[J]. 食品工业科技,2020,41(8):196−201. [JIANG S L, LIN B F, LIU Z D. Effects of Thaumatin on blood glucose and blood lipid in mice[J]. Science and Technology of Food Industy,2020,41(8):196−201. [21] CERFM E. Beta cell physiological dynamics and dysfunctional transitions in response to islet inflammation in obesity and diabetes[J]. Metabolites,2020,10(11):452. doi: 10.3390/metabo10110452
[22] BESEDOVSKY H, SORKIN E. Network of immune-neuroendo-crine interactions[J]. Clin Exp Lm Munol,1977,27(1):1−12.
[23] ZHANG H N, YU X B, TANG C R, et al. Atorvastatin ameliorates depressive behaviors and neuroinflammatory in streptozotocin-induced diabetic mice[J]. Psychopharmacology,2020,237(3):695−705. doi: 10.1007/s00213-019-05406-w
[24] LIN Y, ZHANG Z, WANG S, et al. Hypothalamus-pituitary-adrenal axis in glucolipid metabolic disorders[J]. Reviews in Endocrine and Metabolic Disorders,2020,21(4):421−429. doi: 10.1007/s11154-020-09586-1
[25] MOSILIi P, MKHIZE B C, NGUBANE P, et al. The dysregulation of the hypothalamic-pituitary-adrenal axis in diet-induced prediabetic male Sprague Dawley rats[J]. Nutrition & Metabolism,2020,17(1):1−12.
[26] 丁曦, 姚定国. 黄芪多糖对2型糖尿病大鼠HPA轴及海马糖皮质激素受体水平的调节作用[J]. 江西中医学院学报,2013,25(5):58−60. [DING X, YAO D G. Regulating effect of APS on the expression levels of HPA axis and GR mRNA in the hippocampus of type 2 diabetic rats[J]. Journal of Jiangxi University of Traditional Chinese Medicine,2013,25(5):58−60. [27] JAZANI N H, SAVOJ J, LUSTGARTEN M, et al. Impact of gut dysbiosis on neurohormonal pathways in chronic kidney disease[J]. Diseases,2019,7(1):21−28. doi: 10.3390/diseases7010021
[28] CUSSOTTO S, SANDHU K V, DINAN T G, et al. The neuroendocrinology of the microbiota-gut-brain axis: A behavioural perspective[J]. Frontiers in Neuroendocrinology,2018,51:80−101. doi: 10.1016/j.yfrne.2018.04.002
[29] WU Q, XU Z, SONG S, et al. Gut microbiota modulates stress-induced hypertension through the HPA axis[J]. Brain Research Bulletin,2020,162:49−58. doi: 10.1016/j.brainresbull.2020.05.014
[30] KOEPSELL H. The Na+-D-glucose cotransporters SGLT1 and SGLT2 are targets for the treatment of diabetes and cancer[J]. Pharmacology & Therapeutics,2017,170:148−165.
[31] DEGEN A S, KRYNYTSKA I Y, KAMYSHNYI A M. Changes in the transcriptional activity of the entero-insular axis genes in streptozotocin-induced diabetes and after the administration of TNF-α non-selective blockers[J]. Endocrine Regulations,2020,54(2):1−5.
[32] WILEY J W, HIGGINS G A, ATHEY B D. Stress and glucocorticoid receptor transcriptional programming in time and space: Implications for the brain-gut axis[J]. Neurogastroenterol Motil,2016,28(1):12−25. doi: 10.1111/nmo.12706





 下载:
下载:
 下载:
下载:
